Оглавление:



Сложные эфиры
- Эфиры Сложные эфиры содержат органические вещества, которые образуются в результате реакции кислот со спиртом с удалением воды. Общая формула эфира-R-C. хо-Р R ’представляет собой углеводородную группу, которая может быть разной и одинаковой.
- Долгое время ученые считали, что при взаимодействии кислот и спиртов водород следует отделять от молекулы кислоты, а гидроксильную группу-от молекулы спирта. Однако, используя изотоп кислорода с атомной массой 18, ученым удалось установить, что гидроксильная группа отделена от молекулы карбоновой кислоты. ^ «<Адрес>». R_C (+Н40-Р ’ 4±Р-С; + Н2О O-H SO-R ’ Номенклатура.
Название эфира происходит от названия соответствующей кислоты и спирта. Людмила Фирмаль
Пример: Этилацетат. Или этиловый эфир уксусной кислоты Изопентилацетат. Или эфиры эзокса Торна уксусной кислоты Быть на природе. Сложные эфиры содержатся в цветах, фруктах и ягодах, которые определяют специфический запах. Мы получили ваши отзывы. Сложные эфиры в лабораторных условиях получают в основном взаимодействием спирта с карбоновыми кислотами в присутствии концентрированной серной кислоты.
CH3-cf + H-O-C2H5 ^^ CH3-cf 4-H20 Чон Хо-C2H5 Реакция образования сложных эфиров называется реакцией этерификации(от этерификации-эфир).Реакция этерификации обратима. Концентрированная серная кислота в сочетании с водой обычно используется для смещения равновесия этой реакции в сторону получения сложных эфиров.
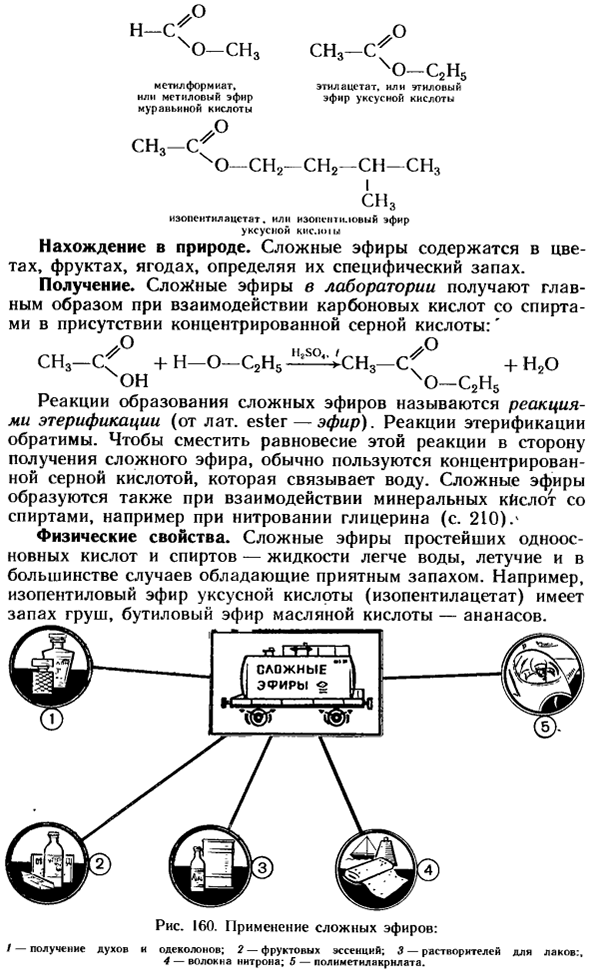
Сложные эфиры образуются также при взаимодействии минеральных кислот и спиртов, например, при нитровании глицерина(С. 210).Четыре Физические характеристики. Простейшие одноосновные и спиртовые эфиры-жидкость легче воды, Летучая и в большинстве случаев обладает приятным ароматом. Например, сложные эфиры изопентилацетата (изопентилацетат) имеют грушевый запах, сложные эфиры масляной кислоты-ананасовый. Рисунок 160.
- Использование сложных эфиров: / — Получить одеколон с духами. 2 — фруктовая эссенция; 3-растворитель, длина лака: 4-Нитронное волокно; 5-метилакрилат в комплекте. Метиловый эфир формиата Авед или Мурановой кислоты Об Эстере Температура кипения и плавления сложных эфиров ниже, чем у соответствующих органических кислот. Только низкомолекулярные эфиры воды растворимы в воде.
Химическое свойство. Свойством сложных эфиров является их взаимодействие с водой (гидролиз). СН3—CfHOH СН3—С1^+С2Н5ОН 0-C2H5OH Этилацетат」 Применение (рисунок 160).Эфиры используются в качестве добавки при производстве прохладительных напитков, сладостей и других пищевых продуктов, а также парфюмерии.
В естественных условиях эфир легко гидролизуется ферментами. Людмила Фирмаль
Некоторые из них являются растворителями лака. • Метилметакрилат СН2 = СН-Эстер и хо-СН3 Метилметакрилат ч ^ с-МН ГнГН3 и-1 Plastic производство пластмасс. G. схема генетической связи между эфирами и другими классами органических веществ 55 (стр. 233). Ответьте на вопрос, упражнение 1-8 (стр. 1м2).Решите задачу I и 2(стр. 242).
Смотрите также:
| Одноосновные предельные карбоновые кислоты | Жиры |
| Краткие сведения о непредельных карбоновых кислотах | Глюкоза |
Если вам потребуется помощь по химии вы всегда можете написать мне в whatsapp.

