Оглавление:


Молярная масса
- Молярная масса Как уже говорилось, в химических реакциях количество веществ должно учитываться в moles. To для этого нужно уметь выражать массу вещества в граммах и наоборот, от выражения количества вещества в моле.
- Для этой цели используется понятие молярной (или молярной) массы вещества. Молярная масса вещества равна массе 1 моля конкретного вещества. Молярная масса M представлена 1 граммом на моль (г / моль). Если масса вещества задана, то ее отношение к соответствующему количеству (молю) данного вещества есть определенная величина, то есть молярная масса данного вещества.
Где m-масса в граммах, а V-количество вещества в молях. Людмила Фирмаль
Пример: AL / s s \ 264 g 176 g 88 g 00、 M (FeS) — = — = — m — = 88 г / моль x ’3 моль 2 моль I моль’ Численное значение молярной массы вещества совпадает с численным значением массы молекулы (атома) и относительной молекулярной (атома) массой (табл.17). Однако следует отметить, что понятия»молекулярная масса»,»относительная молекулярная масса»и»молярная масса» совершенно различны concepts.
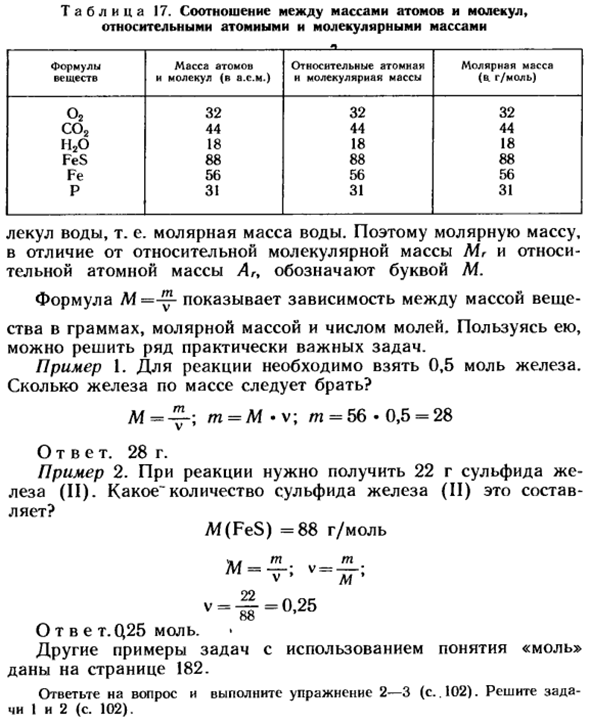
So например, для воды число 18 (то есть относительная молекулярная масса воды) указывает на то, во сколько раз вода 1 молекулы тяжелее единицы массы атома, а для 18 г воды-6,02•1023 МО.- Таблица 17.Масса атомов и молекул, относительная атомная масса и молекулярная масса
- Формула масса джатмон относительная атомная молярная масса Вещества и молекулы (а. с. м. и молекулярная масса (в г / моль) О2 32 32 32 32 ко 44 44 44 44 Н2О 18 18 18 18 ФЭС 88 88 88 88 Фе 56 56 56 П 31 31 31 Молекулы воды, а именно молярная масса воды. Таким образом, молярная масса обозначается буквой M, в отличие от относительной молекулярной массы Mr и относительной атомной массы Ar.
Формула M показывает соотношение между массой вещества (грамм), молярной массой и числом молей. С его помощью можно решить несколько действительно важных задач. Пример 1.Сколько я должен взять железа? м = м * в; ш = 56 * 0.5 = 28 Ответ. 28 г. Пример 2.
Для реакции следует использовать железо 0,5 моль. Людмила Фирмаль
В ходе реакции необходимо получить 22 г сульфида железа (II).Каково количество сульфида железа (II)? M (FeS)= 88 г /моль ш м т т т М = в = ЛГ: с V — £ 0.25 Т. видно из вопроса 25 мол. Другие примеры задач, использующих термин «кроты», перечислены на стр. 182. Отвечая на этот вопрос, выполните упражнение 2-3(стр..102).Решите задачи 1 и 2(стр. 102).
Смотрите также:
| Соли | Закон Авогадро |
| Моль — единица количества вещества | Объемные отношения газов при химических реакциях |
Если вам потребуется заказать решение по химии вы всегда можете написать мне в whatsapp.

