Оглавление:
Способы выражения состава раствора
Задача 11.
Реакция с участием FeCl3 протекает по уравнению: 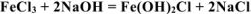 . Определить массу хлорида железа (III), содержащуюся в 200 см3 0,1 н раствора хлорида железа (III)
. Определить массу хлорида железа (III), содержащуюся в 200 см3 0,1 н раствора хлорида железа (III)

Решение:
Молярную концентрацию эквивалентов 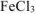 определяем по формуле
определяем по формуле
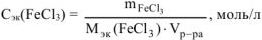
откуда 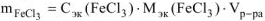
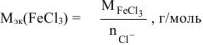
где 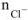 — число ионов
— число ионов 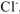 , замещенных в данной реакции на
, замещенных в данной реакции на 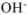
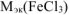 -молярная масса эквивалентов хлорида железа (III), г/моль,
-молярная масса эквивалентов хлорида железа (III), г/моль,

 — молярная масса хлорида железа (III), г/моль
— молярная масса хлорида железа (III), г/моль
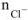 = 2, так как в данной реакции два иона хлора замещаются на 2 иона
= 2, так как в данной реакции два иона хлора замещаются на 2 иона 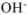
Тогда 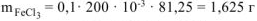
где 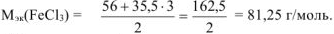
где 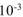 — пересчет
— пересчет 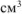 в л.
в л.
Ответ: 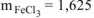 г.
г.
Задача 12.
Сколько граммов хлорида магния потребуется для приготовления 800 см3 25%-ного водного раствора плотностью 1,2 г/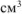 ?
?

Решение:
Массовая доля 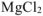 равна:
равна:
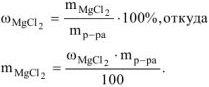
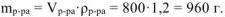
Откуда: 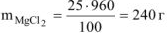
Ответ: 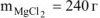
Задача 13.
Определить массу сульфата меди (II), содержащуюся в 800 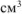 0,3 М водного раствора сульфата меди (II).
0,3 М водного раствора сульфата меди (II).

Решение:
Молярную концентрацию 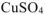 определяем по формуле:
определяем по формуле:
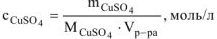
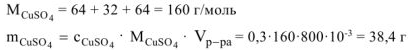
где 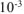 — пересчет
— пересчет 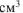 в л.
в л.
Ответ: 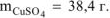 .
.
Задача 14.
Определить моляльность вещества в водном растворе, если в 100 г раствора содержится 5,3 г карбоната натрия.
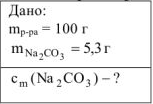
Решение:
Моляльность 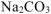 в растворе определяем по формуле:
в растворе определяем по формуле:
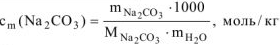
Массу воды определяем из условия:
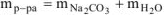
Тогда 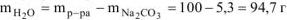
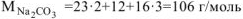
Следовательно, 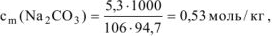
где 1000 — коэффициент пересчета г в кг.
Ответ: 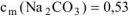 моль/кг.
моль/кг.
Задача 15.
Определить титр раствора вещества, если в 200 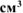 раствора содержится 0,1 моль гидроксида калия.
раствора содержится 0,1 моль гидроксида калия.
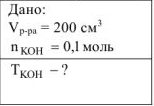
Решение:
Титр раствора вещества определяем по формуле:
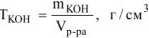
Согласно условию задачи: 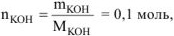 , откуда
, откуда 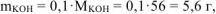 , где
, где 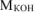 — молярная масса гидроксида калия, г/моль
— молярная масса гидроксида калия, г/моль
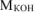 = 39 + 16 + 1 = 56 г/моль.
= 39 + 16 + 1 = 56 г/моль.
Следовательно, 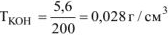
Ответ: 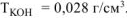 .
.
Задача 16.
Определить молярную долю растворенного вещества в 3,42%-ном водном растворе сахарозы 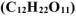 .
.

Решение:
Молярную долю сахарозы в растворе определяем по формуле:
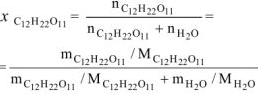
где:
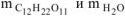 ’ соответственно массы сахарозы и воды, г
’ соответственно массы сахарозы и воды, г
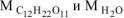
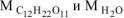 соответственно молярные массы сахарозы и воды, г/моль
соответственно молярные массы сахарозы и воды, г/моль
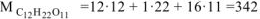 г/моль
г/моль
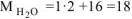 г/моль
г/моль
Согласно условия задачи, в 100 г раствора содержится 3,42 г 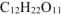 .
.
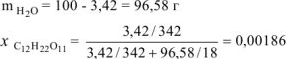
Ответ: 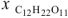 =0,00186.
=0,00186.
Задача 17.
Плотность 6% водного раствора ортофосфорной кислоты равна 1,031 г/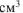 . Рассчитать:
. Рассчитать:
а) молярную концентрацию ;
б) моляльность;
в) молярную долю кислоты в растворе.

Решение:
а) Молярную концентрацию кислоты определяем по формуле:
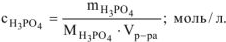
Согласно условию задачи в 100 г раствора содержится 6 г 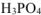 . Тогда 6 г
. Тогда 6 г 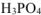 содержится в объеме раствора
содержится в объеме раствора
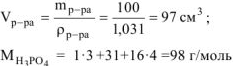
Следовательно, 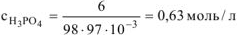 ,
,
где 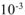 — пересчет
— пересчет 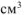 в л.
в л.
б) моляльность кислоты в растворе определяем по формуле:
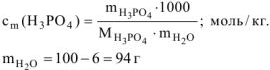
Тогда 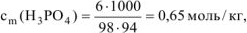 ,
,
где 1000 — коэффициент пересчета г в кг.
в) молярную долю кислоты определяют по формуле:

Ответ: 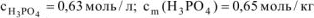 ;
;
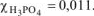
Задача 18.
Определить объем 16%-ного раствора карбоната калия плотностью 1,149 г/ , необходимого для приготовления 3 л 0,2 М водного раствора данного вещества. Пояснить процесс приготовления раствора.
, необходимого для приготовления 3 л 0,2 М водного раствора данного вещества. Пояснить процесс приготовления раствора.

Решение:
а) Молярную концентрацию карбоната калия определяем по формуле:
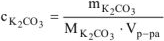
Следовательно:
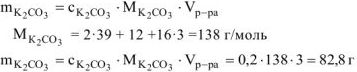
Рассчитываем массу 16%-ного раствора 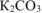 , который содержит 82,8 г
, который содержит 82,8 г 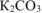 .
.
Составляем пропорцию:
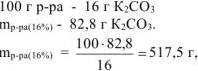
Определим объём 16% — ного раствора:
м
Ответ: для приготовления 3 л 0,2 М раствора 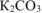 нужно взять 450,4 мл 16%-ного раствора
нужно взять 450,4 мл 16%-ного раствора 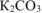 и разбавить его водой до 3 л.
и разбавить его водой до 3 л.
Задача 19.
Найти массы воды и кристаллогидрата 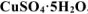 , необходимые для приготовления 2 литра раствора, содержащего 8% мае. безводной соли. Плотность 8%-го раствора
, необходимые для приготовления 2 литра раствора, содержащего 8% мае. безводной соли. Плотность 8%-го раствора 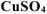 равна 1,084 г/
равна 1,084 г/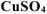 .
.

Решение:
Массу безводной соли 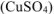 , необходимую для приготовления заданного раствора определяем из формулы:
, необходимую для приготовления заданного раствора определяем из формулы:
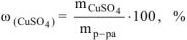
откуда 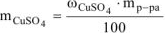
Масса раствора равна
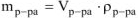
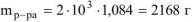
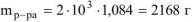 , где
, где 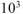 коэффициент перевода л в
коэффициент перевода л в 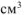 . Тогда масса
. Тогда масса 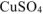 в растворе составляет:
в растворе составляет:
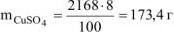
Массу 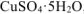 , содержащую 86,7 г
, содержащую 86,7 г 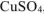 , определяем из пропорции:
, определяем из пропорции:

где
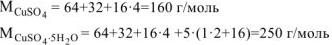
Тогда
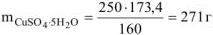
Зная массу раствора и кристаллогидрата, определяем массу воды, необходимую для приготовления заданного раствора:
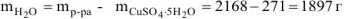
Ответ: 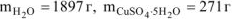
Эти задачи взяты со страницы готовых задач по предмету химия:
Возможно эти страницы вам будут полезны:

