Оглавление:

Здравствуйте, на этой странице я собрала краткий курс лекций по предмету «материаловедение».
Лекции подготовлены для студентов любых специальностей и охватывает полный курс предмета «материаловедение».
| Если что-то непонятно — вы всегда можете написать мне в WhatsApp и я вам помогу! |
Материаловедение (от рус. материал и ведать) — междисциплинарный раздел науки, изучающий изменения свойств материалов как в твёрдом, так и в жидком состоянии в зависимости от некоторых факторов. К изучаемым свойствам относятся: структура веществ, электронные, термические, химические, магнитные, оптические свойства этих веществ. Материаловедение можно отнести к тем разделам физики и химии, которые занимаются изучением свойств материалов. Кроме того, эта наука использует целый ряд методов, позволяющих исследовать структуру материалов. При изготовлении наукоёмких изделий в промышленности, особенно при работе с объектами микро- и наноразмеров необходимо детально знать характеристику, свойства и строение материалов. Решить эти задачи и призвана наука — материаловедение.wikipedia.org/wiki/Материаловедение
Введение в материаловедение
Материаловедение — это наука о связи между составом, структурой и свойствами. материалы и закономерности их изменения во внешних физико-химических условиях последствий.
Все химические материалы разделены на две основные группы — металлический и неметаллический. Металлические включает в себя металлы и их сплавы.
Металлы составляют более 2/3 всех известных химических элементов. В свою очередь, металлические материалы делятся на черные и цветные. К черным материалам относятся чугун и сплавы на его основе — сталь и чугун.
Все другие металлы классифицируются как цветные. Чистые металлы имеют низкое содержание механические свойства по сравнению с сплавами, и поэтому их применение ограничено теми случаями, когда необходимо использовать их особые свойства (например, магнитные или электрические).
Практическое значение различных металлов не является одинаковым. Самым большим из них является. черные металлы были приобретены для использования в машиностроении. На основе железа производить более 90% всей металлопродукции. Однако цветные металлы имеют ряд ценных физических и химических свойств, которые делают их ценными. незаменимый. Из цветных металлов наибольшее промышленное значение имеют следующие алюминий, медь, магний, титан и др.
Помимо металла, значительное место в промышленности занимает различные неметаллические материалы — пластмассы, керамика, резина и др. Они . производство и применение в настоящее время разрабатываются с опережением графика по сравнению с металлическими материалами. Но использование их в промышленности невелико (до 10%) и прогноз 30-ти летней давности о том, что неметаллические материалы значительно выдавливаются к концу века металлическими, не оправдался.
Основные теоретические сведения о теории сплавов.
Фазовый состав сплавов
Сплавами называются вещества, полученные сплавлением или спеканием из двух и более элементов. В сплавах элементы могут по-разному взаимодействовать между собой, образуя различные по химическому составу, типу связи и строению кристаллические фазы. Фазой называется однородная часть системы, отделенная от других частей системы поверхностью раздела, имеющая одинаковые состав, строение и свойства. В зависимости от атомно-кристаллической структуры различают твердые растворы и химические соединения.
Твердыми растворами называют кристаллы, в которых сохраняется тип кристаллической решетки элемента-растворителя. Твердые растворы являются кристаллическими фазами переменного состава. Если твердый раствор состоит из двух элементов 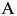 и
и 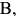 то атомы растворенного элемента
то атомы растворенного элемента 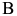 (или
(или 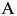 ) размещаются в кристаллической решетке растворителя — элемента
) размещаются в кристаллической решетке растворителя — элемента 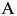 (или
(или 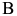 ), замещая атомы в узлах решетки или внедряясь между узлами. В первом случае кристаллы называют твердыми растворами замещения, во втором — твердыми растворами внедрения.
), замещая атомы в узлах решетки или внедряясь между узлами. В первом случае кристаллы называют твердыми растворами замещения, во втором — твердыми растворами внедрения.
Твердые растворы обозначаются буквами греческого алфавита: 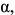
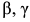 и т. д.
и т. д.
Кристаллы, образованные различными элементами, вступившими в химическую связь и имеющие собственный тип кристаллической решетки, отличающийся от решеток, составляющих их элементов, называются химическими соединениями.
Строение металлических сплавов зависит от того, в какие взаимодействия вступают компоненты, их образующие. Структура характеризует форму, размеры и взаимное расположение фаз в сплаве.
При кристаллизации сплавов могут образоваться однородные твердые растворы, химические соединения и смеси различных фаз. Эти сведения можно получить из анализа диаграмм состояния, изучению которых посвящена эта глава.
Диаграмма состояния представляет собой графическое изображение фазового состава сплавов данной системы в функции температуры и химического состава сплавов. Диаграмма состояния двухкомпонентной системы строится в координатах температура — химический состав сплава (рис. 1.1).
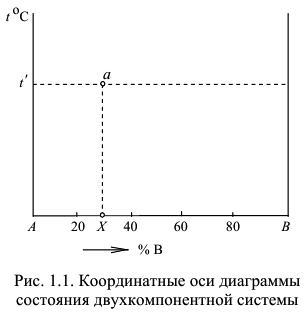
В точках 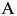 и
и 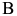 проходят вертикальные оси, между которыми расположена диаграмма состояния компонентов
проходят вертикальные оси, между которыми расположена диаграмма состояния компонентов 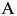 к
к 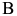 . Точки абсциссы
. Точки абсциссы 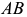 соответствуют составам сплавов компонентов
соответствуют составам сплавов компонентов 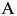 и
и 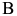 которые выражаются через содержание одного из компонентов (например, компонента
которые выражаются через содержание одного из компонентов (например, компонента 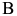 ). При этом величина отрезка
). При этом величина отрезка 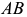 принимается за 100% компонента
принимается за 100% компонента 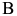 (или
(или 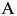 ).
).
Так, сплав 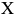 , указанный на рис. 1.1, содержит
, указанный на рис. 1.1, содержит 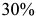 компонента
компонента 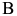 и
и 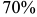 компонента
компонента 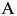 .
.
Диаграмма состояния двухкомпонентной системы с неограниченной растворимостью компонентов в жидком и твердом состояниях
Диаграмма состояния двухкомпонентной системы с неограниченной растворимостью компонентов в жидком и твердом состояниях представлена на рис. 1.2. На диаграмме состояния имеются две линии: 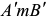 — линия температур начала кристаллизации (конца плавления) сплавов, или линия ликвидуса а твердого раствора;
— линия температур начала кристаллизации (конца плавления) сплавов, или линия ликвидуса а твердого раствора; 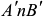 — линия температур конца кристаллизации (начала плавления), или линия солидуса
— линия температур конца кристаллизации (начала плавления), или линия солидуса  твердого раствора. Эти линии делят всю диаграмму состояния на три фазовые области. Выше линии ликвидуса располагается область однофазных жидких растворов, ниже солидуса — область однофазных твердых растворов. Между линиями ликвидуса и солидуса находится двухфазная область
твердого раствора. Эти линии делят всю диаграмму состояния на три фазовые области. Выше линии ликвидуса располагается область однофазных жидких растворов, ниже солидуса — область однофазных твердых растворов. Между линиями ликвидуса и солидуса находится двухфазная область 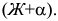
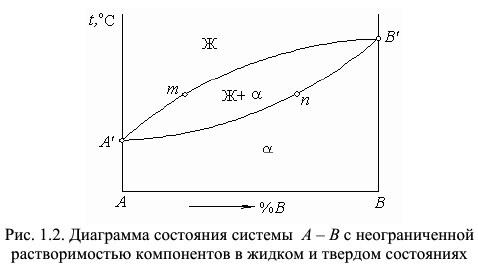
Рассмотрим процессы, которые будут происходить в сплаве 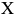 при его равновесном охлаждении (рис. 1.3, а). При охлаждении образца, находящегося в жидком состоянии, до комнатной температуры в сплаве будут наблюдаться две критические точки (
при его равновесном охлаждении (рис. 1.3, а). При охлаждении образца, находящегося в жидком состоянии, до комнатной температуры в сплаве будут наблюдаться две критические точки (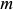 и
и 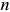 ), соответствующие температурам
), соответствующие температурам 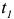 и
и 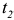 . В исходном состоянии сплав представляет собой жидкий раствор, состав которого соответствует составу сплава. При охлаждении образца сплава до температуры первой критической точки
. В исходном состоянии сплав представляет собой жидкий раствор, состав которого соответствует составу сплава. При охлаждении образца сплава до температуры первой критической точки 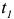 сплав будет оставаться однофазным.
сплав будет оставаться однофазным.
При температуре 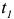 из жидкого раствора, состав которого отвечает точке
из жидкого раствора, состав которого отвечает точке 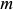 , начнут выделяться кристаллы
, начнут выделяться кристаллы  твердого раствора, состав которых соответствует точке
твердого раствора, состав которых соответствует точке 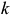 . Произойдет изменение фазового состояния сплава, он станет двухфазным, начнется процесс кристаллизации. Температура
. Произойдет изменение фазового состояния сплава, он станет двухфазным, начнется процесс кристаллизации. Температура 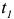 — температура ликвидуса сплава
— температура ликвидуса сплава 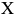 .
.
Фигуративная точка, отвечающая жидкой фазе, при понижении температуры будет перемещаться от точки 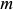 вниз по кривой ликвидуса, а фигуративная точка, соответствующая
вниз по кривой ликвидуса, а фигуративная точка, соответствующая  твердому раствору, — от точки
твердому раствору, — от точки 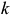 вниз по кривой солидуса. При какой-то промежуточной температуре
вниз по кривой солидуса. При какой-то промежуточной температуре 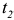 составы находящихся в равновесии жидкой и твердой фаз будут описываться фигуративными точками
составы находящихся в равновесии жидкой и твердой фаз будут описываться фигуративными точками 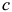 и
и 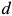 , а состояние сплава
, а состояние сплава 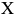 — фигуративной точкой
— фигуративной точкой 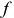 . Отрезок
. Отрезок 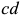 , соединяющий фигуративные точки равновесных фаз, носит название коноды. Количество каждой из равновесных фаз в рассматриваемом сплаве может быть определено по правилу рычага. Если принять за точку опоры мысленного рычага
, соединяющий фигуративные точки равновесных фаз, носит название коноды. Количество каждой из равновесных фаз в рассматриваемом сплаве может быть определено по правилу рычага. Если принять за точку опоры мысленного рычага 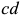 фигуративную точку
фигуративную точку 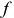 , согласно правилу рычага отношение масс фаз будет обратно отношению отрезков от точки
, согласно правилу рычага отношение масс фаз будет обратно отношению отрезков от точки 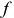 до фигуративных точек соответствующих фаз.
до фигуративных точек соответствующих фаз.
Таким образом,

где 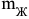 и
и 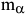 — масса соответственно жидкой и твердой фаз.
— масса соответственно жидкой и твердой фаз.
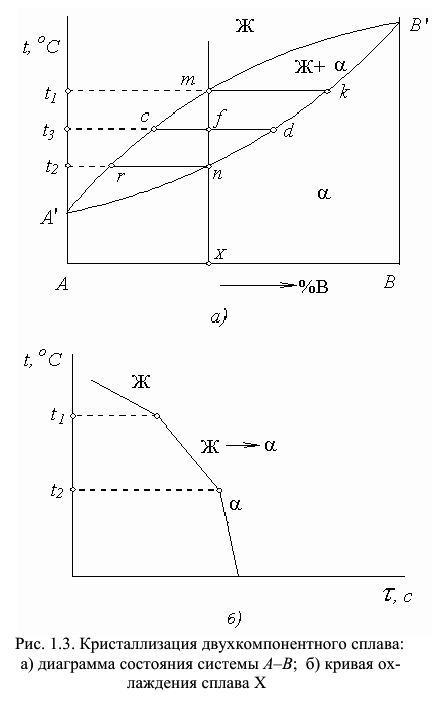
Из уравнения (1) следует, что
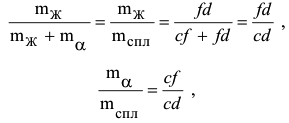
где 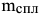 — масса сплава.
— масса сплава.
Как видно из этих уравнений, количество той или иной фазы в сплаве может быть выражено в долях или в процентах от массы всего сплава. При этом вся длина коноды 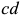 будет соответствовать массе всего сплава, то есть
будет соответствовать массе всего сплава, то есть 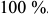 , а отрезки
, а отрезки 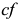 и
и 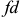 — массам
— массам  фазы и жидкой фазы.
фазы и жидкой фазы.
Процесс кристаллизации закончится при такой температуре, при которой отрезок коноды между точками, соответствующими кристаллам  фазы и сплаву, будет равен нулю. Такой температурой будет температура
фазы и сплаву, будет равен нулю. Такой температурой будет температура 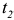 . Температура конца кристаллизации сплава
. Температура конца кристаллизации сплава 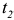 называется температурой солидуса сплава.
называется температурой солидуса сплава.
Точки 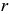 и
и 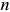 будут соответствовать составам последних капель жидкого раствора и кристаллов
будут соответствовать составам последних капель жидкого раствора и кристаллов  фазы, находящихся в равновесии друг с другом при температуре
фазы, находящихся в равновесии друг с другом при температуре 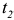 . Следовательно, процесс кристаллизации сплава
. Следовательно, процесс кристаллизации сплава 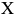 происходит в интервале температур от
происходит в интервале температур от 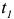 до
до 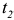 . При этом фигуративная точка жидкого раствора перемещается по кривой ликвидуса от точки
. При этом фигуративная точка жидкого раствора перемещается по кривой ликвидуса от точки 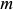 до точки
до точки 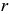 , а фигуративная точка
, а фигуративная точка  твердого раствора — по кривой солидуса от
твердого раствора — по кривой солидуса от 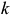 до точки
до точки 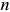 . Процесс кристаллизации может быть записан в виде реакции
. Процесс кристаллизации может быть записан в виде реакции
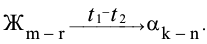
Эта реакция является реакцией кристаллизации сплава.
При охлаждении сплава 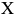 от
от 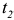 до комнатной температуры в нем никаких фазовых превращений не происходит.
до комнатной температуры в нем никаких фазовых превращений не происходит.
Кривая охлаждения образца сплава 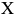 (рис. 1.3, б) в интервале температур от
(рис. 1.3, б) в интервале температур от 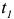 до
до 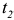 изменяет свой ход, что связано с выделением теплоты кристаллизации. Поэтому по термограммам охлаждения сплава можно определить температуры ликвидуса и солидуса.
изменяет свой ход, что связано с выделением теплоты кристаллизации. Поэтому по термограммам охлаждения сплава можно определить температуры ликвидуса и солидуса.
Подобные кривые получаются и при термическом анализе других сплавов заданной системы. Различие между кривыми охлаждения различных сплавов заключается лишь в температурах критических точек.
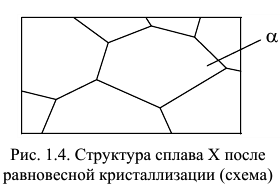
После равновесной кристаллизации структура сплава 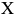 будет состоять из кристаллов
будет состоять из кристаллов  твердого раствора, состав которых соответствует составу сплава (рис. 1.4).
твердого раствора, состав которых соответствует составу сплава (рис. 1.4).
Диаграмма состояния двухкомпонентной системы с неограниченной растворимостью компонентов в жидком и ограниченной растворимостью компонентов в твердом состояниях (эвтектический тин)
Диаграмма состояния двухкомпонентной системы с неограниченной растворимостью в жидком состоянии и ограниченной растворимостью в твердом состоянии эвтектического типа приведена на рис. 1.5.
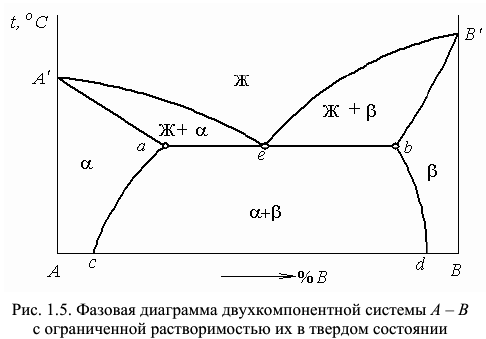
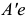 — линия ликвидуса
— линия ликвидуса  твердого раствора (твердого раствора компонента
твердого раствора (твердого раствора компонента 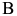 в компоненте
в компоненте 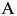 ),
), 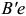 — линия ликвидуса
— линия ликвидуса  твердого раствора (твердого раствора компонента
твердого раствора (твердого раствора компонента 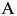 в компоненте
в компоненте 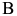 ).
). 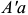 и
и 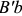 — это линии солидуса
— это линии солидуса  и
и  твердых растворов соответственно;
твердых растворов соответственно; 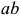 — эвтектическая линия;
— эвтектическая линия; 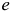 — эвтектическая точка;
— эвтектическая точка; 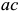 является линией ограниченной растворимости компонента
является линией ограниченной растворимости компонента 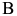 в компоненте
в компоненте 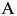 (линией сольвуса
(линией сольвуса  раствора), a
раствора), a 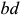 — линией ограниченной растворимости компонента
— линией ограниченной растворимости компонента 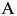 в компоненте
в компоненте 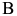 (линией сольвуса
(линией сольвуса  раствора). Эти линии разбивают всю диаграмму состояния системы
раствора). Эти линии разбивают всю диаграмму состояния системы 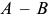 на шесть фазовых областей: три однофазные области
на шесть фазовых областей: три однофазные области 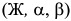 и три двухфазные области
и три двухфазные области 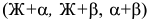 . Эвтектическая прямая является по существу седьмой, выродившейся в линию трехфазной областью
. Эвтектическая прямая является по существу седьмой, выродившейся в линию трехфазной областью 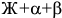 .
.
Все сплавы системы 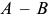 могут быть подразделены на доэвтектические, эвтектический и заэвтектические сплавы. Состав эвтектического сплава соответствует составу точки эвтектики
могут быть подразделены на доэвтектические, эвтектический и заэвтектические сплавы. Состав эвтектического сплава соответствует составу точки эвтектики 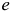 . Доэвтектические сплавы находятся в области, расположенной между точками
. Доэвтектические сплавы находятся в области, расположенной между точками 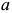 и
и 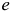 , а заэвтектические сплавы — в области между точками
, а заэвтектические сплавы — в области между точками 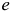 и
и 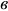 .
.
Проанализируем процессы, происходящие при охлаждении эвтектического сплава 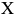 такой системы, в которой величина предельной растворимости как компонента
такой системы, в которой величина предельной растворимости как компонента 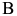 в
в  твердом растворе, так и компонента
твердом растворе, так и компонента 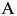 в
в  твердом растворе не изменяется при изменении температуры (рис. 1.6, а). Вертикаль, проходящая через точку
твердом растворе не изменяется при изменении температуры (рис. 1.6, а). Вертикаль, проходящая через точку 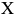 , пересекает линии диаграммы состояния в точке
, пересекает линии диаграммы состояния в точке 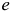 .
.
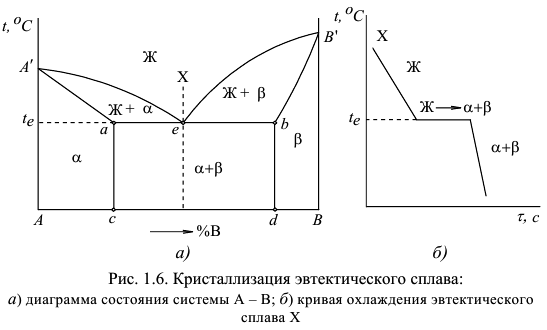
Следовательно, сплав 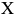 будет иметь одну критическую точку, которой соответствует эвтектическая температура
будет иметь одну критическую точку, которой соответствует эвтектическая температура 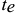 . При охлаждении сплава до
. При охлаждении сплава до 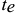 фазовый состав сплава изменяться не будет. Точка
фазовый состав сплава изменяться не будет. Точка 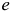 одновременно принадлежит как кривой ликвидуса
одновременно принадлежит как кривой ликвидуса  твердого раствора, так и кривой ликвидуса
твердого раствора, так и кривой ликвидуса  твердого раствора. Жидкий сплав, фигуративная точка которого соответствует точке
твердого раствора. Жидкий сплав, фигуративная точка которого соответствует точке 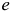 , будет одновременно насыщен как по отношению к кристаллам
, будет одновременно насыщен как по отношению к кристаллам  раствора, так и по отношению к кристаллам
раствора, так и по отношению к кристаллам  фазы.
фазы.
Поэтому из этого жидкого раствора в процессе равновесной кристаллизации одновременно будут выделяться как  , так и
, так и  кристаллы. Получающаяся в результате кристаллизации сплава
кристаллы. Получающаяся в результате кристаллизации сплава 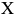 смесь
смесь  и
и  кристаллов носит название эвтектической смеси, или эвтектики. Процесс эвтектической кристаллизации может быть записан в виде реакции
кристаллов носит название эвтектической смеси, или эвтектики. Процесс эвтектической кристаллизации может быть записан в виде реакции
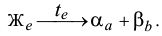
При равновесной эвтектической кристаллизации в образце сплава 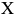 в равновесии находятся три фазы: жидкий раствор, кристаллы
в равновесии находятся три фазы: жидкий раствор, кристаллы  твердого раствора и кристаллы
твердого раствора и кристаллы  твердого раствора, составы которых соответствуют фигуративным точкам
твердого раствора, составы которых соответствуют фигуративным точкам 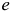 ,
, 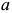 и
и 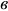 . После окончания эвтектической кристаллизации структура сплава будет представлять собой эвтектическую смесь кристаллов
. После окончания эвтектической кристаллизации структура сплава будет представлять собой эвтектическую смесь кристаллов  и
и  фаз. Соотношение количеств этих фаз в эвтектике
фаз. Соотношение количеств этих фаз в эвтектике
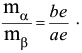
Предельные растворимости компонентов 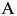 и
и 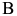 в фазах
в фазах  ,
,  при изменении температуры не изменяются, поэтому в процессе охлаждения сплава
при изменении температуры не изменяются, поэтому в процессе охлаждения сплава 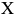 до комнатной температуры составы фаз в сплаве изменяться не будут.
до комнатной температуры составы фаз в сплаве изменяться не будут.
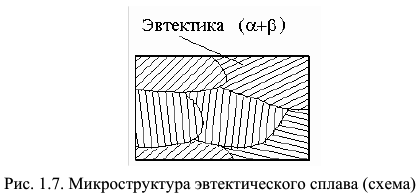
На рис. 1.6, б представлена кривая охлаждения сплава 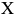 . На кривой охлаждения наблюдается горизонтальная площадка, соответствующая эвтектической кристаллизации. Микроструктура эвтектического сплава (рис. 1.7) имеет одну структурную составляющую эвтектику, но фазовых составляющих в структуре сплава
. На кривой охлаждения наблюдается горизонтальная площадка, соответствующая эвтектической кристаллизации. Микроструктура эвтектического сплава (рис. 1.7) имеет одну структурную составляющую эвтектику, но фазовых составляющих в структуре сплава 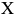 будет две. Это эвтектические кристаллы
будет две. Это эвтектические кристаллы  твердого раствора и эвтектические кристаллы
твердого раствора и эвтектические кристаллы  твердого раствора.
твердого раствора.
Рассмотрим процессы, происходящие при охлаждении образца до-эвтектического сплава 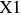 такой системы, в которой предельная растворимость компонента
такой системы, в которой предельная растворимость компонента 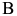 в
в  твердом растворе и предельная растворимость компонента
твердом растворе и предельная растворимость компонента 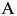 в
в  твердом растворе уменьшаются с понижением температуры (рис. 1.8). Вертикаль сплава
твердом растворе уменьшаются с понижением температуры (рис. 1.8). Вертикаль сплава 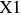 пересекает в точках 1 и 2 две линии диаграммы состояния. В интервале температур от
пересекает в точках 1 и 2 две линии диаграммы состояния. В интервале температур от 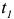 до
до 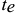 происходит кристаллизация твердого раствора:
происходит кристаллизация твердого раствора:
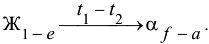
Кристаллы  фазы, выделяющиеся в эту стадию кристаллизации, называются первичными. В конечный момент кристаллизации фигуративная точка первичных кристаллов оказывается в точке
фазы, выделяющиеся в эту стадию кристаллизации, называются первичными. В конечный момент кристаллизации фигуративная точка первичных кристаллов оказывается в точке 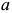 , а фигуративная точка жидкого раствора в точке
, а фигуративная точка жидкого раствора в точке 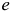 .
.
При температуре 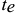 жидкий раствор кристаллизуется в виде эвтектики
жидкий раствор кристаллизуется в виде эвтектики
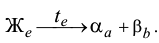
Таким образом, кристаллизация сплава 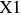 происходит в две стадии. Поэтому после эвтектической кристаллизации при температуре
происходит в две стадии. Поэтому после эвтектической кристаллизации при температуре 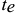 структура сплава будет состоять из двух структурных составляющих: первичных кристаллов
структура сплава будет состоять из двух структурных составляющих: первичных кристаллов  твердого раствора и эвтектики
твердого раствора и эвтектики 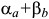 . Фазовых составляющих в структуре сплава
. Фазовых составляющих в структуре сплава 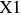 после кристаллизации эвтектики будет также две. Это кристаллы
после кристаллизации эвтектики будет также две. Это кристаллы  и
и  фаз.
фаз.
В результате того, что предельная растворимость компонента 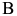 в
в  твердом растворе уменьшается с понижением температуры, в процессе охлаждения будет происходить распад
твердом растворе уменьшается с понижением температуры, в процессе охлаждения будет происходить распад  твердого раствора с выделением вторичных
твердого раствора с выделением вторичных  кристаллов. При этом фигуративная точка
кристаллов. При этом фигуративная точка  кристаллов будет перемещаться по кривой
кристаллов будет перемещаться по кривой 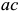 , а
, а  кристаллов — по кривой
кристаллов — по кривой 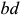 .
.
Этот процесс может быть записан в виде реакции
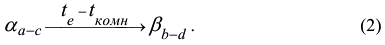
В результате этого процесса в кристаллах а фазы появятся мелкие вторичные кристаллы  фазы. С понижением температур предельная растворимость компонента
фазы. С понижением температур предельная растворимость компонента 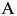 в
в  твердом растворе также уменьшается, поэтому аналогичный процесс будет происходить и в кристаллах
твердом растворе также уменьшается, поэтому аналогичный процесс будет происходить и в кристаллах  фазы:
фазы:
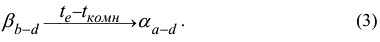
Реакции (2) и (3) могут быть объединены, так как они протекают одновременно:
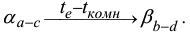
В результате этих процессов появляются вторичные кристаллы в первичных кристаллах  фазы и в кристаллах
фазы и в кристаллах  и
и  фаз эвтектики. Однако выделения вторичных кристаллов в эвтектике не заметно, так как сама эвтектика на шлифе выглядит как достаточно дисперсная смесь двух видов кристаллов.
фаз эвтектики. Однако выделения вторичных кристаллов в эвтектике не заметно, так как сама эвтектика на шлифе выглядит как достаточно дисперсная смесь двух видов кристаллов.
Поэтому вторичные кристаллы заметны только в первичных кристаллах а твердого раствора. Кривая охлаждения 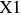 приведена на рис. 1.8, б. В структуре сплава
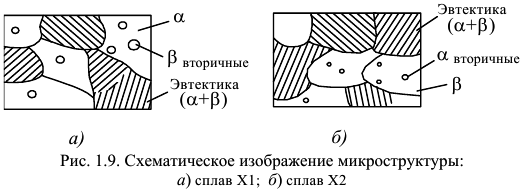
приведена на рис. 1.8, б. В структуре сплава 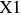 (рис. 1.9, а) наблюдаются следующие структурные составляющие: первичные кристаллы
(рис. 1.9, а) наблюдаются следующие структурные составляющие: первичные кристаллы  твердого раствора с выделением вторичных
твердого раствора с выделением вторичных  кристаллов и
кристаллов и 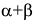 эвтектика. В структуре будут две фазовые составляющие: кристаллы
эвтектика. В структуре будут две фазовые составляющие: кристаллы 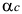 и
и 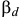 фаз, состав которых соответствует фигуративным точкам
фаз, состав которых соответствует фигуративным точкам 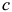 и
и 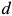 .
.
Заэвтектический сплав 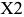 также имеет две критические точки (точки 3 и 4). При охлаждении сплава
также имеет две критические точки (точки 3 и 4). При охлаждении сплава 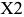 :
:
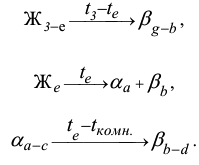
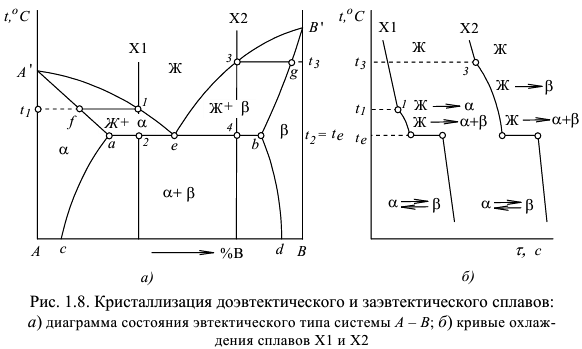
Согласно указанным выше формулам, процесс кристаллизации этого сплава происходит в две стадии и в структуре сплава будут следующие структурные составляющие: первичные кристаллы  фазы с включениями вторичных
фазы с включениями вторичных  кристаллов и эвтектика (рис. 1.9, б).
кристаллов и эвтектика (рис. 1.9, б).
Кривая охлаждения сплава  приведена на рис. 1.8, б. В других до- и заэвтектических сплавах при их охлаждении из жидкого состояния будут происходить процессы, аналогичные рассмотренным выше сплавам
приведена на рис. 1.8, б. В других до- и заэвтектических сплавах при их охлаждении из жидкого состояния будут происходить процессы, аналогичные рассмотренным выше сплавам  и
и 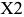 .
.
Рассмотрим процессы, происходящие при равновесом охлаждении образца сплава 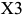 (рис. 1.10). Вертикаль сплава пересекает три линии диаграммы состояния в точках 5, 6 и 7. Поэтому при охлаждении сплава
(рис. 1.10). Вертикаль сплава пересекает три линии диаграммы состояния в точках 5, 6 и 7. Поэтому при охлаждении сплава 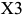 будут наблюдаться три критические точки (
будут наблюдаться три критические точки (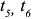 и
и 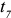 ):
):
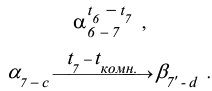
Стадии охлаждения до температуры 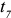 аналогичны стадиям охлаждения и кристаллизации сплавов типа твердых растворов. При температуре
аналогичны стадиям охлаждения и кристаллизации сплавов типа твердых растворов. При температуре 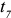 фигуративная точка сплава оказывается на кривой сольвуса
фигуративная точка сплава оказывается на кривой сольвуса  твердого раствора. Поэтому
твердого раствора. Поэтому  твердый раствор будет насыщенным относительно кристаллов
твердый раствор будет насыщенным относительно кристаллов  фазы и при дальнейшем охлаждении из кристаллов
фазы и при дальнейшем охлаждении из кристаллов  фазы будут выделяться вторичные кристаллы
фазы будут выделяться вторичные кристаллы  фазы.
фазы.
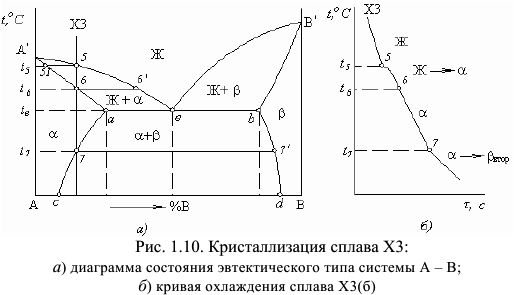
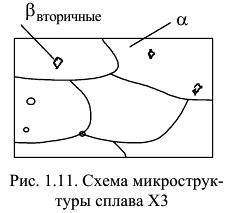
Эти кристаллы  фазы образуются как по границам, так и внутри
фазы образуются как по границам, так и внутри  кристаллов. На рис. 1.11 приведена структура образца сплава
кристаллов. На рис. 1.11 приведена структура образца сплава  , а на рис. 1.10, б — кривая его охлаждения. Структура сплава
, а на рис. 1.10, б — кривая его охлаждения. Структура сплава  состоит из кристаллов
состоит из кристаллов  раствора, содержащих включения вторичных кристаллов
раствора, содержащих включения вторичных кристаллов  твердого раствора. В структуре сплава
твердого раствора. В структуре сплава  будут фазовые составляющие: кристаллы
будут фазовые составляющие: кристаллы  и
и  фаз.
фаз.
Возможно эта страница вам будет полезна:
| Примеры решения задач по материаловедению |
Железоуглеродистые сплавы
Основные теоретические сведения
Несмотря на то, что железоуглеродистые сплавы — сталь и чугун, как правило, содержат некоторые примеси (кремний, марганец, серу, фосфор, кислород, азот и др.), т. е. практически являются многокомпонентными, однако основными составляющими, определяющими структуру и свойства, являются железо и углерод и условно их можно рассматривать как двойные. Сплавы железа распространены в промышленности наиболее широко. Поэтому среди диаграмм состояния металлических сплавов самое большое значение имеет диаграмма состояния системы железо — цементит 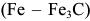 , которая показывает фазовый состав и структуру железоуглеродистых сплавов.
, которая показывает фазовый состав и структуру железоуглеродистых сплавов.
Компоненты в сплавах железа с углеродом
Железо. Железо находится в периодической системе Д. И. Менделеева в IV периоде, в восьмой группе (порядковый номер 26).
Температура плавления чистого железа равна 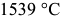 , кипения —
, кипения — 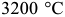 . Плотность —
. Плотность — 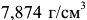 , атомный вес —
, атомный вес — 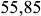 . Железо имеет две полиморфные модификации
. Железо имеет две полиморфные модификации  и
и 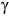 . Кристаллическая решетка
. Кристаллическая решетка 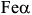 — ОЦК (объемноцентрированная кубическая);
— ОЦК (объемноцентрированная кубическая); 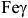 — ГЦК (гранецентрированная кубическая). Полиморфное превращение сопровождается изменением объема, поскольку переход
— ГЦК (гранецентрированная кубическая). Полиморфное превращение сопровождается изменением объема, поскольку переход 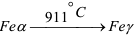 связан с уменьшением компактности решетки. Различие объемов составляет около
связан с уменьшением компактности решетки. Различие объемов составляет около 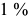 .
.
Углерод является вторым основным компонентом железоуглеродистых сплавов. Углерод неметаллический элемент II периода, четвертой группы. Он занимает шестое место в периодической системе Д. И. Менделеева. Обладает относительно малой плотностью 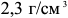 , температура плавления около
, температура плавления около 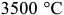 . Углерод полиморфен. В обычных условиях углерод находится в виде графита с гексагональной слоистой решеткой. Метастабильная модификация углерода (алмаз) имеет кубическую решетку.
. Углерод полиморфен. В обычных условиях углерод находится в виде графита с гексагональной слоистой решеткой. Метастабильная модификация углерода (алмаз) имеет кубическую решетку.
Диаграмма состояния железо-углерод должна, очевидно, охватывать все сплавы от 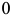 до
до 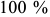 углерода. Однако, как правило, приводится небольшой участок системы от железа до ближайшего химического соединения
углерода. Однако, как правило, приводится небольшой участок системы от железа до ближайшего химического соединения 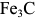 . Это обусловлено тем, что практически применяются сплавы железа с углеродом с содержанием углерода не более
. Это обусловлено тем, что практически применяются сплавы железа с углеродом с содержанием углерода не более 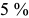 .
.
Фазы в сплавах железа с углеродом
В сплавах системы 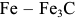 встречаются следующие фазы: жидкий раствор, твердые растворы на основе различных кристаллических модификаций железа, химическое соединение карбид железа
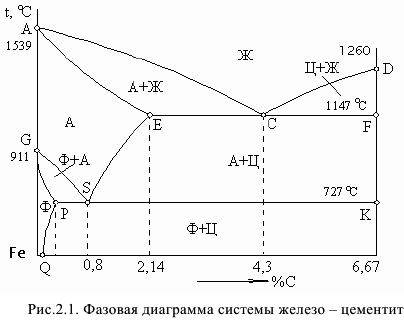
встречаются следующие фазы: жидкий раствор, твердые растворы на основе различных кристаллических модификаций железа, химическое соединение карбид железа 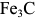 (цементит). На рис. 2.1 представлена диаграмма состояния железо-цементит в фазовом виде (упрощенный вид).
(цементит). На рис. 2.1 представлена диаграмма состояния железо-цементит в фазовом виде (упрощенный вид).
Жидкая фаза представляет собой неограниченный раствор железа и углерода, распространяющийся выше линии ликвидус 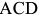 — от
— от 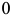 до
до 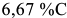 .
.
Твердые растворы. В данной системе имеются твердые растворы железа с углеродом на основе двух кристаллических модификаций железа. Они являются твердыми растворами внедрения, т. е. атомы железа занимают узлы пространственной решетки, а атомы углерода размещаются в междоузлиях.
Твердый раствор углерода в  -железе называется ферритом (обозначают Ф). В феррите сохраняется кристаллическая решетка
-железе называется ферритом (обозначают Ф). В феррите сохраняется кристаллическая решетка  -железа — объемно-центрированный куб. Феррит занимает на диаграмме узкую область, примыкающую к железу
-железа — объемно-центрированный куб. Феррит занимает на диаграмме узкую область, примыкающую к железу 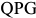 . Максимальная растворимость углерода в нем не более
. Максимальная растворимость углерода в нем не более 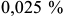 при температуре
при температуре 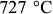 Твердость феррита около
Твердость феррита около 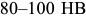 , предел прочности
, предел прочности 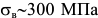 ; относительное удлинение
; относительное удлинение 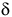 до
до 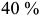 , а поперечное сужение
, а поперечное сужение 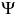 до
до 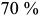 . До температуры
. До температуры 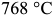 феррит ферромагнитен, выше — парамагнитен.
феррит ферромагнитен, выше — парамагнитен.
Значительно большую область на диаграмме железо-углерод занимает твердый раствор углерода в 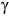 -железе с гранецентрирован-ной кубической решеткой, который называется аустенитом (обозначается
-железе с гранецентрирован-ной кубической решеткой, который называется аустенитом (обозначается 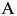 ). В аустените предел растворимости углерода достигает
). В аустените предел растворимости углерода достигает 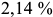 при температуре
при температуре 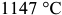 . Твердость его равна
. Твердость его равна 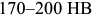 . Аустенит обладает малой склонностью к хрупкому разрушению.
. Аустенит обладает малой склонностью к хрупкому разрушению.
Цементит (обозначают Ц) — карбид железа 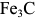 (химическое соединение железа с углеродом) содержит
(химическое соединение железа с углеродом) содержит 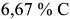 , обладает сложной ромбической решеткой. В решетке цементита реализуются связи как ковалентные, так и металлического типа. Цементит имеет высокую твердость
, обладает сложной ромбической решеткой. В решетке цементита реализуются связи как ковалентные, так и металлического типа. Цементит имеет высокую твердость 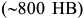 . Температура плавления цементита при нагреве лазерным лучом равна
. Температура плавления цементита при нагреве лазерным лучом равна 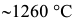 .
.
Линии и точки диаграммы 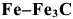
Все линии делят поле диаграммы на области равновесного нахождения фаз: линия ликвидус — начало затвердения при охлаждении или конец плавления при нагревании; линия солидус — конец затвердевания при охлаждении и начало плавления при нагревании; линии превращения в твердом состоянии.
В табл. 2.1 приведены основные характеристики линий диаграммы.
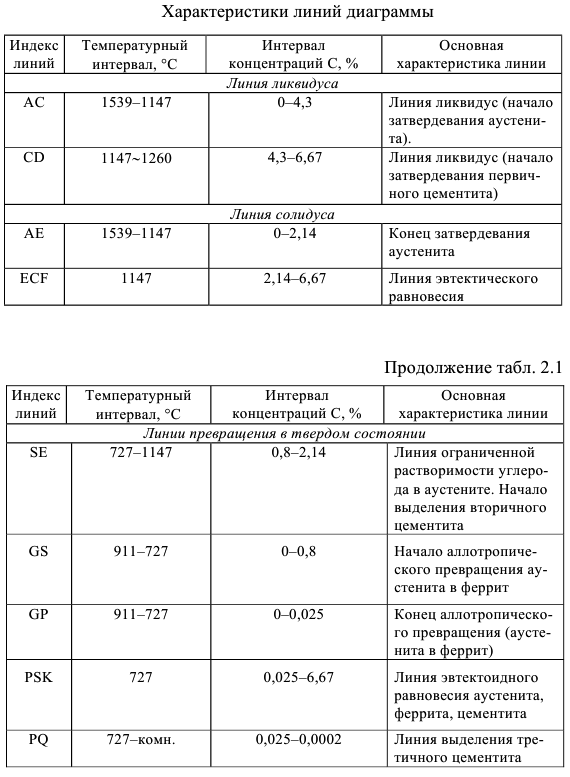
Концентрация углерода в характерных точках диаграммы приводится в табл. 2.2.
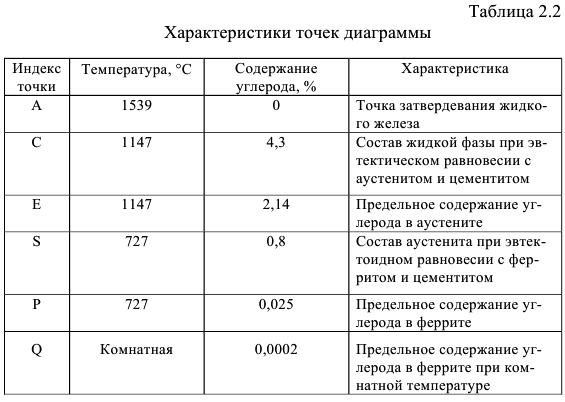
Горизонтальные линии диаграммы 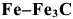
В системе железо — цементит происходят изотермические превращения: эвтектическое и эвтектоидное.
В табл. 2.3 приведены линии изотермических превращений.
Принято температуры равновесных превращений, совершающихся в железе и в сталях в твердом состоянии, обозначать буквой 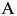 с соответствующим индексом.
с соответствующим индексом.

Эвтектоидную температуру (линия 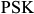 ) обозначают
) обозначают 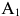 , температуру магнитного превращения (линия
, температуру магнитного превращения (линия 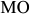 ) —
) — 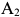 , температуру линии
, температуру линии 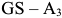 , температуру линии
, температуру линии 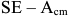 .
.
Вследствие гистерезиса, температуры превращений при нагреве всегда выше соответствующих температур при охлаждении, поэтому введена дополнительная индексация: при нагреве — индекс 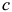 , при охлаждении — индекс
, при охлаждении — индекс 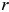 .
.
Кристаллизации и формирование структуры сплавов
Сталями называются железоуглеродистые сплавы с содержанием углерода до 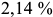 . Сплавы с большим содержанием углерода (
. Сплавы с большим содержанием углерода (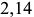 до
до 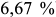 ) называются чугунами. Границей между сталями и чугунами принято считать проекцию точки
) называются чугунами. Границей между сталями и чугунами принято считать проекцию точки 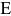 , т. е. точки максимального насыщения аустенита углеродом, от которой начинается линия эвтектического равновесия. В результате первичной кристаллизации стали образуется аустенит (линия
, т. е. точки максимального насыщения аустенита углеродом, от которой начинается линия эвтектического равновесия. В результате первичной кристаллизации стали образуется аустенит (линия 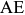 ).
).
В отличии от сталей структура чугуна характеризуется наличием эвтектики, которая состоит из аустенита и цементита.
Первичная кристаллизация стали. На рис. 2.2 показан верхний участок упрощенной диаграммы 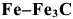 .
.
В сталях из жидкой фазы кристаллизуется аустенит. Состав жидкой фазы меняется по проекции линии 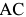 на ось концентраций, твердой фазы по проекции линии
на ось концентраций, твердой фазы по проекции линии 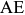 .
.
Превращения в твердом состоянии. Окончательное формирование структуры стали происходит в результате превращений аустенита при дальнейшем охлаждении. Основой этого превращения является полиморфизм, связанный с перегруппировкой атомов из ГЦК решетки аустенита в ОЦК решетку феррита, а также изменение растворимости углерода по линии 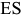 в аустените и
в аустените и 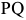 в феррите.
в феррите.
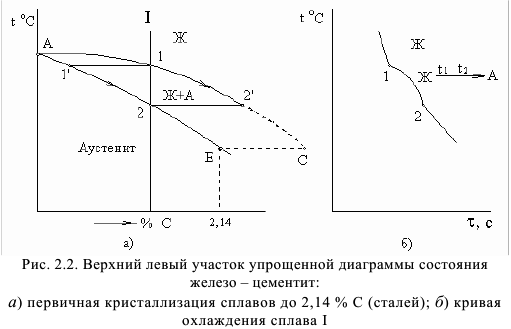
В сплавах с содержанием от 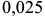 до
до 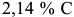 вторичные превращения начинаются при температурах, соответствующих линиям
вторичные превращения начинаются при температурах, соответствующих линиям 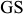 и
и 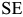 и заканчиваются при температуре ниже
и заканчиваются при температуре ниже 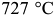 и линии
и линии 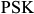 , в результате эвтектоидной реакции.
, в результате эвтектоидной реакции.
Возможно эта страница вам будет полезна:
| Методические указания по материаловедению |
Сплавы с содержанием углерода менее 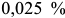 не испытывают эвтектоидного превращения. Распад аустенита при эвтектоидном превращении проходит с образованием феррита и цементита при переохлаждении ниже
не испытывают эвтектоидного превращения. Распад аустенита при эвтектоидном превращении проходит с образованием феррита и цементита при переохлаждении ниже 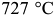 :
:
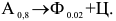
Эвтектоидная смесь феррита и цементита называется перлитом (обозначается П).
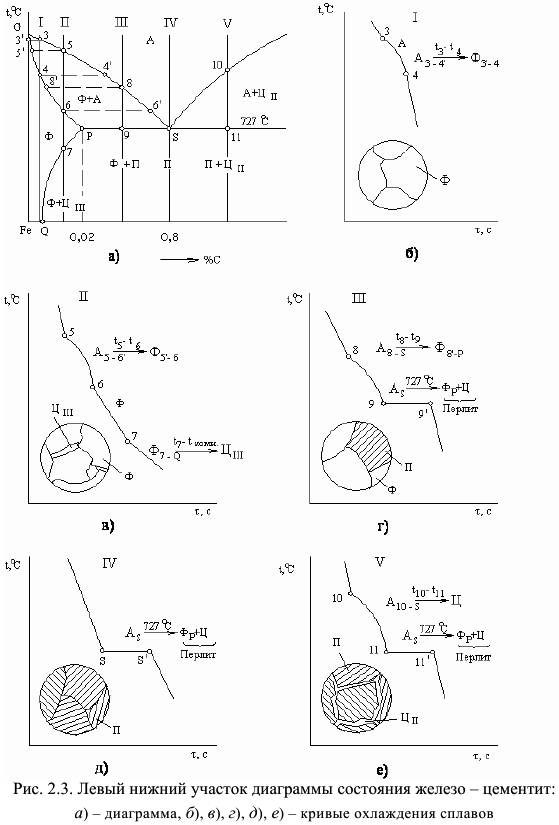
Рассмотрим структурообразование нескольких групп сплавов. На рис. 2.3 приведена левая нижняя часть диаграммы состояния железо-цементит с кривыми охлаждения типичных сплавов и микроструктурой.
Техническое железо (сплавы, содержание углерода в которых не превышает 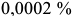 — на примере сплава I). До температуры несколько ниже
— на примере сплава I). До температуры несколько ниже 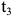 (линия
(линия 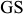 ) аустенит охлаждается без изменения состава. В интервале
) аустенит охлаждается без изменения состава. В интервале 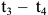 происходит полиморфное
происходит полиморфное 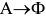 превращение. На стыках и границах зерен аустенита возникают зародыши феррита, которые растут и развиваются за счет атомов аустенитной фазы. Ниже температуры
превращение. На стыках и границах зерен аустенита возникают зародыши феррита, которые растут и развиваются за счет атомов аустенитной фазы. Ниже температуры 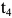 сплав состоит из однородного a-твердого раствора -феррита. При дальнейшем охлаждении никаких превращений не происходит (рис. 2.3, б).
сплав состоит из однородного a-твердого раствора -феррита. При дальнейшем охлаждении никаких превращений не происходит (рис. 2.3, б).
Техническое железо (сплавы с содержанием углерода от 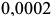 до
до 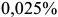 (сплав II рис. 2.3, в). Так же как и в предыдущем сплаве в интервале температур
(сплав II рис. 2.3, в). Так же как и в предыдущем сплаве в интервале температур  происходит полиморфное
происходит полиморфное 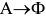 превращение. Ниже
превращение. Ниже 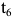 в сплаве имеется ферритная фаза. Однако ниже температуры
в сплаве имеется ферритная фаза. Однако ниже температуры 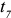 изменение состава феррита, согласно предельной растворимости углерода в феррите по линии
изменение состава феррита, согласно предельной растворимости углерода в феррите по линии 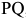 , приводит к образованию более высокоуглеродистой фазы, цементита. Этот цементит называется третичным. Как правило, третичный цементит располагается по границам ферритных зерен (рис. 2.3, в). Максимальное количество третичного цементита составляет около
, приводит к образованию более высокоуглеродистой фазы, цементита. Этот цементит называется третичным. Как правило, третичный цементит располагается по границам ферритных зерен (рис. 2.3, в). Максимальное количество третичного цементита составляет около 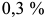 .
.
Сталь эвтектоидного состава — содержание углерода 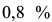 (рис. 2.3, д, сплав IV).
(рис. 2.3, д, сплав IV).
В этом случае при охлаждении аустенита имеется только одна критическая точка 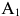 , отвечающая температуре
, отвечающая температуре 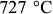 . При этой температуре аустенит находится в равновесии с ферритом и цементитом:
. При этой температуре аустенит находится в равновесии с ферритом и цементитом:
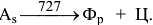
Эвтектоидный распад аустенита состава точки 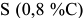 на феррит состава точки
на феррит состава точки 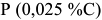 и цементит происходит при некотором переохлаждении, т. е. ниже
и цементит происходит при некотором переохлаждении, т. е. ниже 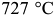 . Эвтектоидная смесь феррита с цементитом называется перлитом. Соотношение феррита и цементита в перлите составляет примерно
. Эвтектоидная смесь феррита с цементитом называется перлитом. Соотношение феррита и цементита в перлите составляет примерно 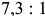 .
.
Доэвтектоидные стали. Сплавы с содержанием углерода от 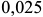 до
до 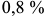 называются доэвтектоидными сталями. Рассмотрим фазовые и структурные изменения доэвтектоидной стали на примере сплава Ш (рис. 2.3, г). В интервале температур
называются доэвтектоидными сталями. Рассмотрим фазовые и структурные изменения доэвтектоидной стали на примере сплава Ш (рис. 2.3, г). В интервале температур 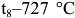 идет полиморфное превращение
идет полиморфное превращение 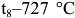 . Состав аустенита меняется по линии
. Состав аустенита меняется по линии 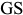 , а феррита — по линии
, а феррита — по линии 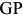 . При
. При 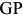 концентрация углерода в аустените равна
концентрация углерода в аустените равна 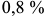 (точка
(точка 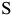 ) и в феррите —
) и в феррите — 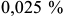 (точка
(точка 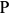 ).
).
Ниже этой температуры происходит эвтектоидное превращение. В равновесии находятся три фазы: феррит состава точки 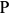 , аустенит состава точки
, аустенит состава точки 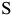 , цементит. На кривых охлаждения или нагрева наблюдается температурная остановка. Таким образом, структура доэвтектоидной стали характеризуется избыточными кристаллами феррита и эвтектоидной смесью феррита с цементитом, называемой перлитом. Количественные соотношения феррита и перлита зависят от состава сплава. Чем больше углерода в доэвтектоидной стали, тем больше в структуре ее перлита и, наоборот, чем меньше углерода, тем больше феррита и меньше перлита. При дальнейшем охлаждении в результате изменения растворимости углерода в феррите (соответственно линии
, цементит. На кривых охлаждения или нагрева наблюдается температурная остановка. Таким образом, структура доэвтектоидной стали характеризуется избыточными кристаллами феррита и эвтектоидной смесью феррита с цементитом, называемой перлитом. Количественные соотношения феррита и перлита зависят от состава сплава. Чем больше углерода в доэвтектоидной стали, тем больше в структуре ее перлита и, наоборот, чем меньше углерода, тем больше феррита и меньше перлита. При дальнейшем охлаждении в результате изменения растворимости углерода в феррите (соответственно линии 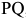 ) выделяется третичный цементит. Однако в структуре обнаружить его при наличии перлита невозможно.
) выделяется третичный цементит. Однако в структуре обнаружить его при наличии перлита невозможно.
Заэвтектоидные стали
Сплавы с содержанием углерода от 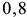 до
до 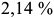 называются заэвтектоидными. Процессы структурообра-зования рассмотрим на примере сплава
называются заэвтектоидными. Процессы структурообра-зования рассмотрим на примере сплава 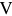 (рис. 2.3, е). До температуры
(рис. 2.3, е). До температуры 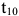 (линия
(линия 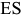 ) аустенит охлаждается без изменения состава. Несколько ниже этой температуры аустенит достигает предельного насыщения углеродом согласно линии растворимости углерода в аустените
) аустенит охлаждается без изменения состава. Несколько ниже этой температуры аустенит достигает предельного насыщения углеродом согласно линии растворимости углерода в аустените 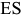 . В интервале температур
. В интервале температур 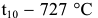 из пересыщенного аустенита выделяется высокоуглеродистая фаза — цементит, который называется вторичным. Состав аустенита меняется по линии
из пересыщенного аустенита выделяется высокоуглеродистая фаза — цементит, который называется вторичным. Состав аустенита меняется по линии 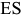 и при температуре
и при температуре 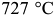 достигает точки
достигает точки 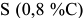 .
.
Ниже 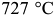 происходит эвтектоидное превращение: аустенит состава точки
происходит эвтектоидное превращение: аустенит состава точки 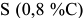 распадается на смесь феррита состава точки
распадается на смесь феррита состава точки 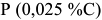 и цементита. Таким образом, структура заэвтектоидной стали характеризуется зернами перлита и вторичного цементита. При медленном охлаждении цементит, как правило, располагается в виде тонкой оболочки вокруг перлитных зерен.
и цементита. Таким образом, структура заэвтектоидной стали характеризуется зернами перлита и вторичного цементита. При медленном охлаждении цементит, как правило, располагается в виде тонкой оболочки вокруг перлитных зерен.
Чугуны
Все превращения в белых чугунах, начиная от затвердевания и до комнатных температур, полностью проходят по метаста-бильной диаграмме 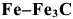 . Наличие цементита придает излому светлый блестящий цвет, что привело к термину «белый чугун». Независимо от состава сплава обязательной структурной составляющей белого чугуна является цементитная эвтектика {ледебурит). На рис. 2.4 изображена структурная диаграмма равновесия железо — цементит и кривые охлаждения типичных сплавов.
. Наличие цементита придает излому светлый блестящий цвет, что привело к термину «белый чугун». Независимо от состава сплава обязательной структурной составляющей белого чугуна является цементитная эвтектика {ледебурит). На рис. 2.4 изображена структурная диаграмма равновесия железо — цементит и кривые охлаждения типичных сплавов.
Эвтектический белый чугун
Рассмотрим процессы затвердевания, формирования первичной структуры и дальнейших структурных превращений в твердом состоянии сплава эвтектического состава с 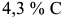 (сплав I, рис. 2.4).
(сплав I, рис. 2.4).
Затвердевание происходит в один этап при температуре ниже 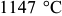 . Жидкая фаза с
. Жидкая фаза с 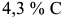 образует эвтектическую структуру: смесь аустенита с
образует эвтектическую структуру: смесь аустенита с 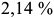 С и цементита. Эта эвтектика называется ледебуритом. При эвтектической реакции содержание углерода в аустените максимально (
С и цементита. Эта эвтектика называется ледебуритом. При эвтектической реакции содержание углерода в аустените максимально (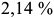 ).
).
Превращения в твердом состоянии
Окончательное формирование структуры стали происходит в результате превращений аустенита при дальнейшем охлаждении.
Дальнейшее охлаждение от температуры 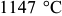 до
до 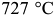 приводит к непрерывному уменьшению в нем углерода согласно линии ограниченной растворимости
приводит к непрерывному уменьшению в нем углерода согласно линии ограниченной растворимости 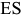 . Углерод выделяется из аустенита в виде цементита, который называется вторичным цементитом (Цп). Однако он, как правило, не обнаруживается, т. к. присоединяется к эвтектическому цементиту. Ниже температуры
. Углерод выделяется из аустенита в виде цементита, который называется вторичным цементитом (Цп). Однако он, как правило, не обнаруживается, т. к. присоединяется к эвтектическому цементиту. Ниже температуры 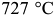 аустенит эвтектики состава (
аустенит эвтектики состава (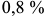 ) претерпевает эвтектоидное превращение
) претерпевает эвтектоидное превращение
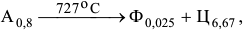
т. е. образуется перлит.
Таким образом, ниже 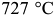 ледебурит представляет собой смесь перлита и цементита. Такой ледебурит называется превращенным. При охлаждении до комнатной температуры в результате изменения растворимости углерода в феррите (линия
ледебурит представляет собой смесь перлита и цементита. Такой ледебурит называется превращенным. При охлаждении до комнатной температуры в результате изменения растворимости углерода в феррите (линия 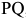 ) выделяется третичный цементит. Однако в структуре он не обнаруживается. На рис. 2.4, б показана структура белого чугуна эвтектического состава. Она представляет собой одну эвтектику — ледебурит. Темные участки (зернышки и пластинки) отвечают перлитным включениям, равномерно распределенным на светлом фоне цементита.
) выделяется третичный цементит. Однако в структуре он не обнаруживается. На рис. 2.4, б показана структура белого чугуна эвтектического состава. Она представляет собой одну эвтектику — ледебурит. Темные участки (зернышки и пластинки) отвечают перлитным включениям, равномерно распределенным на светлом фоне цементита.
Доэвтектические белые чугуны
Железоуглеродистые сплавы состава 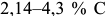 называются доэвтектическими белыми чугунами. Рассмотрим процесс кристаллизации и вторичных превращений на примере сплава П (рис.2.4, в). От температуры несколько ниже линии ликвидус
называются доэвтектическими белыми чугунами. Рассмотрим процесс кристаллизации и вторичных превращений на примере сплава П (рис.2.4, в). От температуры несколько ниже линии ликвидус 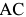 до
до 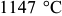 из жидкости выделяются кристаллы аустенита.
из жидкости выделяются кристаллы аустенита.
Аустенит кристаллизуется в форме дендритов, которые, как правило, обладают химической неоднородностью, называемой дендритной ликвацией. Состав жидкой фазы меняется по линии ликвидус, стремясь к эвтектическому, а твердой — по линии солидус, стремясь к составу точки 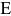 . При температуре
. При температуре 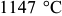 концентрация жидкой фазы достигает точки
концентрация жидкой фазы достигает точки 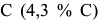 , а аустенита — точки
, а аустенита — точки 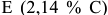 . Из жидкости эвтектического состава образуется смесь аустенита и цементита — ледебурит
. Из жидкости эвтектического состава образуется смесь аустенита и цементита — ледебурит  .
.
Таким образом, ниже эвтектической линии 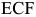 структура характеризуется избыточными кристаллами аустенита и эвтектикой (ледебуритом). При охлаждении от
структура характеризуется избыточными кристаллами аустенита и эвтектикой (ледебуритом). При охлаждении от  до
до 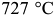 состав аустенита непрерывно меняется по линии
состав аустенита непрерывно меняется по линии 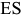 , при этом выделяется цементит вторичный (Цп).
, при этом выделяется цементит вторичный (Цп).
Вторичный цементит выделяется как из избыточного аустенита, так и из аустенита эвтектики. Однако, если вторичный цементит, выделяющийся из аустенита эвтектики, присоединяется к эвтектическому цементиту, то из избыточного аустенита он выделяется в виде оболочек вокруг дендритов аустенита и представляет собой самостоятельную структурную составляющую.
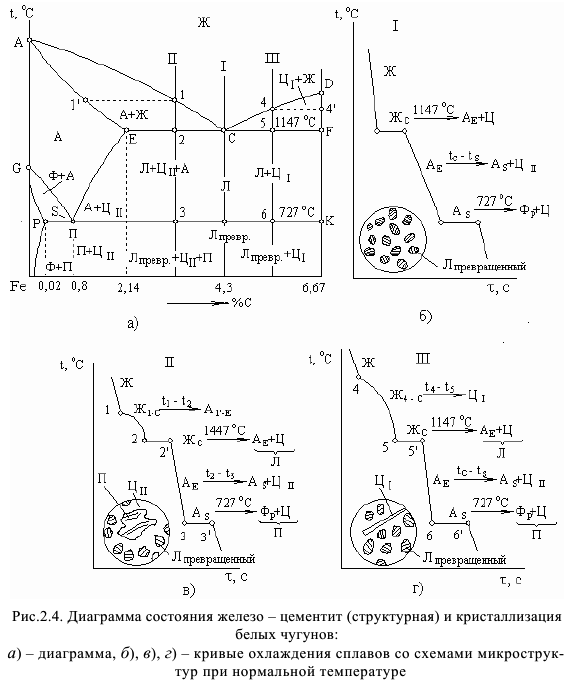
Однако, если вторичный цементит, выделяющийся из аустенита эвтектики, присоединяется к эвтектическому цементиту, то из избыточного аустенита он выделяется в виде оболочек вокруг дендритов аустенита и представляет собой самостоятельную структурную составляющую.
Ниже 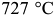 весь аустенит — и избыточный, и тот, который входит в состав эвтектики, претерпевает эвтектоидное превращение, при котором образуется перлит. Таким образом, ниже
весь аустенит — и избыточный, и тот, который входит в состав эвтектики, претерпевает эвтектоидное превращение, при котором образуется перлит. Таким образом, ниже 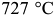 структура до-эвтектического белого чугуна характеризуется следующими структурными составляющими: избыточным перлитом (бывшим аустенитом), ледебуритом превращенным, состоящим из перлита и цементита, и цементитом вторичным. Структура реального доэвтектического белого чугуна изображена на рис. 2.4, в. Чем ближе состав сплава к эвтектическому, тем больше в нем эвтектики — ледебурита.
структура до-эвтектического белого чугуна характеризуется следующими структурными составляющими: избыточным перлитом (бывшим аустенитом), ледебуритом превращенным, состоящим из перлита и цементита, и цементитом вторичным. Структура реального доэвтектического белого чугуна изображена на рис. 2.4, в. Чем ближе состав сплава к эвтектическому, тем больше в нем эвтектики — ледебурита.
Заэвтектический белый чугун
Железоуглеродистые сплавы с содержанием углерода от 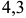 до
до 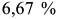 (сплав
(сплав 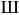 ) называются заэв-тектическими белыми чугунами. Кристаллизация начинается при температуре
) называются заэв-тектическими белыми чугунами. Кристаллизация начинается при температуре 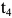 несколько ниже линии
несколько ниже линии 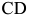 выпадением цементита, который называется цементитом первичным (
выпадением цементита, который называется цементитом первичным (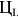 ). Состав жидкой фазы меняется по линии
). Состав жидкой фазы меняется по линии 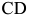 , твердая — остается без изменения. При температуре
, твердая — остается без изменения. При температуре 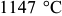 заканчивается кристаллизация избыточных кристаллов
заканчивается кристаллизация избыточных кристаллов 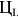 . Жидкость состава точки
. Жидкость состава точки 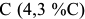 , согласно эвтектической реакции, образует ледебурит. При дальнейшем охлаждении изменение состава аустенита по линии
, согласно эвтектической реакции, образует ледебурит. При дальнейшем охлаждении изменение состава аустенита по линии 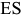 приводит к выделению цементита вторичного (
приводит к выделению цементита вторичного (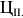 ), который присоединяется к эвтектическому.
), который присоединяется к эвтектическому.
Температура 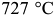 является температурой эвтектоидного равновесия аустенита, феррита и цементита. Ниже этой температуры аустенит превращается в перлит.
является температурой эвтектоидного равновесия аустенита, феррита и цементита. Ниже этой температуры аустенит превращается в перлит.
Таким образом, ниже
структура заэвтектического белого чугуна характеризуется избыточными кристаллами цементита первичного (белые пластины) и превращенным ледебуритом, состоящим из темных полосок или зернышек перлита и светлой основы — цементита. На рис. 2.4, г изображена кривая охлаждения и структура белого заэвтектического чугуна.
Возможно эта страница вам будет полезна:
| Учебник по материаловедению |
Термическая обработка углеродистых сталей
Основные теоретические сведения
Термическую обработку стали можно определить как процесс теплового воздействия на сталь, направленный на изменение ее структуры и свойств.
Режимы термической обработки сталей связаны с критическими точками, точками фазовых превращений в сталях. Температуру, соответствующую линии 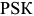 на диаграмме состояния
на диаграмме состояния 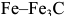 , обозначают точкой
, обозначают точкой 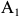 . Температуры, соответствующие линии
. Температуры, соответствующие линии 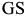 , обозначают точкой
, обозначают точкой 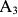 , а линии
, а линии 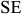 — точкой
— точкой 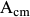 .
.
Из-за теплового гистерезиса превращения при нагреве стали начинаются при температурах выше точек 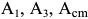 , а при охлаждении -ниже этих точек. Для обозначения температур превращения при нагревании у буквы
, а при охлаждении -ниже этих точек. Для обозначения температур превращения при нагревании у буквы 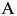 внизу ставят индекс
внизу ставят индекс 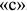 , а при охлаждении —
, а при охлаждении — 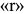 (например,
(например, 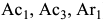 ).
).
Структура термически обработанной стали данного состава, а следовательно и ее свойства, определяется тремя основными факторами — температурой нагрева, временем выдержки при этой температуре и скоростью охлаждения. Любой процесс термической обработки можно изобразить в виде графика (рис. 3.1), на котором по оси ординат указывают температуру, а по оси абсцисс — время.
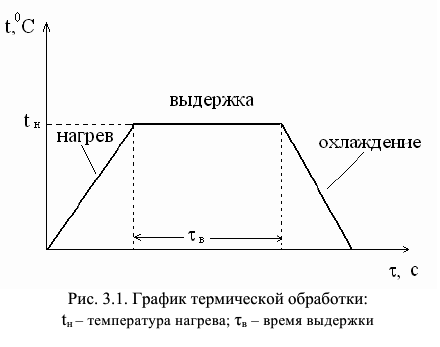
Термическую обработку можно разделить на несколько основных видов, исходя из сущности происходящих в металле процессов. Такими основными видами являются: отжигу нормализация, закалка и отпуск.
Возможно эта страница вам будет полезна:
| Рефераты по материаловедению |
Отжиг
Отжигом называют процесс термической обработки, при котором сталь сначала нагревают до определенной температуры, выдерживают при этой температуре, а затем медленно охлаждают вместе с печью. В результате отжига в стали образуются равновесные структурные составляющие (см. диаграмму состояния 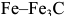 , рис. 2.3, а).
, рис. 2.3, а).
Различают отжиг первого и второго рода. Отжиг первого рода имеет целью снятие напряжений, осуществление рекристаллизации и гомогенизации. Применительно к углеродистым сталям отжиг для снятия напряжений производится при 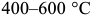 . Рекристаллизаци-онный отжиг осуществляется при
. Рекристаллизаци-онный отжиг осуществляется при 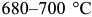 , т. е. ниже превращения
, т. е. ниже превращения 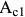 . Гомогенизационный отжиг для устранения дендритной ликвации в литой стали производится в аустенитной области при температуре
. Гомогенизационный отжиг для устранения дендритной ликвации в литой стали производится в аустенитной области при температуре 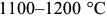 в течение
в течение 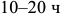 . За это время в металле может заметно вырасти аустенитное зерно, что приводит к пониженным механическим свойствам. Поэтому после гомогенизационного отжига сталь всегда подвергают отжигу второго рода — фазовой перекристаллизации с целью измельчения аустенитного зерна.
. За это время в металле может заметно вырасти аустенитное зерно, что приводит к пониженным механическим свойствам. Поэтому после гомогенизационного отжига сталь всегда подвергают отжигу второго рода — фазовой перекристаллизации с целью измельчения аустенитного зерна.
Для отжига с полной фазовой перекристаллизацией стали (отжига второго рода) необходимо выполнить два условия:
- Во-первых, необходимо нагреть сталь до такой температуры, при которой она находится в аустенитном состоянии, и выдержать при этой температуре до полной аустенизации.
- Во-вторых, необходимо охладить сталь с относительно небольшой скоростью, чтобы произошло фазовое превращение с образованием из аустенита феррито-цементитной смеси.
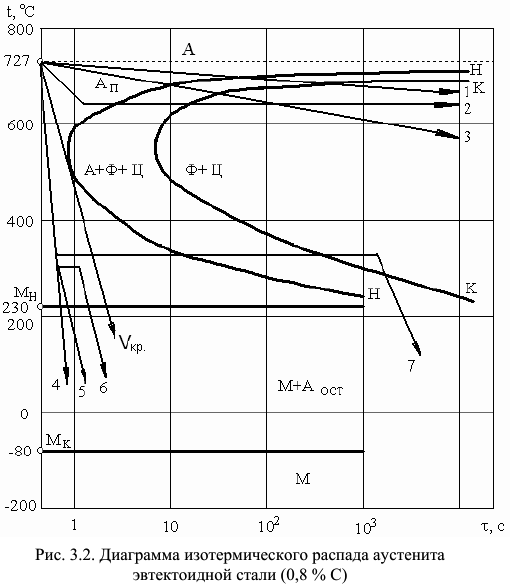
Увеличивая скорость охлаждения стали, можно значительно повысить степень переохлаждения аустенита, от которой зависят механизм и кинетика превращения, и, соответственно, структура и свойства продуктов превращения. Влияние степени переохлаждения на устойчивость аустенита и скорость превращения представляют графически в виде диаграмм. Эти диаграммы строят в координатах температура превращения — время. На рис. 3.2 изображена диаграмма изотермического распада аустенита для эвтектоидной стали с 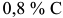 .
.
На этом рисунке кривая 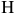 показывает начало распада аустенита, кривая
показывает начало распада аустенита, кривая 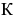 — его конец. По диаграмме ниже
— его конец. По диаграмме ниже 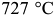 слева от кривой
слева от кривой 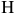 структура стали состоит из переохлажденного аустенита
структура стали состоит из переохлажденного аустенита 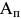 . Выдержка переохлажденного аустенита при температурах от
. Выдержка переохлажденного аустенита при температурах от 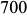 до
до 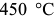 приводит к обычному распаду на эвтектоидную смесь феррита и цементита.
приводит к обычному распаду на эвтектоидную смесь феррита и цементита.
Эвтекоидная смесь феррита с цементитом растет в виде колоний из отдельных центров в аустенитных зернах. Чем больше скорость охлаждения стали, тем сильнее переохлаждается аустенит ниже 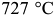 , и более тонкое внутреннее строение имеют колонии эвтектоидной смеси. В зависимости от дисперсности пластинчатой ферритоцементитной смеси различают перлит, сорбит и троостит. Перлит образуется при небольших степенях переохлаждения аустенита (охлаждение с печью со скоростью в несколько градусов в минуту), и двухфазное строение его колоний хорошо видно при увеличении 300 крат.
, и более тонкое внутреннее строение имеют колонии эвтектоидной смеси. В зависимости от дисперсности пластинчатой ферритоцементитной смеси различают перлит, сорбит и троостит. Перлит образуется при небольших степенях переохлаждения аустенита (охлаждение с печью со скоростью в несколько градусов в минуту), и двухфазное строение его колоний хорошо видно при увеличении 300 крат.
Твердость перлита 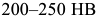 . Сорбит образуется при несколько больших степенях переохлаждения аустенита (охлаждение на воздухе со скоростью в несколько десятков градусов в минуту). Поэтому он более дисперсен и его внутреннее строение можно различить при большем увеличении.
. Сорбит образуется при несколько больших степенях переохлаждения аустенита (охлаждение на воздухе со скоростью в несколько десятков градусов в минуту). Поэтому он более дисперсен и его внутреннее строение можно различить при большем увеличении.
Сорбит обладает твердостью 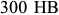 . Троостит (
. Троостит (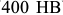 ) образуется при еще больших степенях переохлаждения аустенита (охлаждение в масле со скоростью в несколько десятков градусов в секунду). Благодаря большей дисперсности, троостит сильно растравливается, и в световой микроскоп виден сплошной темный фон шлифа.
) образуется при еще больших степенях переохлаждения аустенита (охлаждение в масле со скоростью в несколько десятков градусов в секунду). Благодаря большей дисперсности, троостит сильно растравливается, и в световой микроскоп виден сплошной темный фон шлифа.
На использовании фазовой перекристаллизации основаны разные виды отжига. Из них наиболее важен полный отжиг. Цель отжигов состоит в повышении пластических свойств металла и улучшении обрабатываемости резанием.
- Полному отжигу обычно подвергают доэвтектоидные стали, при этом нагрев ведут выше
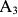 на
на 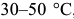 , выдерживают и медленно вместе с печью охлаждают.
, выдерживают и медленно вместе с печью охлаждают. - Неполный отжиг применяется для заэвтектоидной стали, нагрев при этом ведут выше
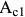 но ниже
но ниже 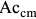 . При этих температурах в структуре сохраняется вторичный цементит. Во время выдержки при указанных температурах происходит сфероидизация пластинчатых выделений цементита.
. При этих температурах в структуре сохраняется вторичный цементит. Во время выдержки при указанных температурах происходит сфероидизация пластинчатых выделений цементита.
Обычно при отжиге второго рода сталь охлаждают медленно с печью (кривая 1 на рис. 3.2). Если после нагрева выше 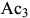 или
или 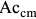 сталь охладить на спокойном воздухе, то появляющийся перлит приобретает более тонкое строение, чем после охлаждения с печью. Это приводит к повышению прочности и твердости стали. Данная разновидность термообработки называется нормализацией (кривая 3 на рис. 3.2).
сталь охладить на спокойном воздухе, то появляющийся перлит приобретает более тонкое строение, чем после охлаждения с печью. Это приводит к повышению прочности и твердости стали. Данная разновидность термообработки называется нормализацией (кривая 3 на рис. 3.2).
Кроме скорости охлаждения, на структуру стали сильно влияет температура нагрева в аустенитной области. Чем выше температура нагрева, тем более крупным вырастает аустенитное зерно и тем крупнее получаются выделения избыточного феррита и колонии эвтектоида. Если при полном отжиге доэвтектоидную сталь сильно перегреть выше точки 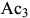 , то образуется характерная видмапштеттова структура.
, то образуется характерная видмапштеттова структура.
Из крупных зерен аустенита образуются крупные колонии перлита, а избыточный феррит выделяется в виде ориентированных пластин. В сечении шлифа эти пластины представляют собой крупные иглы. При такой структуре сталь обладает пониженной удар-ной вязкостью. Поэтому при полном отжиге и нормализации температура нагрева стали не должна значительно превышать точку 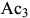 .
.
Ради экономии времени и затрат энергии сталь подвергают изотермическому отжигу, который состоит в том, что сначала сталь переводят в аустенитное состояние, а затем быстро охлаждают до температур на 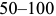 град ниже
град ниже 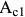 и выдерживают здесь столько времени, чтобы завершился переход переохлажденного аустенита в перлит. После этого изделие охлаждают на спокойном воздухе.
и выдерживают здесь столько времени, чтобы завершился переход переохлажденного аустенита в перлит. После этого изделие охлаждают на спокойном воздухе.
Изотермический отжиг позволяет получать более однородные свойства в разных участках объема металла, так как превращение везде идет примерно с одинаковой скоростью, тогда как при нормализации условия охлаждения на поверхности и в толще металла существенно различаются. Условия изотермического отжига изображены на рис. 3.2 линией 2.
Отжиг и нормализация чаще всего являются предварительными операциями термической обработки, осуществляемыми в целях устранения дефектов предыдущих операций (литья, ковки и др.) либо подготовки структуры для последующей обработки резанием или закалки. Нормализации — более экономичная термическая операция, чем отжиг, так как меньше времени затрачивается на охлаждение стали. Рекомендуется подвергать нормализации малоуглеродистые стали, так как у них практически отсутствует разница в свойствах после отжига и нормализации.
Возможно эта страница вам будет полезна:
| Лабораторные по материаловедению |
Закалка
При охлаждении углеродистой стали с достаточно большой скоростью, например, в холодной воде (сотни градусов в секунду), аустенит настолько сильно переохлаждается ниже 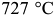 , что не распадается на смесь двух стабильных фаз, т. к. подвижность атомов при сильном переохлаждении слишком мала.
, что не распадается на смесь двух стабильных фаз, т. к. подвижность атомов при сильном переохлаждении слишком мала.
При больших переохлаждениях в условиях малой подвижности атомов происходит бездиффузионное полиморфное превращение 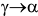 : аустенит — твердый раствор внедрения углерода в
: аустенит — твердый раствор внедрения углерода в 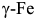 с ГЦК решеткой превращается в мартенсит — пересыщенный твердый раствор внедрения углерода в
с ГЦК решеткой превращается в мартенсит — пересыщенный твердый раствор внедрения углерода в 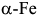 . Мартенсит — совершенно новая, метастабильная фаза. Он появляется в переохлажденном аустените при
. Мартенсит — совершенно новая, метастабильная фаза. Он появляется в переохлажденном аустените при 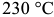 . Это отражено на диаграмме (рис. 3.2) горизонтальной линией
. Это отражено на диаграмме (рис. 3.2) горизонтальной линией 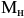 .
.
Растворимость углерода в 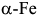 при комнатной температуре в равновесных условиях мала. В мартенсите же сохраняются все то количество углерода, которое было в исходном аустените. Поэтому мартенсит является метастабильным пересыщенным раствором углерода в
при комнатной температуре в равновесных условиях мала. В мартенсите же сохраняются все то количество углерода, которое было в исходном аустените. Поэтому мартенсит является метастабильным пересыщенным раствором углерода в 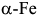 . Избыточные атомы углерода делают ОЦК решетку тетрагональной.
. Избыточные атомы углерода делают ОЦК решетку тетрагональной.
При закалке стали нагревают до температуры получения аустенита (выше критических точек), выдерживают некоторое время при этой температуре, а затем быстро охлаждают со скоростью не ниже критической. Для каждой стали существует критическая скорость закалки, под которой понимается наименьшая скорость охлаждения, необходимая для переохлаждения аустенита до температуры мартенситного превращения. На рис. 3.2 указана критическая скорость закалки 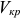 . для эвтектоидной стали.
. для эвтектоидной стали.
Температура нагрева стали при закалке зависит от содержания в ней углерода. Доэвтектоидные углеродистые стали повергают полной закалке, для этого их необходимо нагреть выше линии 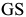 на
на 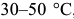 (рис. 3.4), выдержать до завершения аустенизации и охладить в воде. После такой обработки структура закаленной стали будет состоять из мартенсита и небольшого количества остаточного аустенита (рис. 3.3).
(рис. 3.4), выдержать до завершения аустенизации и охладить в воде. После такой обработки структура закаленной стали будет состоять из мартенсита и небольшого количества остаточного аустенита (рис. 3.3).
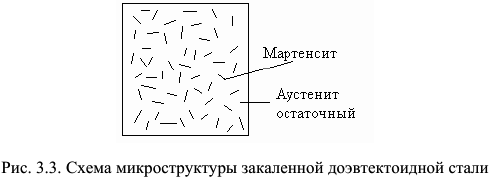
Мартенсит имеет больший объем, чем исходный аустенит, из-за чего непревращенный аустенит испытывает сильное сжатие, а пластины мартенсита располагаются по определенным кристаллографическим плоскостям. На шлифах пластины мартенсита выглядят как иглы, часто расположенные под углом 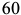 и
и 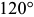 друг к другу. Начавшееся при
друг к другу. Начавшееся при 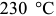 мартенситное превращение идет дальше только по мере снижения температуры.
мартенситное превращение идет дальше только по мере снижения температуры.
Появление новых количеств мартенсита продолжается до 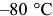 . При этой температуре в структуре остается несколько процентов аустенита (
. При этой температуре в структуре остается несколько процентов аустенита (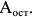 ). Температура
). Температура 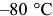 считается концом мартенситного превращения, и на диаграмме (рис. 3.2.) это отражено горизонтальной линией
считается концом мартенситного превращения, и на диаграмме (рис. 3.2.) это отражено горизонтальной линией 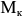 . Мартенсит резко отличается по свойствам от аустенита. Он ферромагнитен и очень тверд — твердость по Роквеллу
. Мартенсит резко отличается по свойствам от аустенита. Он ферромагнитен и очень тверд — твердость по Роквеллу 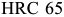 . Свойства мартенсита сталей зависят от количества растворенного в нем углерода — чем больше углерода, тем выше твердость.
. Свойства мартенсита сталей зависят от количества растворенного в нем углерода — чем больше углерода, тем выше твердость.
Закалка доэвтектоидной стали с температуры выше линии 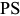 , но ниже
, но ниже 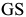 (рис. 3.4), называется неполной. В этом случае при нагреве в стали, кроме аустенита, находится также избыточный феррит. При закалке аустенит переходит в мартенсит, а феррит остается в виде мягких светлых включений на фоне мартенсита. Неполная закалка доэвтектоидной стали — это, как правило, брак термической обработки.
(рис. 3.4), называется неполной. В этом случае при нагреве в стали, кроме аустенита, находится также избыточный феррит. При закалке аустенит переходит в мартенсит, а феррит остается в виде мягких светлых включений на фоне мартенсита. Неполная закалка доэвтектоидной стали — это, как правило, брак термической обработки.
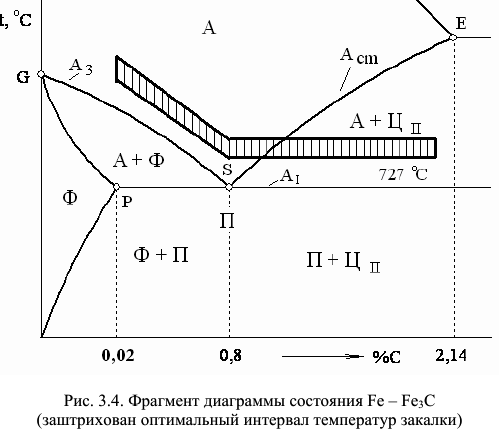
Заэвтектоидные стали нагревают выше 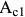 с тем, чтобы сохранить в структуре твердые включения вторичного цементита, которые за время выдержки успевают приобрести округлую форму. Структура заэвтектоидной стали после неполной закалки состоит из мартенсита, вторичного цементита и остаточного аустенита.
с тем, чтобы сохранить в структуре твердые включения вторичного цементита, которые за время выдержки успевают приобрести округлую форму. Структура заэвтектоидной стали после неполной закалки состоит из мартенсита, вторичного цементита и остаточного аустенита.
Закалка очень часто производится в воду. Водные растворы едкого натра или поваренной соли обладают большей охлаждающей способностью.
Разные сорта и марки стали имеют различную закаливаемость, т. е. способность воспринимать закалку. Закаливаемость оценивается по наибольшей твердости, получаемой в результате закалки. Как уже отмечалось, стали, содержащие менее 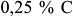 , не обладают закаливаемостью. С ростом содержания углерода закаливаемость быстро растет, достигает наибольшей величины при
, не обладают закаливаемостью. С ростом содержания углерода закаливаемость быстро растет, достигает наибольшей величины при 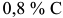 и затем почти не меняется.
и затем почти не меняется.
Важнейшим свойством стали является прокаливаемость, способность стали закаливаться на определенную глубину.
Простейший вид закалки — закалка в одной среде (режим 4, рис. 3.2). Недостаток этого способа заключается в возникновении больших напряжений в изделии из-за высокой скорости охлаждения. Закалка в двух средах (режим 5, рис. 3.2) осуществляется путем погружения изделия вначале в воду, а затем в масло.
Первоначальное охлаждение в воде позволяет быстро пройти область наименьшей устойчивости аустенита и достичь температур, при которых он более устойчив. Дальнейшее более замедленное охлаждение в масле позволяет несколько выровнять перепад температур по сечению изделия. При этом виде закалки требуется очень точно выбрать время смены закалочных сред.
Ступенчатая закалка (режим 6, рис. 3.2) состоит в том, что нагретое изделие быстро помещают в среду, имеющую температуру 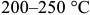 , т. е. на
, т. е. на 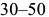 градусов выше точки начала появления мартенсита, и выдерживают некоторое время для выравнивания температуры во всем объеме. Охлаждающей средой служат расплавы селитры и щелочей.
градусов выше точки начала появления мартенсита, и выдерживают некоторое время для выравнивания температуры во всем объеме. Охлаждающей средой служат расплавы селитры и щелочей.
Затем изделие извлекают из соляной ванны и охлаждают на воздухе, при этом происходит образование мартенсита. В начале охлаждения до образования мартенсита сталь сохраняет аустенитную структуру и поэтому возможна правка покоробившихся изделий. Способ ступенчатой закалки применим лишь для небольших по размеру изделий, так как во внутренних слоях, где охлаждение идет с меньшей скоростью, может произойти обычный распад аустенита с образованием троостита или сорбита.
Изотермическая закалка осуществляется по режиму 7 на рис. 3.2. Ее также проводят в соляной ванне, имеющей температуру 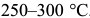 . Изотермическая закалка позволяет получать сталь с меньшей твердостью, чем после обычной закалки, но с большей вязкостью.
. Изотермическая закалка позволяет получать сталь с меньшей твердостью, чем после обычной закалки, но с большей вязкостью.
Закалка с самоотпуском заключается в том, что изделие извлекают из охлаждающей среды прежде, чем температура в средних слоях достигла 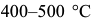 . Наружные слои в это время успевают охладиться до
. Наружные слои в это время успевают охладиться до 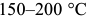 . В извлеченном из охлаждающей среды изделии за счет тепла центральных слоев наружные слои, где успел появиться мартенсит, прогреваются до
. В извлеченном из охлаждающей среды изделии за счет тепла центральных слоев наружные слои, где успел появиться мартенсит, прогреваются до 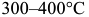 и в них происходит отпуск мартенсита.
и в них происходит отпуск мартенсита.
В результате изделие приобретает твердую корку с вязкой сердцевиной. Для закалки с самоотпуском решающее значение имеет определение температуры поверхности по цветам побежалости, появляющимся на чистой поверхность из-за возникновения слоя окислов разной толщины. Желтый цвет соответствует 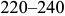 , оранжевый
, оранжевый 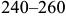 , красно-фиолетовый
, красно-фиолетовый 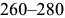 , синий
, синий 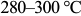 .
.
Поверхностная закалка проводится путем нагрева поверхностных слоев изделия на глубину 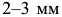 и соответствующего охлаждения. Нагрев осуществляется в индукторе токами высокой частоты. Таким образом обрабатывают шейки стальных коленчатых валов, шестерни. Нагрев поверхности больших изделий осуществляется с помощью газовых или керосиновых горелок. Поверхностная закалка позволяет получить структуру мартенсита в поверхностном слое до
и соответствующего охлаждения. Нагрев осуществляется в индукторе токами высокой частоты. Таким образом обрабатывают шейки стальных коленчатых валов, шестерни. Нагрев поверхности больших изделий осуществляется с помощью газовых или керосиновых горелок. Поверхностная закалка позволяет получить структуру мартенсита в поверхностном слое до 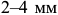 . Структура и свойства сердцевины изделия при этом не меняются, они определяются предварительной общей термообработкой всего изделия.
. Структура и свойства сердцевины изделия при этом не меняются, они определяются предварительной общей термообработкой всего изделия.
Обработка холодом была предложена русским металловедом А.П. Гуляевым. По рис. 3.2 видно, что окончание мартенситного превращения происходит при 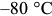 . Следовательно, при обычном охлаждении до комнатной температуры в структуре остается некоторое количество аустенита. Это значит, что не достигается наибольшее возможное значение твердости.
. Следовательно, при обычном охлаждении до комнатной температуры в структуре остается некоторое количество аустенита. Это значит, что не достигается наибольшее возможное значение твердости.
Кроме того, остаточный аустенит с течением времени может постепенно превращаться в бейнит. Из-за этого возможно изменение размеров готовых изделий. Следовательно, для ответственных деталей прецизионного оборудования, шарикоподшипников, высокоточного мерительного инструмента и т.п. желательно наиболее полно перевести аустенит в мартенсит. Это достигается охлаждением до температуры 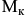 . Важно, чтобы охлаждение после обычной закалки происходило как можно быстрее, иначе сохранившийся аустенит становится устойчивым и не столь полно превращается в мартенсит.
. Важно, чтобы охлаждение после обычной закалки происходило как можно быстрее, иначе сохранившийся аустенит становится устойчивым и не столь полно превращается в мартенсит.
Отпуск
Вслед за закалкой стальные изделия обычно подвергают отпуску, поскольку в закаленном состоянии сталь слишком тверда и хрупка и находится в напряженном состоянии.
При отпуске закаленную на мартенсит сталь нагревают до температуры ниже 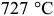 . Основное превращение при отпуске стали — распад мартенсита. При нагреве до
. Основное превращение при отпуске стали — распад мартенсита. При нагреве до 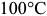 происходит собирание атомов углерода в отдельных участках решетки мартенсита. Затем в интервале
происходит собирание атомов углерода в отдельных участках решетки мартенсита. Затем в интервале 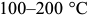 наблюдается образование промежуточного карбида железа, отличного от устойчивого карбида
наблюдается образование промежуточного карбида железа, отличного от устойчивого карбида 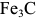 . При
. При 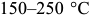 тетрагональная ячейка мартенсита становится кубической. Выше
тетрагональная ячейка мартенсита становится кубической. Выше 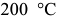 начинается образование частиц
начинается образование частиц 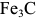 , которые затем постепенно укрупняются и сфероидизируются.
, которые затем постепенно укрупняются и сфероидизируются.
Остаточный аустенит интенсивно распадается при 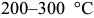 на феррит и промежуточные карбиды. После нагрева ниже
на феррит и промежуточные карбиды. После нагрева ниже 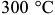 видимых изменений структуры не наблюдается. Отпуск при
видимых изменений структуры не наблюдается. Отпуск при 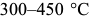 приводит к исчезновению мартенсита и появлению игольчатого троостита, в котором полностью обособляются частицы цементита. Выше
приводит к исчезновению мартенсита и появлению игольчатого троостита, в котором полностью обособляются частицы цементита. Выше 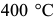 наблюдается укрупнение частиц цементита. Карбид образуется в пределах исходных мартенситных игл.
наблюдается укрупнение частиц цементита. Карбид образуется в пределах исходных мартенситных игл.
Поэтому микроструктура отпущенной стали сохраняет игольчатый характер и похожа на мартенсит. Этим двухфазная феррито-карбидная смесь, получающаяся при распаде мартенсита, отличается от феррито-цементитной смеси, образующийся при распаде переохлажденного аустенита. Нагрев до 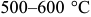 приводит к образованию сорбита отпуска, в котором частицы цементита приобретают округлую форму. Перечисленные изменения структуры сопровождаются соответствующими изменениями механических свойств.
приводит к образованию сорбита отпуска, в котором частицы цементита приобретают округлую форму. Перечисленные изменения структуры сопровождаются соответствующими изменениями механических свойств.
На практике применяют низкотемпературный (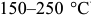 ), сред-нетемпературный (
), сред-нетемпературный (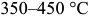 ) и высокий (
) и высокий (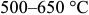 ) отпуск.
) отпуск.
Структуру, получающуюся при низком отпуске стали, называют отпущенным мартенситом: она отличается от мартенсита закалки большей травимостью из-за дисперсных выделений карбида. После среднего отпуска обнаруживается особенно сильно травящаяся игольчатая структура, которую называют трооститом отпуска.
Сильная травимость троостита отпуска обусловлена высокой дисперсностью этой двухфазной смеси. При высоком отпуске получается сорбит отпуска. Цементит в нем находится в виде сферических частиц. Двухфазное строение сорбита отпуска отчетливо выявляется при небольших увеличениях.
Кстати дополнительная теория из учебников тут.
Низкий отпуск иногда вызывает прирост твердости 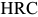 на 1-2 в результате распада остаточного аустенита. Низкотемпературный отпуск применяют для инструментальных сталей, изделий после цементации и поверхностной закалки.
на 1-2 в результате распада остаточного аустенита. Низкотемпературный отпуск применяют для инструментальных сталей, изделий после цементации и поверхностной закалки.
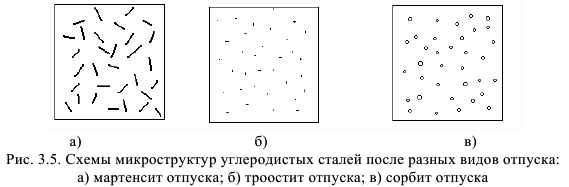
Среднему отпуску подвергают пружинную и рессорную сталь и получают структуру троостита с твердостью  40-45 при достаточной вязкости. При высоком отпуске при соответствующей выдержке в структуре образуется зернистый сорбит. Высокий отпуск после закалки проводят для деталей, испытывающих при работе знакопеременные и ударные нагрузки. Закалку с высоким отпуском называют также улучшением.
40-45 при достаточной вязкости. При высоком отпуске при соответствующей выдержке в структуре образуется зернистый сорбит. Высокий отпуск после закалки проводят для деталей, испытывающих при работе знакопеременные и ударные нагрузки. Закалку с высоким отпуском называют также улучшением.