| 🎓 Заказ №: 22228 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
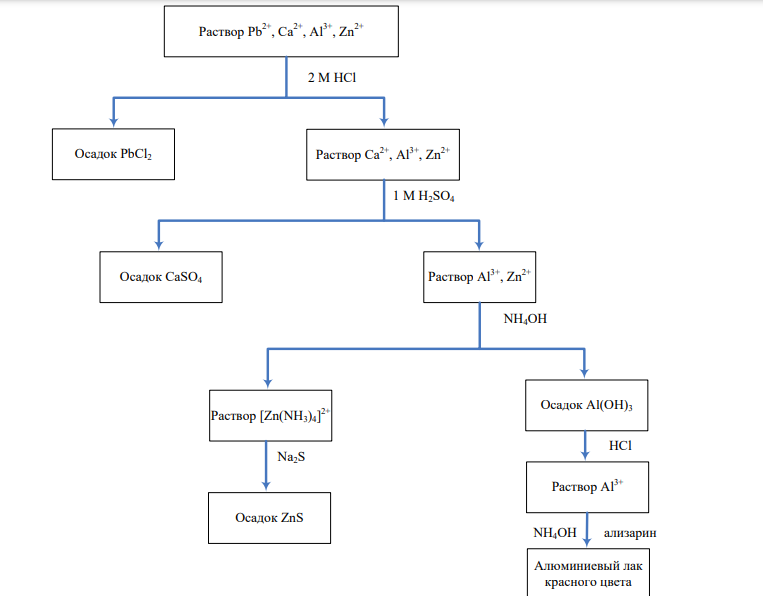
Pb2+ , Ca2+ , Al3+ , Zn2+. Составить схему анализа, написать уравнения реакций разделения и обнаружения каждого иона.
Решение: 328 Осадок PbCl2 Раствор Pb2+ , Ca 2+ , Al 3+ , Zn2+ Осадок ZnS Раствор Ca 2+ , Al 3+ , Zn2+ Раствор Al 3+ , Zn2+ Осадок CaSO4 2 M HCl 1 M H2SO4 NH4OH Раствор [Zn(NH3)4] 2+ Na2S Осадок Al(OH)3 Раствор Al 3+ HCl Алюминиевый лак красного цвета NH4OH ализарин Вначале проводим отделение ионов свинца. На анализируемый раствор действуем 2М раствором хлороводородной кислоты. Происходит выпадение белого осадка хлорида свинца. Pb 2HCl PbCl2 2H 2 Осадок растворяется в избытке осадителя 2 [ ] PbCl2 HCl H2 PbCl4 Для дополнительного подтверждения наличия ионов свинца воздействуем на осадок хлорида свинца раствором йодида калия. Поскольку произведение растворимости йодида свинца (8,0∙10-10) намного меньше произведения растворимости хлорида свинца (2∙10-5 ), один осадок переходит в другой, белый цвет осадка меняется на желтый. PbCl2 2KI 2KCl PbI2


| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Дайте обоснование определению подлинности ингредиентов лекарственной смеси.
- Рассчитать навеску (г) нитрита калия в 0,5 дм3 раствора, если рН раствора равен 10.
- В мерной колбе вместимостью 500,00 см3 приготовлен раствор карбоната натрия из навески массой 2,5000 г.
- Определить направление протекания взаимодействия между ионами железа(III) и йодид ионами.
- Среди солей – Na2CO3, NH4NO2, CH3COONH4, Na2SO4, NH4Cl – указать соли, гидролизующиеся по катиону и аниону.
- Реакции выражаются схемами: H2S + Cl2 + H2O H2SO4 + HCl
- Стандартные (установочные) вещества, применяемые для стандартизации титрованного раствора тиосульфата натрия.
- Коэффициент поправки титранта и пределы его значений.
- Дописать уравнения реакций и уравнять ионно-электронным методом (метод полуреакций): а) 1) K4[Fe(CN)6] + KMnO4 + H2SO4 2) NaNO3 + Cu + H2SO4 3) K2Cr2O7 + FeCl2 + HCl
- Классификация методов осаждения.
