Некоторые правила определения степеней окисления элементов в химических соединениях
1. Степень окисления атомов в простых веществах равна нулю.
Например; 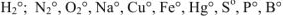 и др.
и др.
2. Атомы кислорода в основных классах неорганических соединений проявляют степень окисления (-2).
Например: 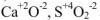 и т.д.
и т.д.
Исключения: фторид кислорода 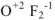 — степень окисления кислорода (+2), пероксиды — степень окисления кислорода
— степень окисления кислорода (+2), пероксиды — степень окисления кислорода
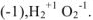
3. Атом водорода в основных классах неорганических соединений проявляет степень окисления (+ 1).
Например: 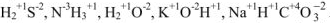
Исключения: гидриды металлов типа 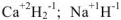 ; в которых степень окисления водорода (-1).
; в которых степень окисления водорода (-1).
4. Металлы 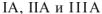 главных подгрупп Периодической системы проявляют степень окисления равную номеру группы в которой находится этот элемент т.с. соответственно (+1), (+2) и (+3) (см. табл. 1.2).
главных подгрупп Периодической системы проявляют степень окисления равную номеру группы в которой находится этот элемент т.с. соответственно (+1), (+2) и (+3) (см. табл. 1.2).
Например: 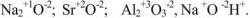
5. Алгебраическая сумма степеней окисления отдельных атомов, образующих молекулу, с учетом их стехиометрических индексов равна нулю. Например, можно определить степень окисления азота в молекуле 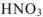 , зная степени окисления кислорода (-2) и водорода (+1):
, зная степени окисления кислорода (-2) и водорода (+1): 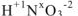
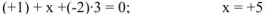
или степень окисления хрома в молекуле 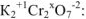
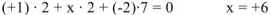
Большинство элементов могут проявлять переменную степень окисления в соединениях. Например:
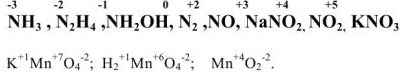
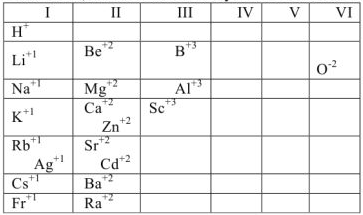
Элементы, имеющие постоянную степень окисления в большинстве соединений
Эта теория взята со страницы помощи по химии:
Возможно эти страницы вам помогут:
| Оксиды. Классификация. Свойства. Номенклатура |
| Кислоты и основания. Классификация. Свойства. Номенклатура |
| Электрохимическая коррозия в химии |
| Коррозия металлов с кислородной деполяризацией в химии |

