Оглавление:


Направление и пределы самопроизвольного течения химических реакций
- Направление и ограничения естественного потока химических веществ Реакция. Согласно (IV. 19) и (IV. 21) Для самой большой работы Энергия Гельмгольца A f и энергия Гиббса D (7 химия Реакция. Другими словами, при постоянной температуре и давлении Реакция протекает естественно в этом направлении Это соответствует уменьшению энергии Гиббса системы (G i <, G ). поэт.
- Условия естественного хода химических реакций Учитывая р и 7 «неравенства d s ,, <0. (IV.25) Предел спонтанного течения ответа при р, Т = = const, т.е. условием равновесия является достижение мини Минимальное значение данных p и Γ функции G (Ор, ‘т) — Реакция протекает при определенной температуре и объеме Добровольно в направлении, соответствующем снижению Энергия системы Гельмгольца {F 2 <.F ).
Поэтому в условиях самопроизвольного протекания химической реакции с ладаном. Людмила Фирмаль
Это неравенство l ^ .l 0 ). Это значит Там нет спонтанной реакции. неравенство (IV.27) Означает, что реакция может происходить только спонтанно Противоположное направление, соответствующее уменьшению энергии Гиббса Система. Рассчитать стандартную химическую энергию Гиббса 298.16 KAíÍwr реакция и обнаружение признаков восстания Функция G проста.
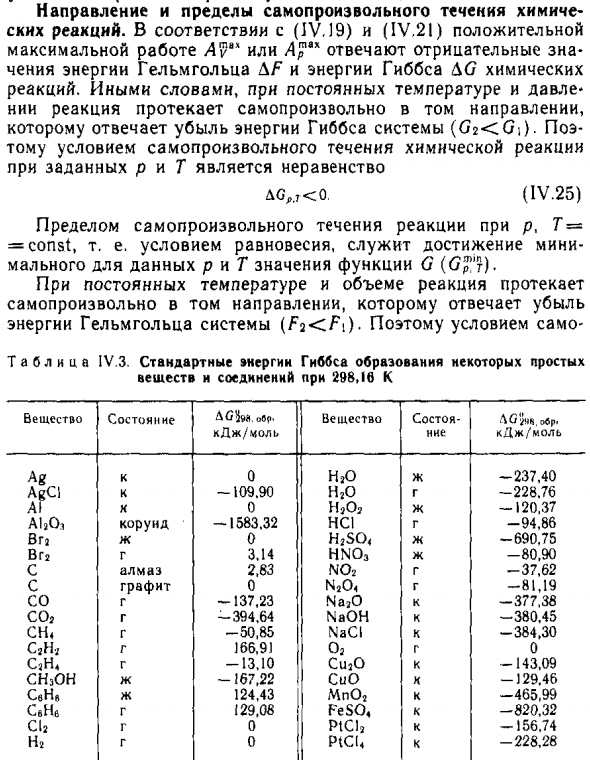
Например, Исаоли: у меня есть данные: «ТКБл можно, можно ра». Является ли стандартная энергия HbF.h. для реакции Nin (jOIk) + H. 1 () (х) = 2NaOH (к) 298,16 К на 1 моль Na ^ O: 2СC2 », фут p ^ й (() П (Ч) -AG 2КC, Л |> NuiOlK) — | ljC) (/ К) — = 2 (-380,45) + 377,38-b237,40 = -146,12 кДж / моль, Полученная энергия реакции Гиббса не имеет значения (IV-25) — это означает процесс взаимодействия при 101 кПа и 298 К. Оксид натрия и вода могут протекать естественным путем.
1 объемная пила Значение NaOH (k), Однако стандартная энергия Гиббса для химических озер равна «1, им LSH не будет эталоном направления или нпене. случайный поток химических взаимодействий в у Да. Это отличается от стандарта. Невозможно заменить AGt — это значение Дожа. Это делает его немного сложнее в использовании.
Энергия Гиббса для оценки фактического процесса условия Из формулы (IV.22) 7 ‘= const и энергия Чем меньше химической реакции \ G, тем больше АН и Больше как. Высочайшее химическое сродство между веществами Выявлено реакцией с выделением тепла (Я << 0) и увеличенная энтропия системы (5 5> 0). Из формулы (IV .22) Эндотермический процесс (Д / ^> 0), утечка Снижение энтропии (Д5- <0) Всегда положительный в DO.
- Эндотермическое взаимодействие. Действие (D //> 0) может быть выполнено только спонтанно при этом условии 7’D5> D // Этот вид взаимодействия Это увеличивает значение энтропии, ТАС факторы процесса. Следовательно, реакция при постоянной температуре и давлении Он самопроизвольно развивается в направлении уменьшения энергии Гиббса.
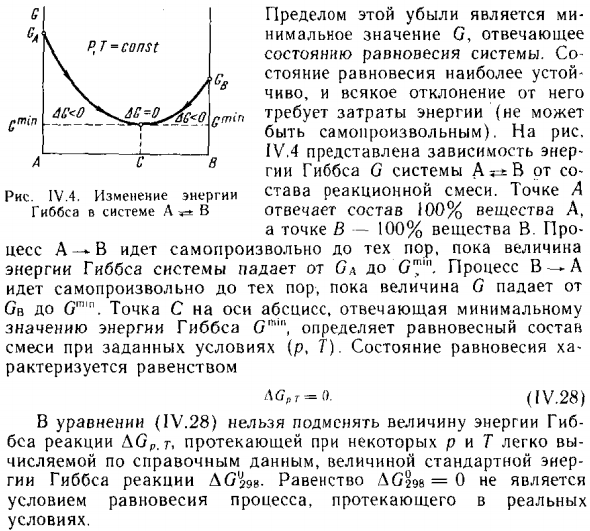
Этот предел потерь является ми Минимальное значение O, соответствующее Системное равновесие. и Равновесие является наиболее стабильным Чисто и любое отклонение от него . Рисование IV.4 показывает энергетическую зависимость Из теории Гиббса I ± B системы A Рисунок 1U.4, Изменение энергии от реакционной смеси.
Мне нужна энергия Это добровольное) Людмила Фирмаль
Указать 100% вещества A B, ответственного в системе, Точка B-100% Вещества B. Cess A- ^ B это количество Энергия Гиббса системы падает от C a d o процесса B A Значение С Ov to O «» «. Точка C на горизонтальной оси, соответствующая минимальному значению Энергетическая величина Гиббса 0 «» ‘\ определяет равновесный состав Смесь при определенных условиях (р, Т).
Состояние равновесия, га Особенности равенства = (IV.28) В уравнении (IV .28) величина энергии Гиббса не может быть заменена bsa реакция легко протекает при AOP, t, некоторых p и T Рассчитано с использованием справочных данных и стандартной энергии Реакция Гиббса GI равенство К 298 = 0 Равновесное состояние реального процесса условия
Смотрите также:
| Энергия Гельмгольца химической реакции | Константа равновесия |
| Энергия Гиббса образования химических соединений | Общие представления о скорости химических реакций |
Если вам потребуется помощь по химии вы всегда можете написать мне в whatsapp.

