| 🎓 Заказ №: 22215 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Молярная концентрация. Молярная концентрация эквивалента (нормальная концентрация). Взаимный переход от одних видов выражения концентрации к другим а) Определите молярность и нормальность растворов, содержащих: 310 в 0,3 л 32,44 г хлорида железа (III)
Решение: Молярность (молярная концентрация растворенного вещества) – отношение количества растворенного вещества к объему раствора. ( ) ( ) ( ) 3 3 3 V р ра FeCl n FeCl C FeCl M Количество вещества равно отношению массы вещества к молярной массе вещества ( ) ( ) ( ) 3 3 3 M FeCl m FeCl n FeCl Молярная масса хлорида железа (III) равна M(FeCl ) 162,2 г/ моль 3 Находим молярность раствора C FeCl M 0,667 / 162,2 0,3 32,44 ( ) ( ) ( ) ( ) 3 3 3


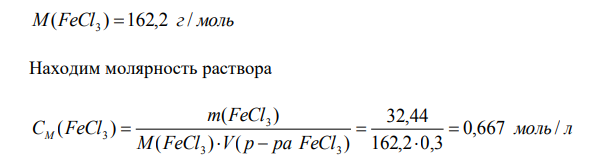
| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Составьте уравнения реакций, расставив коэффициенты методом электронноионного (или электронного) баланса: № задания Металл Окислитель 666. Pb HNO3 (разб.)
- Приведена схема гальванического элемента. Разберите работу гальванического элемента. Mg | Mg(NO3)2 || Al2(SO4)3 | Al, 10 / ; 10 / . 2 3 C 2 моль л C 3 моль л Mg Al
- Методом электронного баланса подберите коэффициенты в уравнениях реакций. Укажите окислитель и восстановитель, процессы окисления и восстановления.
- Методом электронного баланса подберите коэффициенты в уравнениях реакций. KMnO4 NH3 MnO2 KNO3 KOH H2O
- Методом электронного баланса подберите коэффициенты в уравнениях реакций. Fe2O3 KNO3 KOH K2FeO4 KNO2 H2O
- Охарактеризуйте особенности строения полимеров (геометрическая форма макромолекул, строение, молекулярная масса). Каковы общие физи-ческие свойства полимеров?
- Соотнесите функциональную группу (ФГ), реактивы и внешний эффект реакции с её типом, напишите химизм реакции и обоснуйте ( Прокаина гидрохлорид )
- Соотнесите функциональную группу (ФГ), реактивы и внешний эффект с типом реакции, используемой для доказательства подлинности ЛС (напишите химизм реакции) (Метионин)
- Методом электронного баланса подберите коэффициенты в уравнениях реакций. KMnO4 +NH3 → MnO2 + KNO3 + KOH + H2O, MnO2 + HCl → MnCl2 + Cl2 + H2O.
- Соотнесите функциональную группу (ФГ), реактивы и внешний эффект реакции с её типом, напишите химизм реакции и обоснуйте ( Ацетилсалициловая кислота )
