| 🎓 Заказ №: 22194 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
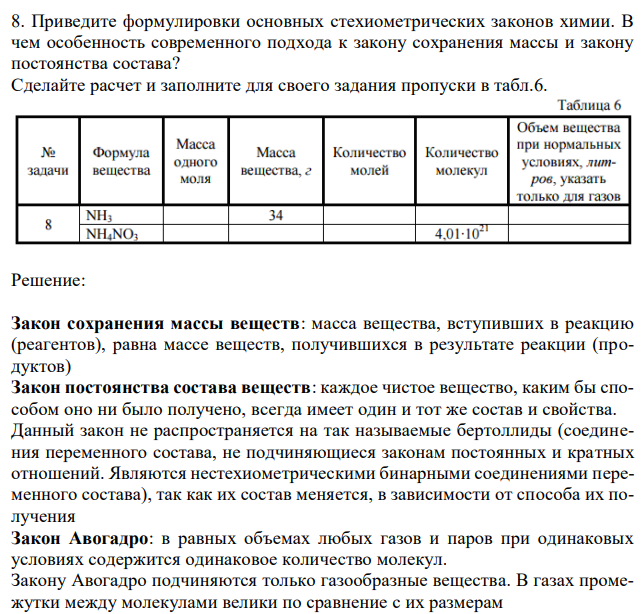
Приведите формулировки основных стехиометрических законов химии. В чем особенность современного подхода к закону сохранения массы и закону постоянства состава? Сделайте расчет и заполните для своего задания пропуски в табл.6.
Решение: Закон сохранения массы веществ: масса вещества, вступивших в реакцию (реагентов), равна массе веществ, получившихся в результате реакции (продуктов) Закон постоянства состава веществ: каждое чистое вещество, каким бы способом оно ни было получено, всегда имеет один и тот же состав и свойства. Данный закон не распространяется на так называемые бертоллиды (соединения переменного состава, не подчиняющиеся законам постоянных и кратных отношений. Являются нестехиометрическими бинарными соединениями переменного состава), так как их состав меняется, в зависимости от способа их получения Закон Авогадро: в равных объемах любых газов и паров при одинаковых условиях содержится одинаковое количество молекул. Закону Авогадро подчиняются только газообразные вещества. В газах промежутки между молекулами велики по сравнение с их размерам
| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Какова нормальность раствора NaOH, если на нейтрализацию 150 мл этого раствора пошло 80 г 5 % раствора серной кислоты 1,05 / ?
- Для умягчения 300 л воды потребовалось 15 г карбоната натрия.
- Назовите комплексное соединение А (табл.12).
- Для соединений А, Б и В выпишите из справочной литературы значения константы нестойкости (см. прил.3), сравните устойчивость комплексных соединений.
- Уравняйте реакции, укажите окислитель и восстановитель: PH3 + KMnO4 + H2SO4 → H3PO4 + MnSO4 + K2SO4 + H2O F2 + H2O → HF + O2
- Определите объем газа, выделившегося при растворении в избытке кон-центрированной H2SO4 смеси, полученной при действии 6,72 л водорода (при н.у.) на 30 г CuO.
- Составьте электронные формулы и представьте графически размещение электронов по квантовым ячейкам для указанных в табл.8 элементов, соответствующих вашему заданию.
- Вычислите теплоту образования гидроксида кальция по данным таблицы 1 и тепловому эффекту реакции 3 ( ) ( ) 3 , 341,8 . 2 2 5 3 4 2 2 ( ) Ca OH P O Ca PO H O газ H кДж
- Сделайте предварительный расчет объёма 1 М раствора натрия гидроксида, который должен израсходоваться при количественном определении хлористоводородной кислоты разведенной по методике ФС.2.2.0035.18 (Приложение № 3).
- Осмотическое давление водного раствора, содержащего в 100 мл 1 г сахарозы С12H22O11, равно 0,655 атм при 0ºC. Рассчитайте величину универсальной газовой постоянной R.
