| 🎓 Заказ №: 22184 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
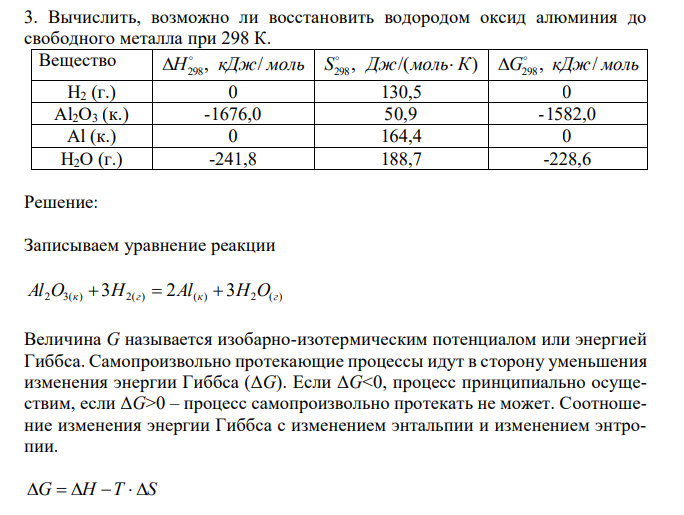
Вычислить, возможно ли восстановить водородом оксид алюминия до свободного металла при 298 К. Вещество H , кДж/ моль 298 , /( ) S298 Дж мольК G , кДж/ моль 298 H2 (г.) 0 130,5 0 Al2O3 (к.) -1676,0 50,9 -1582,0 Al (к.) 0 164,4 0 H2O (г.) -241,8 188,7 -228,6
Решение: Записываем уравнение реакции Al2O3(к) 3H2(г) 2Al(к) 3H2O(г) Величина G называется изобарно-изотермическим потенциалом или энергией Гиббса. Самопроизвольно протекающие процессы идут в сторону уменьшения изменения энергии Гиббса (ΔG). Если ΔG<0, процесс принципиально осуществим, если ΔG>0 – процесс самопроизвольно протекать не может. Соотношение изменения энергии Гиббса с изменением энтальпии и изменением энтропии. G H T S
| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Как следует изменить температуру, чтобы сместить равновесие влево в следующих системах: а) 2 , 172,5 ; 2 С СO CO H кДж б) 2 3 , 85,6 . 2 2 6 С H C H H кДж
- Используя термодинамические данные рассчитать константу равновесия системы N2 + 3Н2 ↔ 2NН3 при 450 ºС (зависимостью ΔН и ΔS от температуры пренебречь).
- Водный раствор содержит 784 г H2SO4 в объеме 1 л.
- Зависит ли скорость коррозионного процесса с водородной деполяризацией от величины рН?
- Написать уравнения диссоциации следующих соединений: Ni(OH)2, HF, Al2(SO4)3, KH2PO4.
- Ток силой 10 А проходит через электролизер, в котором находится 0,5 л 4,5 %-го раствора NаОН (плотность 1,06 г/мл).
- Охарактеризуйте электронное строение карбоксильной группы.
- Какие характеристики электрона и электронной орбитали в атоме отражает орбитальное квантовое число l?
- Методом электронного баланса составить уравнения окислительно-восстановительных реакций.
- Написать уравнения реакций, при которых можно осуществить превращения: Na → NaOH → Na2CO3 → NaNO3
