| 🎓 Заказ №: 22216 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
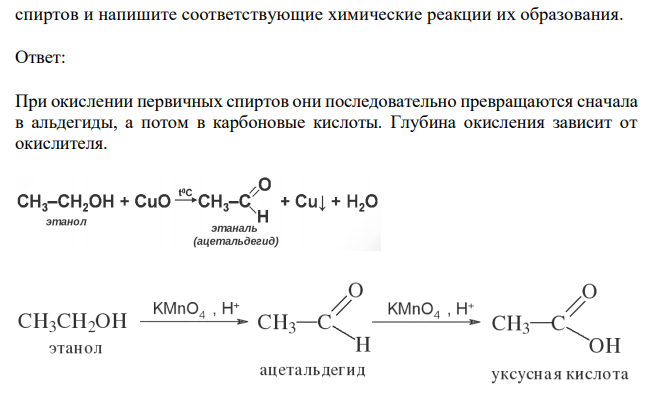
Перечислите продукты окисления первичных, вторичных и третичных спиртов и напишите соответствующие химические реакции их образования.
Решение При окислении первичных спиртов они последовательно превращаются сначала в альдегиды, а потом в карбоновые кислоты. Глубина окисления зависит от окислителя. Вторичные спирты окисляются в кетоны.

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Как изменится скорость реакции SO2 + 2H2S = 3S + 2H2O, если: 204 а) увеличить концентрацию оксида серы (IV) в 3 раза; б) увеличить концентрацию сероводорода в 3 раза; в) увеличить концентрацию и оксида серы (IV) и сероводорода в 3 раза?
- Рассчитать изменение стандартной свободной энергии Гиббса и сделать вывод о направлении процесса: МоО3(тв) + СО(г) ↔ Мо(тв) + СО2(г) при температуре 700 ºС.
- Рассчитать теплотворную способность каменного угля беззольного.
- Охарактеризуйте изомеры у двух- и трехатомных фенолов.
- Рассчитать, сколько граммов Ca(HCO3)2 содержится в 1 м3 воды, жесткость которой равна 3 мэкв/л
- Написать в ионно-молекулярной и молекулярной форме уравнения реакций, протекающих при смешивании водных растворов солей и объяснить механизм их протекания: Pb(CH3COO)2 + Na2S.
- Произведение растворимости Аg3АsО4 составляет 1∙10-22.
- Рассчитать объем кислорода, необходимый для сжигания 700 л Н2S.
- Температура плавления кобальта 1490 ºС.
- Составить полные структурные формулы изомеров, имеющих состав С5H12.
