| 🎓 Заказ №: 22193 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Приведите способы получения: а) пропана реакцией Вюрца, б) бутана пиролизом натриевой соли пентановой кислоты, в) 2,3-диметилгексана электролизом изомасляной кислоты. Охарактеризуйте химические свойства алканов. Напишите схемы получения 2-метил-2-гексена из: а) спирта, б) галогенпроизводного. Сформулируйте правило Зайцева. На 2-метил-2-гексен подействуйте молекулой брома, затем спиртовым раствором щелочи. Напишите уравнения реакций, назовите продукты. Приведите структурные формулы всех изомерных алкинов состава C5H8. Назовите по рациональной и международной номенклатурам. Отметьте среди них соединения, способные проявлять кислотные свойства, приведите уравнения реакций.
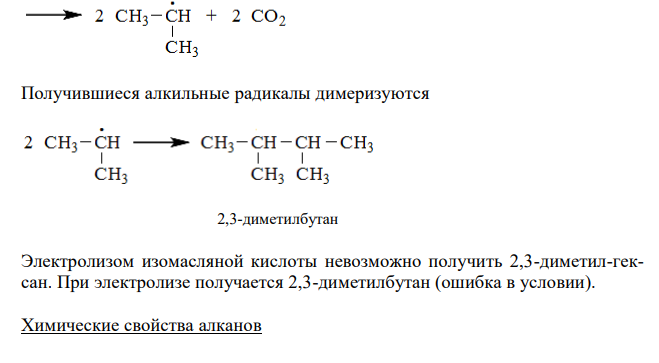
Решение: а) поскольку пропан относится к углеводородам несимметричного строения, то для его получения (реакцией Вюрца) необходимо действовать натрием на смесь двух алкилгалогенидов (например, йодметана и йодэтана). При этом получится смесь трех алканов (этана, пропана и бутана): б) При нагревании натриевой соли пентановой кислоты в присутствии щелочи при температуре 250-300 ºС происходит разложение и выделяется бутан в) при электролизе (электросинтез Кольбе) водного раствора изомасляной кислоты анион (CH3)2CHCOO – отдает на аноде электрон (окисляется), образуя свободный радикал (CH3)2CHCOO ● , который в свою очередь разлагается на СО2 и алкильный радикал (CH3)2CH ● Получившиеся алкильные радикалы димеризуются 2,3-диметилбутан Электролизом изомасляной кислоты невозможно получить 2,3-диметил-гексан. При электролизе получается 2,3-диметилбутан (ошибка в условии). Химические свойства алканов Алканы – химически наименее активные органические соединения. Все связи С–С и С–Н в них одинарные, поэтому алканы неспособны к реакциям присоединения. Для алканов характерны реакции замещения атомов водорода на другие атомы и группы атомов. Галогенирование. Фторирование алканов идет с очень высокой, часто взрывной, скоростью с образованием всех возможных полифторпроизводных исходного алкана. Чаще происходит полное разрушения углеродного скелета атомами фтора. C2H6 + 7F2 → 2CF4 + 6HF Хлорирование алканов идет по радикальному цепному механизму. Под действием света (реже тепла) происходит процесс инициации (зарождения цепи). Cl2 → 2 Cl· Затем атом хлора атакует атом водорода в молекуле алкана. Происходит отрыв водорода и образование свободного алкильного радикала. RCH3 + Cl → RCH2 + HCl Далее алкильный радикал атакует молекулу хлора и цепная реакция продолжается (продолжение цепи) RCH2· + Cl2 → RCH2Cl + Cl· Реакция хлорирования идет до тех пор, пока не произойдет обрыв цепи – уничтожение ведущего цепь радикала. Обрыв может произойти по одной из следующих реакций 2 Cl· → Cl2 RCH2· + RCH2·→ RCH2CH2R RCH2· + Cl·→ RCH2Cl При хлорировании метана образуются метилхлорид CH3Cl, метиленхлорид CH2Cl2, трихлорметан (хлороформ) CHCl3 и тетрахлорид углерода (четыреххлористый углерод) CCl4. При хлорировании алканов, начиная с пропана, первый же атом хлора может заместить разные атомы водорода. Направление замещения зависит от прочности связи С–Н. Первичные связи С–Н, как правило, прочнее вторичных, а вторичные прочнее третичных. Из нескольких возможных продуктов хлорирования будет преобладать только один.




| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Вычислите rG (298 К) и определите возможность осуществления в стандартных условиях реакции N2O(г) + 0,5O2(г) = 2NO(г).
- Укажите значение органической химии в системе фармацевтического образования.
- В каких единицах определяется скорость химических реакций ?
- Какие из веществ – NaCl, Ni(OH)2, Be(OH)2, KHCO3 – взаимодействуют с раствором гидроксида натрия?
- Гальванический элемент состоит из цинка, погруженного в 0,1 М Zn(NO3)2 и водородного электрода с рН = 1.
- Какая масса меди выделится на катоде при электролизе CuSO4 в течение 1 ч при силе тока 4 А?
- Написать координационную формулу комплексного соединения: дицианоаргентат калия.
- Написать уравнения реакций, при которых можно осуществить превращения: Al → Al2(SO4)3 → Al(OH)3 → Na3[Al(OH)6] → AlCl3
- Приведите определение кислот по теории Бренстеда. Примеры.
- Приведите определение оснований по теории Льюиса. Примеры.
