| 🎓 Заказ №: 22171 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
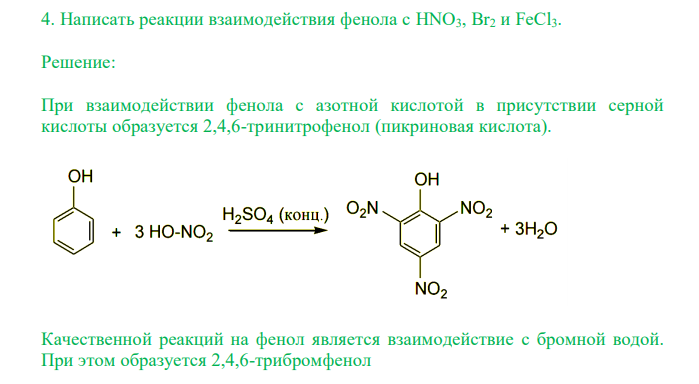
Написать реакции взаимодействия фенола с HNO3, Br2 и FeCl3.
Решение: При взаимодействии фенола с азотной кислотой в присутствии серной кислоты образуется 2,4,6-тринитрофенол (пикриновая кислота). Качественной реакций на фенол является взаимодействие с бромной водой. При этом образуется 2,4,6-трибромфенол
| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Составьте схему электролиза раствора электролита, чтобы на катоде получить Н2, на аноде – Cl2 объемом 112 л (н.у.).
- Уравняйте реакции методом электронного баланса, укажите окислитель и восстановитель: а) Fe2S3 + HCl → FeCl2 + H2S + S б) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O в) Fe(OH)3 + KOH + Br2 → K2FeO4 + KBr + H2O
- Рассчитайте давление в сосуде: 1.1.1. объемом 5 л, содержащем 16 г кислорода и 28 г азота при 0ºС
- Какую массу сероводорода можно окислить до свободной серы одним граммом йода?
- Какую массу сульфата железа (II) можно окислить в кислой среде с помощью 20 мл 0,1 н раствора перманганата калия?
- Дайте заключение о качестве магния сульфата (М.м. магния сульфата гептагидрата 246,47) порошка для приготовления раствора для приема внутрь 20,0 г по количественному содержанию с учетом требования ГФ XIV, 60 ФС.3.2.0007.18 (должно быть не менее 90,0 % и не более 110,0 % от заявленного количества магния сульфата гептагидрата), если на титрование 0,1492 г порошка израсходовалось 12,30 мл 0,05 М раствора натрия эдетата (К = 0,9998).
- На нейтрализацию 31 мл 0,16 н. раствора щелочи требуется 217 мл раствора серной кислоты.
- Для водного раствора Cd(NO3)2 напишите уравнения процессов, идущих на графитовых электродах при электролизе; рассчитайте, сколько и каких веществ выделится на катоде и аноде, если электролиз вести при силе тока 1 А в течение времени 1,5 час.
- Вычислить электродные потенциалы положительного и отрицательного электродов и ЭДС гальванического элемента. Zn|ZnSO4 (0,01 М) || ZnSO4 (2,0 М)|Zn
- Вычислите эквивалентную массу: 1.2.1. азота в оксидах N2O, NO, NO2
