| 🎓 Заказ №: 22180 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
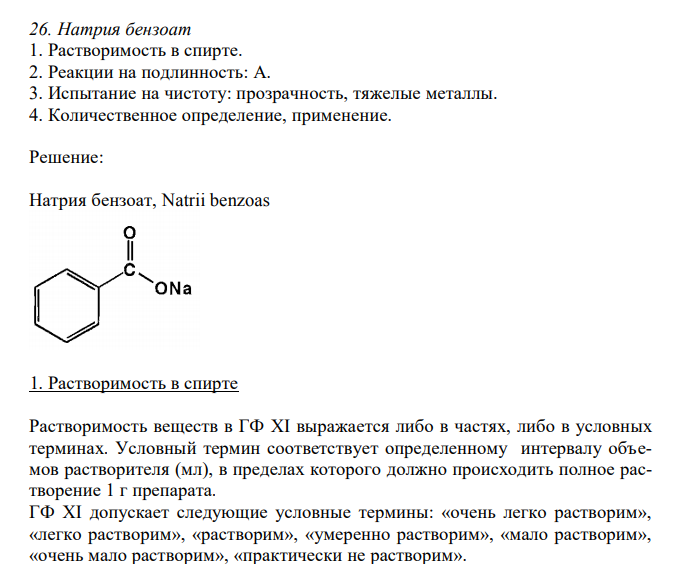
Натрия бензоат 1. Растворимость в спирте. 2. Реакции на подлинность: А. 3. Испытание на чистоту: прозрачность, тяжелые металлы. 4. Количественное определение, применение.
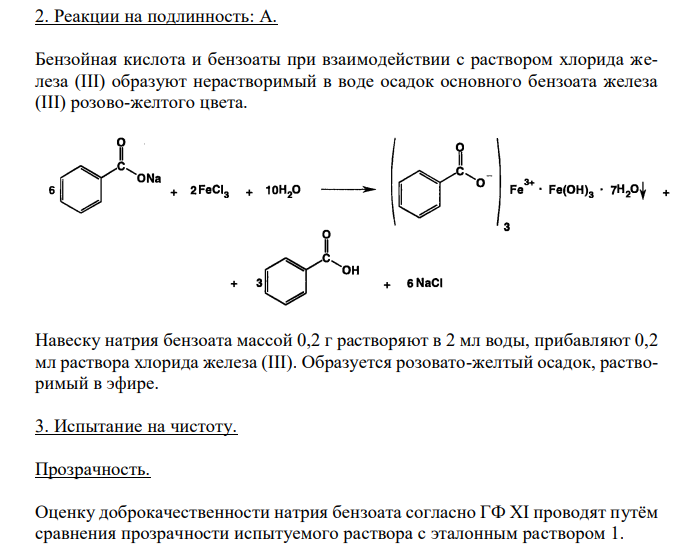
Решение: Натрия бензоат, Natrii benzoas 1. Растворимость в спирте Растворимость веществ в ГФ XI выражается либо в частях, либо в условных терминах. Условный термин соответствует определенному интервалу объемов растворителя (мл), в пределах которого должно происходить полное растворение 1 г препарата. ГФ XI допускает следующие условные термины: «очень легко растворим», «легко растворим», «растворим», «умеренно растворим», «мало растворим», «очень мало растворим», «практически не растворим». Согласно ФС 42-2458-94, натрия бензоат умеренно растворим в спирте 90 %. То есть, для растворения 1 г препарата необходим объем спирта 90 % от 30 до 100 мл. Для подтверждения подлинности и доброкачественности навеску предварительно растертого натрия бензоата массой 1,00 г вносят в 30 мл спирта 90 % и непрерывно встряхивают в течение 10 мин при 20 ± 2°С. Препарат считают растворившимся, если в растворе при наблюдении в проходящем свете не обнаруживаются частицы вещества. В случае неполного растворения препарата постепенно небольшими порциями прибавляют спирт 90 % (до объема 100 мл) при непрерывном встряхивании. Если навеска полностью растворится в объеме спирта 90 % от 30 до 100 мл, то делают вывод о доброкачественности препарата. 281 2. Реакции на подлинность: А. Бензойная кислота и бензоаты при взаимодействии с раствором хлорида железа (III) образуют нерастворимый в воде осадок основного бензоата железа (III) розово-желтого цвета. Навеску натрия бензоата массой 0,2 г растворяют в 2 мл воды, прибавляют 0,2 мл раствора хлорида железа (III). Образуется розовато-желтый осадок, растворимый в эфире. 3. Испытание на чистоту. Прозрачность. Оценку доброкачественности натрия бензоата согласно ГФ XI проводят путём сравнения прозрачности испытуемого раствора с эталонным раствором 1.

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Почему в алюминиевой посуде нельзя приготовить горячий раствор соды (Na2CO3)? Напишите уравнения возможных реакций.
- С помощью метода электронного баланса расставьте коэффициенты в уравнениях окислительно-восстановительных реакций. Для каждого уравнения укажите, какое вещество является окислителем, какое восстановителем, а также процесс восстановления-окисления. H2SO3 + HClO3 → HCl + H2SO4 FeSO4 + K2Cr2O7 + H2SO4 →Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O
- Реакции выражаются схемами: I2 + Cl2 + Н2О НIO3 + HCl FeCO3 + KMnO4 + H2SO4 → Fe2(SO4)3 + CO2 + MnSO4 +K2SO4+H2O.
- Определите степень окисления элемента в оксидах, назовите их в соответствии с международной номенклатурой, соответствующих данным оксидам 34. СО2
- Глутаминовая кислота (ФС42-0229-07), с.76 1.
- Константы нестойкости комплексных ионов [Co(NH3)6] 3+ , [Fe(CN)6] 4 — , [Fe(CN)6] 3- соответственно равны 6,2 ∙ 10-36 , 1,0 ∙ 10-37 , 1,0 ∙ 10-44
- Дать характеристику атома элемента с указанным номером в периодической системе: указать состав ядра атома, строение электронной оболочки в виде электронной и электроннографической формулы; указать валентные электроны, возможные степени окисления данного элемента, электронное семейство, высший оксид и гидроксид; доказать с помощью химических реакций свойства оксидов и гидроксидов. Порядковый номер элемента: 12.
- Определите степень окисления элемента в оксидах, назовите их в соответствии с международной номенклатурой, соответствующих данным оксидам. 19 – SrO.
- Напишите все возможные реакции получения следующих соединений: гидроксид меди (II), гидроксид цинка, гидроксид магния, гидроксид алюминия. Какие из них растворимы в щелочах? Приведите эти реакции в молекулярном и ионном виде.
- Напишите выражение для константы равновесия гомогенной системы 2SO2 + O2 = 2SO3. Как изменится скорость прямой реакции – образования серного ангидрида, если увеличить концентрацию SO2 в 3 раза?
