| 🎓 Заказ №: 22214 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
а) Cu +HNO3 (конц.) → б) H2S +Cl2 + H2O → H2SO4 + HCl в) KMnO4 + HCl → MnCl2 + Cl2 + KCl + H2O
Решение: а) Cu HNO3 Cu(NO3 ) 2 NO2 H2O В ходе данной окислительно-восстановительной реакции степень окисления меди повышается от 0 до +2, степень окисления части азота понижается от +5 до +4. 0 2 2 Cu e Cu 1 окисление Cu – восстановитель 5 4 N e N 2 восстановление HNO3 – окислитель Cu 2HNO3 Cu(NO3 ) 2 2NO2 H2O 2 молекулы HNO3 восстанавливаются до 2 молекул NO2. Ещё 2 молекулы HNO3 необходимы для образования 1 молекулы Cu(NO3)2. Для уравнивания увеличиваем коэффициент перед формулой HNO3 в левой части до 4. Cu 4HNO3 Cu(NO3 ) 2 2NO2 H2O Теперь в левой части 4 атома водорода и 12 атомов кислорода. В правой части 2 атома водорода и 11 атомов кислорода. Для окончательного уравнивания ставим перед формулой H2O в правой части коэффициент 2. Cu 4HNO3(конц) Cu(NO3 )2 2NO2 2H2O
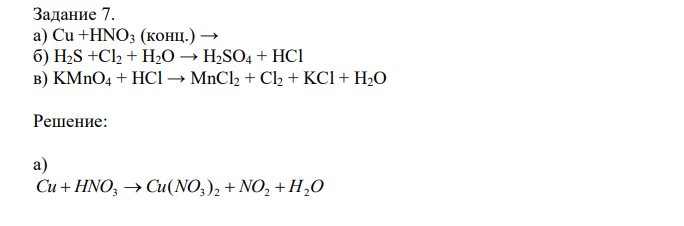

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Найти молярность, нормальность и моляльность 15 %-го раствора H2SO4 (d=1,10 г/мл).
- Определите, какая соль: а) FeS; б) Ag2S; в) CdS растворяется в соляной кислоте.
- Осуществите химическое превращение в указанной последовательности.
- Какие орбитали атома заполняются раньше; 4d или 5s; 6s или 5p?
- Составьте молекулярные и ионно-молекулярные уравнения реакций, протекающих при смешивании растворов: а) гидросульфата калия и гидрок-сида калия, б) нитрата свинца (II) и гидроксида натрия.
- Вывести уравнение для расчета константы гидролиза Na2S; CoCl2.
- Вычислить произведение растворимости селенита цинка, если в 200 мл воды растворяется 1,95∙10-2 г ZnSeO3.
- Смешивают попарно растворы: а) Cu(NO3)2 и Na2SO4; б) BaCl2 и K2SO4; в) NaHCO3 и NaOH; г) Cu(OH)2 и HCl
- Резьбовое крепежное изделие из инструментальной стали (основа – железо), содержащей кобальт и медь, покрыто цинком.
- Рассчитать: 1. молярную концентрацию, 2. молярную концентрацию эквивалента, 3. моляльную концентрацию 4. титр указанного раствора по данным, приведенным в таблице.
