| 🎓 Заказ №: 22181 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Дайте заключение о качестве раствора рибофлавина 0,02 % — 100 мл по количественному содержанию согласно приказу № 305, если при фотометрическом определении навеску 0,5 мл разбавили водой до 10 мл и получи-ли оптическую плотность A = 0,250. Оптическая плотность приготовлен-ного по той же методике стандартного раствора A0 = 0,255.
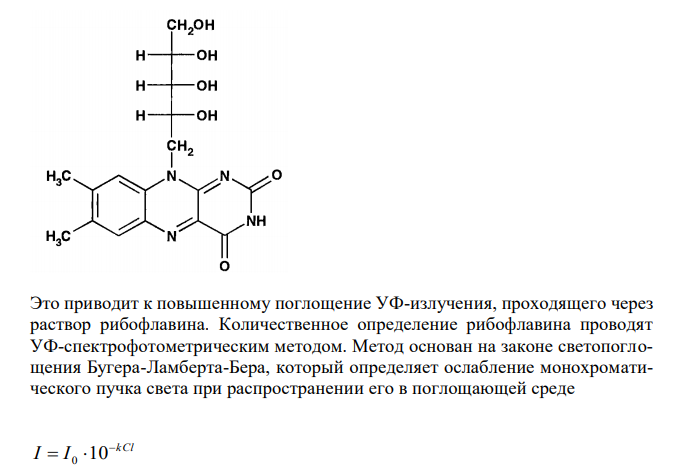
Решение: Молекула рибофлавина содержит один из особых структурных фрагментов (так называемых хромофоров) – азадиеновую группировку с двумя сопряженными двойными связами (в изоаллоксазиновом ядре). 66 Это приводит к повышенному поглощение УФ-излучения, проходящего через раствор рибофлавина. Количественное определение рибофлавина проводят УФ-спектрофотометрическим методом. Метод основан на законе светопоглощения Бугера-Ламберта-Бера, который определяет ослабление монохроматического пучка света при распространении его в поглощающей среде kCl I I 0 10 где: I – интенсивность выходящего пучка, I0 – интенсивность входящего пучка, l – толщина слоя вещества, через которое проходит свет, k – показатель поглощения После логарифмирования kCl I I 0 lg Отношение I I 0 lg обозначается A и называется оптической плотностью раствора. Выражение A kCl отражает прямо пропорциональную зависимость оптической плотности от концентрации и толщины слоя раствора определяемого вещества. Вычисляем прописанное количество вещества


| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Составьте схемы электролиза растворов веществ (на угольных анодах): HCl; Cr(NO3)2.
- Рассчитайте массу азота объемом 30 л при нормальных условиях?
- Назовите полимеры, полученные на основе полиэтилена
- Оксид азота (II), необходимый для производства азотной кислоты и азотных удобрений, заманчиво получать из азота и кислорода воздуха по реакции: N2(г) + O2(г) = 2NO(г).
- Садоводы и огородники борются с грибковыми заболеваниями растений с помощью медного купороса, готовят его 0,5 %-ный раствор для опрыскивания грядок
- В реакции А + Б ↔ Д + Е после установления равновесия концентрация [А] увеличилась в 2 раза, а [Д] – в 4 раза
- Семена древесных пород (сосна, ель, ясень) протравливают раствором, массовая доля CH3COOH в котором 0,5 %
- Используя метод МО, объяснить, почему ионизационные потенциалы атомов кислорода (13,6 эВ) и фтора (17,4 эВ) выше, чем молекул O2 (12,2 эВ) и F2 (15,8 эВ)?
- Для атома фосфора: а) написать полную электронную формулу
- Какое состояние системы называют химическим равновесием ?
