| 🎓 Заказ №: 22210 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
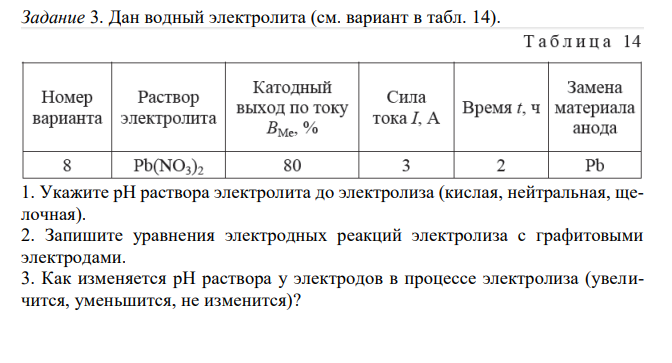
1. Укажите рН раствора электролита до электролиза (кислая, нейтральная, щелочная). 2. Запишите уравнения электродных реакций электролиза с графитовыми электродами. 3. Как изменяется рН раствора у электродов в процессе электролиза (увеличится, уменьшится, не изменится)? 4. Рассчитайте, сколько и каких веществ выделится на электродах при электролизе при заданных условиях (см. табл.14). Анодный выход по току во всех случаях равен 100 %. 5. Как изменится анодный процесс, если анод заменить на другой металл, указанный в таблице? Запишите соответствующие электродные реакции.
Решение: 1. Нитрат свинца Pb(NO3)2 образован слабым основанием и сильной кислотой. В водном растворе происходит гидролиз нитрата свинца благодаря катионам 2 Pb , связывающим гидроксид-анионы. В обычных условиях гидролиз ограничивается первой стадией (ступенью). Ионно-молекулярное уравнение гидролиза Pb H2O PbOH H 2 Молекулярное уравнение гидролиза 3 2 2 3 3 Pb(NO ) H O Pb(OH)NO HNO Избыток катионов водорода обусловливает кислую реакцию среды, рН < 7.

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Для той из реакций, которая является гетерогенной, записать кинетическое уравнение и вычислить, во сколько раз изменится скорость прямой реакции Na2CO3(к) + СO2(г) + H2O(г) ↔ 2NaHCO3(г)
- Изобразите графические (структурные) формулы следующих соединений. Гидроксид меди (II).
- Допишите уравнение реакции, составив к ней электронно-ионную схему (значения электродных потенциалов в табл. П.7, П.8).
- Как изменится скорость химической реакции при нагревании от 20ºС до 60º, если температурный коэффициент скорости реакции равен 4?
- Разложение нитрата аммония при нагревании возможно по двум направлениям: NH4NO3 (к) = N2O (г) + 2H2O(г)
- Вычислите эквивалентную массу железа в оксидах FeO, Fe3O4, Fe2O3
- После смешивания газов А и В в системе A + B ↔ C + D устанавливается равновесие при следующих концентрациях: [B] = 0,05 моль/л
- Как изменятся скорости прямой и обратной реакций в системе: 2NO(г) + O2(г) ↔ 2NO2(г), если увеличить давление в 5 раз.
- Рассчитайте давление в сосуде объемом 20 л, содержащем 8 г кислорода и 22 г оксида углерода (IV) при 398 К.
- Определить изменение энтальпии, энтропии и принципиальную возможность протекания реакций при стандартных условиях: N2O3 + 2H2O (г.) = NH4NO3 (кр.) + O2 (г.) Fe2O3 (кр.) + 3С (графит) = 2Fe (кр.) + 3CO2 (г.)
