| 🎓 Заказ №: 22177 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Приведите способы получения фенола. Какие из них могут быть использованы в промышленности и почему? Какие из них протекают по механизму нуклеофильного замещения? Разберите этот механизм (SN).
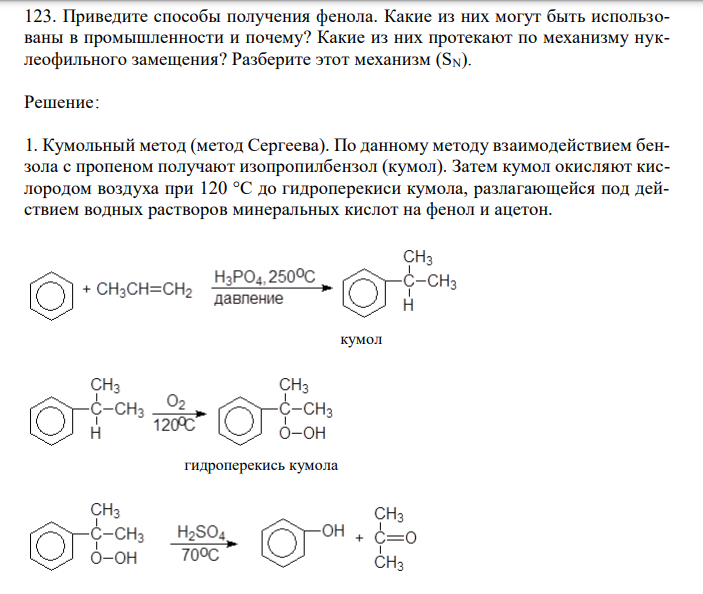
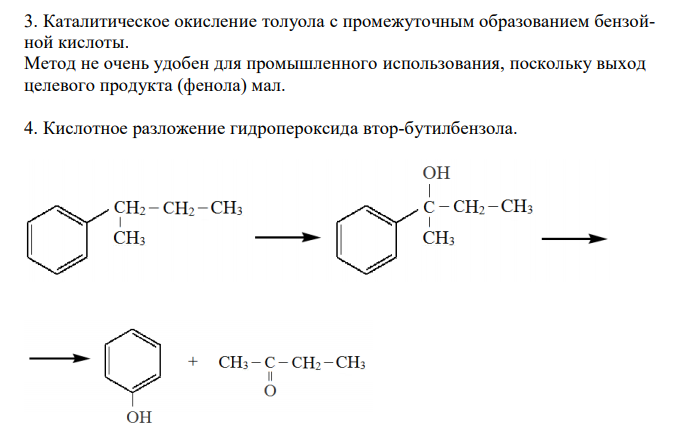
Решение: 1. Кумольный метод (метод Сергеева). По данному методу взаимодействием бензола с пропеном получают изопропилбензол (кумол). Затем кумол окисляют кислородом воздуха при 120 °С до гидроперекиси кумола, разлагающейся под действием водных растворов минеральных кислот на фенол и ацетон. кумол гидроперекись кумола Данный метод наиболее удобен для промышленного получения бензола, поскольку используется достаточно дешёвое и доступное сырьё (бензол, пропен, воздух). Кроме того, уровень селективности при данном процессе около 97 %. 2. Прямое окисление бензола закисью азота. C6H6 N2O C6H5OH N2 Метод очень перспективен для промышленности. Используется оксид азота (I), что очень сильно удешевляет процесс и позволяет частично решить проблему утилизации отходов адипинового производства. 3. Каталитическое окисление толуола с промежуточным образованием бензойной кислоты. Метод не очень удобен для промышленного использования, поскольку выход целевого продукта (фенола) мал. 4. Кислотное разложение гидропероксида втор-бутилбензола.

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Бак автомашины наполнен бензином из смеси 80 % гептановых и 20 % октановых изомеров
- Вычислите константу равновесия для гомогенной системы СО(г) + Н2О (г) ↔ СО2(г) + Н2(г) если равновесные концентрации реагирующих веществ: [CO] = 0,004 моль/л; [Н2О] = 0,064 моль/л; [CO2] = 0,016 моль/л; [Н2] = 0,016 моль/л.
- Дайте заключение о качестве анальгина по количественному определению с учетом требований ГФ XII, ФС 42-0215-07 (должно быть анальгина не менее 99,0 % в пересчете на сухое вещество), если на навеску, равную 0,1498 г израсходовалось 8,45 мл 0,05 М раствора йода с К=1,0036.
- Составьте по три молекулярных уравнения реакций, которые выражаются ионно-молекулярными уравнениями: а) Fe S FeS 2 2 б) 2 3 2 SiO3 2H H SiO
- В 250 мл раствора содержится 0,02 моль экв. хлорида алюминия.
- Определить какую массу раствора гидроксида натрия нормальной концентрацией 2,5 моль-экв/дм3 (ρ = 1,23 гсм3 ) можно получить при растворении 95 г щелочи в воде.
- Навеска КCl 1,4960 г растворена в мерной колбе на 200 см3
- Напишите структурную формулу двухатомного спирта состава С5Н10(ОН)2, содержащего три метильные группы.
- Какую смесь называют «царской водкой»?
- Стеарат натрия (мыло) применяют в качестве поверхностно-активного вещества
