| 🎓 Заказ №: 22203 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Четыре моля гидроксида кобальта (3) растворили в серной кислоте. Какое соединение кобальта и в каком количестве образовалось?
Решение: Записываем уравнение реакции 4Co(OH) 3 2H2 SO4 4CoSO4 O2 10H2O

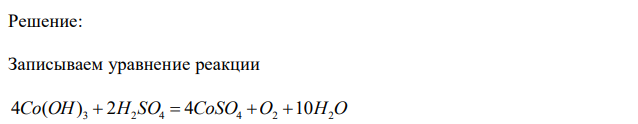
| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Во сколько раз возрастет скорость реакции при увеличении температуры от 20 до 100 °С, если энергия активации равна 125 кДж/моль ?
- Вычислите температуру кипения 5 %-ного раствора нафталина С10H8 в бензоле.
- Продуктом коррозии является гидроксид олова (II) Sn(OH)2.
- При какой концентрации ионов Cu2+ (в моль/л) значение потенциала медного электрода становится равным стандартному потенциалу водородного электрода?
- Используя таблицу генетического кода напишите буквенную последовательность мРНК и комплементарный ей фрагмент ДНК, кодирующий первичную структуру полипептида состава ала-тре-лиз-асп-сер
- Кратко охарактеризуйте роль биохимических методов в стандартизации и контроле качества лекарств, биотехнологии лекарственных препаратов и технологии лекарственных форм.
- Для алканов наиболее типична реакция 1 присоединения 2 замещения 3 полимеризации 4 гидратаци
- Назовите буферные системы крови и приведите примеры их участия в регуляции кислотно-щелочного равновесия.
- Дана реакция СН4(г) Н2О(г) СО(г) 3Н2(г) , Н 206 кДж .
- Гидрохлорирование бутадиена (все возможные случаи).
