Пример №1-18.
Образец органического вещества массой 8,7 г сожгли в избытке кислорода. Продуктами реакции являются оксид углерода (IV) объемом 10,08 л (н. у.) и вода массой 8,1 г. Плотность паров исходного вещества по гелию равна 14,5. Определите формулу вещества, если известно, что анализируемое вещество не обесцвечивает раствор брома в четырех хлористом углероде и не взаимодействует с аммиачным раствором оксида серебра.
Решение:
Состав продуктов реакции 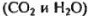 позволяет утверждать, что в состав неизвестного вещества входят углерод и водород, а также, вероятно, кислород. Для окончательного решения вопроса о качественном составе неизвестного вещества определим сначала количества углерода и водорода, входящие его состав.
позволяет утверждать, что в состав неизвестного вещества входят углерод и водород, а также, вероятно, кислород. Для окончательного решения вопроса о качественном составе неизвестного вещества определим сначала количества углерода и водорода, входящие его состав.
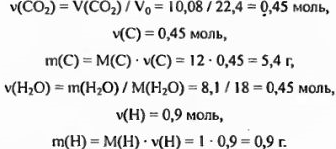
Суммируя массы углерода и водорода, получаем:
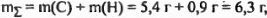
что не равно массе исходного образца. Следовательно, в состав неизвестного вещества входят не только углерод и водород, но и кислород, масса которого составляет
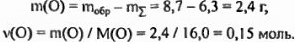
Теперь перейдем непосредственно к установлению формулы неизвестного вещества. Из проведенных расчетов видно, что молярное соотношение компонентов в искомом соединении ровно:
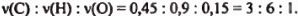
Очевидно, что полученному соотношению компонентов отвечает формула  , а учитывая свойства этого вещества, приведенные в условии задачи, можно утверждать, что неизвестное органическое вещество — ацетон.
, а учитывая свойства этого вещества, приведенные в условии задачи, можно утверждать, что неизвестное органическое вещество — ацетон.
Этот пример взят со страницы решения задач по химии с примерами:
Возможно эти примеры вам будут полезны:

