| 🎓 Заказ №: 22216 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Установите термодинамическую вероятность протекания электрохимической коррозии на поверхности стального изделия с магниевым протектором в нейтральной водной среде, содержащей растворенные соли (NaCl, Na2SO4) в присутствии растворенного кислорода. Запишите схему коррозионной гальванопары, уравнения анодного и катодного процессов. Укажите вид и состав конечного продукта коррозии.
Решение: Сталь – сплав, основой которого является железо. Стандартные электродные потенциалы железа и магния имеют следующие значения B Fe Fe 0,440 / 2 B Mg Mg 2,363 / 2 Поскольку Mg / Mg Fe / Fe 2 2 , то магний является анодом и подвергается окислению, железо является катодом. Схема данной коррозионной гальванопары A()Mg H2O O2 Fe()K Уравнения анодного и катодного процессов 2 A: Mg 2e Mg K : O2 2H2O 4e 4OH Общее уравнение реакции 2Mg O2 2H2O 2Mg(OH) 2 Состав конечного продукта коррозии – гидроксид магния 2 Mg(OH) в виде белой рыхлой аморфной массы.


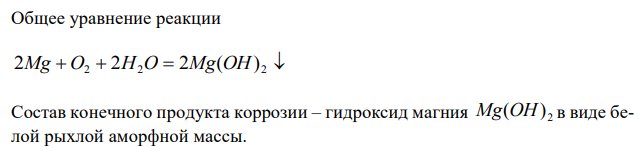
| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Как изменится скорость прямой и обратной реакции в системе СО(г) + 3Н2(г) ↔ СН4(г) + H2O(г), если концентрации исходных веществ и продуктов реакции уменьшить в 2 раза? В каком направлении сместится равновесие?
- Высокомолекулярные соединения, из которых получают лавсан – это: а) полиэтилен; б) полиуретан; в) полиэфир; г) полистирол.
- Константа равновесия реакции N2(г) 3H2(г) 2NH3(г) равна 0,1.
- Водный раствор, содержащий смесь нитратов серебра, калия, цинка с одинаковыми концентрациями, подвергли электролизу. Укажите значение молярной массы вещества, которое будет восстанавливаться на катоде в первую очередь.
- Какова массовая доля фруктозы С6H12O6 в водном растворе, который замерзает при -0,524 °С?
- Составьте молекулярные и ионные уравнения гидролиза солей Al2(SO4)3, KF, KI. Какое значение pH (pH > 7, pH < 7) имеют растворы этих солей?
- Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в водных растворах между веществами. а) NaHS и HCl; б) HCl и K2S; в) KH2PO4 и HNO3
- Напишите уравнения реакций, при помощи которых можно осуществить следующие превращения: Sn → SnCl2 → Sn(OH)2 → Sn(NO3)2 → SnOHNO3.
- Какое количество электричества потребуется для выделения из раствора серной кислоты 20 г водорода.
- Составьте электронную формулу атома аргона. Приведите по два катиона и аниона с такой же электронной формулой.
