| 🎓 Заказ №: 22218 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Составьте ионные и молекулярные уравнения гидролиза солей CuCl2, Сs2СО3. Какое значение рН имеют растворы этих солей?
Решение: Гидролизом называется обменная реакция вещества с водой. При этом происходит смещение равновесия диссоциации воды H2O H OH вследствие связывания одного из ионов (или обоих) с образованием мало-диссоциирующего или труднорастворимого вещества. Гидролизу подвер-гаются соли, образованные либо слабой кислотой, либо слабым основанием, либо и тем и другим. Хлорид меди (II) CuCl2 образован слабым основанием и сильной кислотой. Гидролиз хлорида меди (II) происходит благодаря ионам Cu2+, связывающим гидроксид-ионы. Записываем ионные и молекулярные уравнения гидролиза данной соли по ступеням. I ступень Cu H2O CuOH H 2 CuCl H O CuOHCl HCl


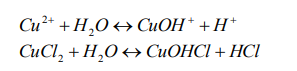
| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Какой объем 60 %-го раствора карбоната натрия (пл.1,25 г/см3) требуется для приготовления 2 л 12 %-го раствора (пл. 1,12 г/см3)?
- Образуется ли осадок при смешении равных объемов Ni(NO3)2 и NaOH с одинаковыми молярными концентрациями 0,002 моль/дм3 .
- Какие из указанных металлов Fe, Au, Zn могут быть использованы для протекторной защиты детали из Cu?
- Объясните, какие соли гидролизуются по аниону
- Объясните, исходя из электронного строения атомов, каков физический смысл номера периода и номера группы
- 2,14 г металла вытесняет из кислоты 2 л водорода. Вычислить молярную массу эквивалента металла.
- Составьте молекулярные и ионные уравнения реакций взаимодействия в растворах между a) CuSO4 и H2S; б) ВаСО3 и HNO3; в) FeCl3 и КОН.
- Уравняйте методом электронного баланса, укажите окислитель, восстановитель и тип ОВР
- Во сколько раз изменится скорость обратной реакции, если концентрацию NH3 увеличить в 2 раза?
- При полном сгорании этилена выделилось 3113 кДж.
