| 🎓 Заказ №: 22205 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Реакции выражаются приведёнными схемами: K2S + KMnO4 + H2SO4 = S + K2SO4 + MnSO4 + H2O HNO3 + Ca = NH4NO3 + Ca(NO3)2 + H2O Составьте электронные уравнения. Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, какое – восстановителем; какое вещество окисляется, какое – восстанавливается.
Решение: K S K MnO H SO S K SO MnSO4 H2O 2 2 4 0 4 2 4 2 7 2 В ходе данной окислительно-восстановительной реакции степень окисления серы, входящей в сульфид калия, повышается от -2 до 0. Степень окисления марганца понижается от +7 до +2. 2 0 S 2e S 5 окисление K2S – восстановитель 7 2 5 Mn e Mn 2 восстановление KMnO4 – окислитель 5K2 S 2KMnO4 H2 SO4 5S K2 SO4 2MnSO4 H2O В левой части 12 атомов калия, в правой части 2 атома калия. Для уравнивания ставим перед формулой K2SO4 коэффициент 6. 5K2 S 2KMnO4 H2 SO4 5S 6K2 SO4 2MnSO4 H2O
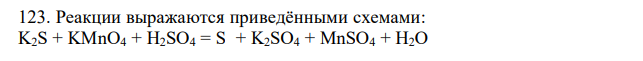

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Какое значение рН (больше или меньше 7) имеют растворы солей: CH3COOK, ZnSO4, Al(NO3)3.
- Перечислите факторы устойчивости коллоидных систем.
- В объеме воды V(H2O) растворили массу вещества m.
- Определите карбонатную жесткость воды, в одном литре которой содержится по 100 мг Ca(HCO3)2, Mg(HCO3)2, Fe(HCO3)2
- Какова временная жесткость воды, в литре которой содержится 0,146 г гидрокарбоната магния?
- Zn => ZnSO4 =>Zn(HSO4)2 => ZnCO3 =>CO2
- Для предотвращения образования накипи проводят допарогенераторную обработку воды
- В случае совместного присутствия в растворе бромид — и иодид — ионов, в какой последовательности они окислятся хлорной водой?
- Соленость морской воды определяют по содержанию хлорид-ионов, осаждая их раствором нитрата серебра AgNO3: Ag+ + Cl- = AgCl↓
- При взаимодействии серы с 6,72 л кислорода образовалось 4,48 л оксида.
