| 🎓 Заказ №: 22225 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Перечислите известные виды катализа. В чем состоят особенности каталитических процессов?
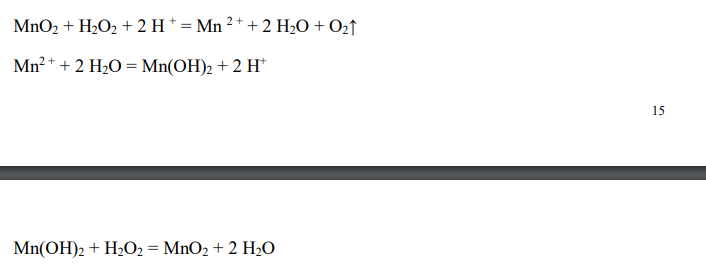
Решение. Катализ — процесс, заключающийся в изменении скорости химических реакций в присутствии веществ, называемых катализаторами. Катализатор изменяет механизм реакции на энергетически более выгодный – снижает энергию активации. В ходе реакции катализатор образует с молекулой одного из реагентов промежуточное соединение, в котором ослаблены химические связи. Это облегчает его реакцию со вторым реагентом. Причем, катализаторы ускоряют обратимые реакции, как в прямом, так и в обратном направлениях. После каждого цикла промежуточных взаимодействий катализаторы восстанавливают свой химический состав, то есть, не расходуются в процессе реакции. Положительным называют катализ, при котором скорость реакции возрастает, отрицательным (ингибированием) — при котором она убывает. Примером положительного катализа может служить процесс окисления аммиака на платине при получении азотной кислоты. Примером отрицательного — снижение скорости коррозии при введении в жидкость, в которой эксплуатируется металл, нитрита натрия, хромата и дихромата калия. В зависимости от того, находится катализатор в той же фазе, что и реагирующие вещества, или образует самостоятельную фазу, говорят о гомогенном или гетерогенном катализе. Примером гомогенного катализа является разложение пероксида водорода в присутствии оксида марганца (IV). Реакция протекает через следующие стадии: MnO2 + H2O2 + 2 H + = Mn 2 + + 2 H2O + O2↑ Mn2 + + 2 H2O = Mn(OH)2 + 2 H+ 16 Mn(OH)2 + H2O2 = MnO2 + 2 H2O

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Напишите структурную формулу простейшей непредельной одноосновной кислоты и уравнение реакции взаимодействия этой кислоты с метиловым спиртом.
- При изучении кинетики реакции A + 2B + 2D = F было обнаружено, что скорость реакции (вдали от состояния равновесия) при увеличении концентрации вещества А в 2 раза возрастает в 4 раза, не зависит от концентрации вещества В и возрастает в 3 раза при увеличении концентрации вещества D в 3 раза.
- ЭДС гальванического элемента, состоящего из свинцового электрода, погруженного 0,1 M раствор соли Pb(NO3)2 и железного электрода, погруженного в 1M раствор соли Fe(NO3)2 составляет:___
- Определите класс и назовите соединения: Ba(HS), HSCN, Na2ZnO2, (FeOH)2SO4, Cl2O5, H2Se, Sn(OH)2, NaOH, Fe2O3, KClO3.
- Имеется раствор соли (см. вариант в табл. 7). 328 1. Напишите ионно-молекулярное и молекулярное уравнения реакции гидролиза и выражение для константы гидролиза данной соли по первой ступени (Kг1).
- При некоторой температуре равновесие гомогенной системы 2NO + O2 = 2NO2 установилось при следующих концентрациях реагирующих веществ: [NO] = 0,2 л моль ; [О2] = 0,1 л моль ; [NO2] = 0,1 л моль.
- Дана схема реакции: I 2 HNO3 HIO3 NO H2O 1) определите степень окисления атомов элементов, меняющих ее в процессе реакции;
- Почему диоксид азота способен к реакциям самоокисления – самовосстановления (диспропорционирования)?
- Напишите качественные реакции на альдегидную группу на примере: 3-метилгексаналя
- На титрование 5 мл раствора кислоты пошло 10 мл раствора щелочи с концентрацией 0,5 н.
