| 🎓 Заказ №: 22193 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
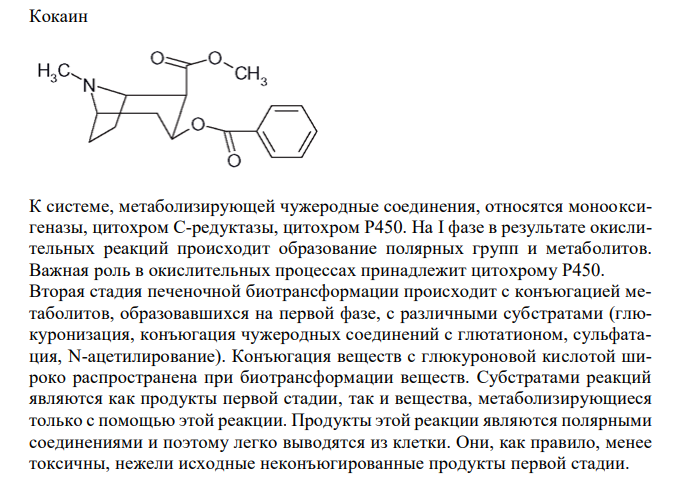
Отразите основные пути метаболизма кокаина. Поясните стадии метаболизма.
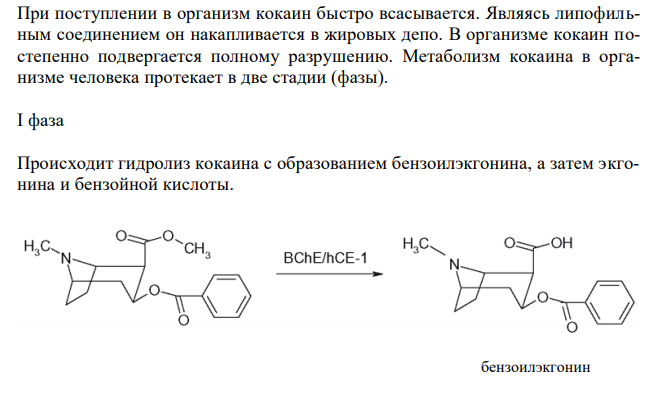
Решение: Кокаин К системе, метаболизирующей чужеродные соединения, относятся монооксигеназы, цитохром С-редуктазы, цитохром Р450. На I фазе в результате окислительных реакций происходит образование полярных групп и метаболитов. Важная роль в окислительных процессах принадлежит цитохрому Р450. Вторая стадия печеночной биотрансформации происходит с конъюгацией метаболитов, образовавшихся на первой фазе, с различными субстратами (глюкуронизация, конъюгация чужеродных соединений с глютатионом, сульфатация, N-ацетилирование). Конъюгация веществ с глюкуроновой кислотой широко распространена при биотрансформации веществ. Субстратами реакций являются как продукты первой стадии, так и вещества, метаболизирующиеся только с помощью этой реакции. Продукты этой реакции являются полярными соединениями и поэтому легко выводятся из клетки. Они, как правило, менее токсичны, нежели исходные неконъюгированные продукты первой стадии. При поступлении в организм кокаин быстро всасывается. Являясь липофильным соединением он накапливается в жировых депо. В организме кокаин постепенно подвергается полному разрушению. Метаболизм кокаина в организме человека протекает в две стадии (фазы). I фаза Происходит гидролиз кокаина с образованием бензоилэкгонина, а затем экгонина и бензойной кислоты.

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Реакция идет по уравнению 2NO + O2 ⇄ 2NO2. Концентрации исходных веществ до начала реакции были: С0(NO)=0,049 моль/л; С0(O2)=0,01 моль/л. Вычислите концентрацию этих веществ в момент, когда концентрация NO2 стала равной 0,005 моль/л.
- Какие из солей, формулы которых приведены, подвергаются гидролизу: Na2SiO3, Ca(NO2)2, KCl?
- Реакция идет по уравнению 2NO+O2=2NO2. Концентрация исходных веществ: [NO]=0,02 моль/дм3 ; [O2]=0,03 моль/дм3 . Как изменится скорость прямой реакции, если увеличить концентрацию O2 до 0,10 моль/дм3 и концентрацию NO до 0,05 моль/дм3 ?
- Приведите классификацию галогенопроизводные УВ.
- Напишите уравнения реакций, при помощи которых можно осуществить следующие превращения: C2H4→C2H6→C2H5Cl→C2H5OH→CH3COOCH3
- Дайте обоснование испытанию сульфадимидина по показателю «Цветность раствора» в соответствии с требованиями ФС.2.1.0181.18 (Приложения № 3, 6).
- Температурный коэффициент скорости некоторой реакции равен 2. Во сколько раз увеличится скорость этой реакции, если повысить температуру на 40 °С ?
- Рассчитайте степень ионизации А в водном растворе с концентрацией В моль/л и рН данного раствора. Коэффициенты активности ионов примите равными 1,00. № А В 1.1. сероводородной кислоты 0,100
- Приведите расчет интервала навески соли (М.м. калия йодида 160,00) исходя из чувствительности иона (И.м. иона калия 39,10) для доказательства подлинности калия йодида по катиону калия по методике А (Приложение № 2).
- Одно и то же количество металла соединяется с 0,2 г кислорода и с 3,17 г одного из галогенов.
