| 🎓 Заказ №: 22196 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
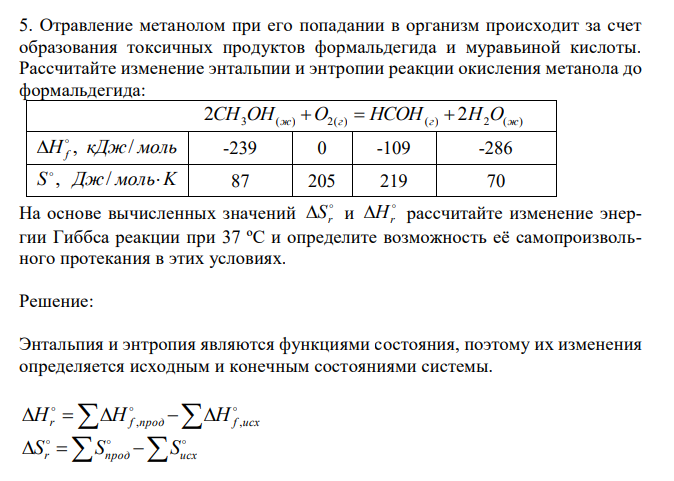
Отравление метанолом при его попадании в организм происходит за счет образования токсичных продуктов формальдегида и муравьиной кислоты. Рассчитайте изменение энтальпии и энтропии реакции окисления метанола до формальдегида: 2CH3OH(ж) O2(г) HCOH(г) 2H2O(ж) H кДж моль f , / -239 0 -109 -286 S , Дж/ мольK 87 205 219 70 На основе вычисленных значений r S и Hr рассчитайте изменение энергии Гиббса реакции при 37 ºС и определите возможность её самопроизвольного протекания в этих условиях.
Решение: Энтальпия и энтропия являются функциями состояния, поэтому их изменения определяется исходным и конечным состояниями системы. Hr H f ,прод H f ,исх Sr Sпрод Sисх Вычисляем изменение энтальпии и изменение энтропии данной реакции, используя табличные значения изменений энтальпий и абсолютных энтропий веществ.

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Над раствором, содержащим 5,59 г неэлектролита и 180 г воды, при 80ºС давление насыщенного пара воды составляло 47,3 кПа, а давление насыщенного пара над этим раствором – 47,2 кПа.
- В организме в процессе метаболизма образуется глицерин, который далее окисляется.
- Рассчитайте изменение энтальпии реакции гидролиза сахарозы C12H22O11 : (водн) 2 (ж) (водн) фруктоза(водн) сахароза H O глюкоза H кДж моль f , / -2215 -286 -1275 -1266
- У какого из p-элементов V группы периодической системы – фосфора или сурьмы – сильнее выражены неметаллические свойства?
- Рассчитайте рН раствора, полученного смешиванием равных объемов A и B.
- С помощью метода валентных связей опишите молекулу Н2О.
- Напишите формулы солей: сульфит хрома (II), cульфид железа(II), гидросульфид кальция, гидрокарбонат железа (III), гидроортофосфат бария, гидроортофосфат кальция.
- Выявить, какое вещество является окислителем, а какое восстановителем, составить уравнения электронного баланса и расставить коэффициенты в приведенных ниже уравнениях окислительно-восстановительных реакций. а) Mg + HNO3 → Mg(NO3)2 + N2 + H2O б) Fe + Ni2O3 + H2O → Fe(OH)3 + Ni(OH)2.
- Напишите уравнение реакции, характерной для катиона бария, укажите её аналитические признаки.
- Через раствор, содержащий 350 г азотной кислоты, пропустили 112 л (н.у.) аммиака. Какова масса образовавшейся соли?
