| 🎓 Заказ №: 22228 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Определение состава неизвестных смесей по диаграмме плавкости. Приведите 2-3 примера.
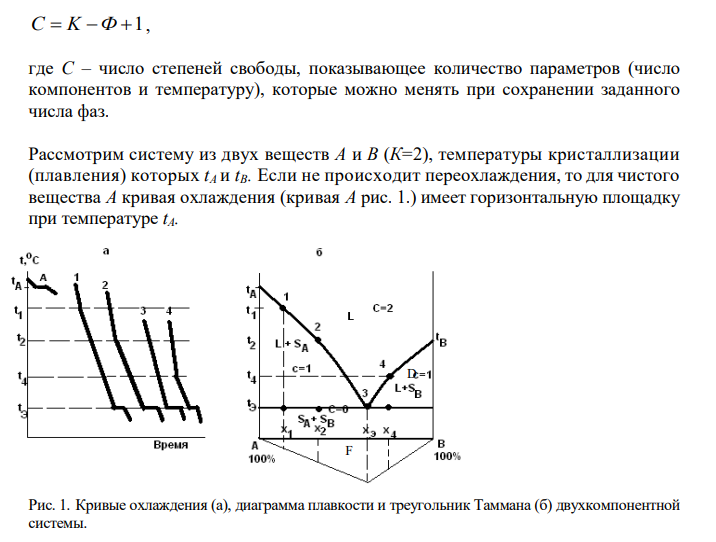
Решение: Диаграмма плавкости – фазовая диаграмма, которая выражает зависимость температуры плавления системы от ее состава. Диаграмма плавкости («температура–состав») строится на основании кривых охлаждения. Кривые охлаждения – графическое изображение зависимости температуры от времени для исходных чистых веществ A и B и их смесей различного состава. Вид этих кривых свидетельствует о наличии или отсутствии фазовых превращений при некоторых определенных температурах или в интервале температур. Знание диаграмм плавкости используется в фармацевтическом анализе для идентификации и определения чистоты лекарственных препаратов, выбора наиболее оптимальных путей их выделения из смесей, определения состава смесей для решения вопроса о совместимости лекарственных препаратов. Число компонентов К и число фаз в системе Ф связаны правилом фаз Гиббса, которое при постоянном давлении выражается уравнением: 232 С K Ф 1, где С – число степеней свободы, показывающее количество параметров (число компонентов и температуру), которые можно менять при сохранении заданного числа фаз. Рассмотрим систему из двух веществ А и В (К=2), температуры кристаллизации (плавления) которых tА и tВ. Если не происходит переохлаждения, то для чистого вещества А кривая охлаждения (кривая А рис. 1.) имеет горизонтальную площадку при температуре tА. D F Рис. 1. Кривые охлаждения (а), диаграмма плавкости и треугольник Таммана (б) двухкомпонентной системы. Для смеси А и В состава x1 температура начала кристаллизации вещества А t1 ниже температуры ta.На кривой охлаждения (рис. 1.) системы состава x1 началу кристаллизации вещества А соответствует излом при температуре t1. В процессе кристаллизации компонента А его концентрация в жидкости уменьшается, а концентрация В увеличивается, что и приводит к постепенному понижению температуры кристаллизации А вплоть до tЭ. По правилу фаз в ходе кристаллизации вещества А из раствора система, содержащая 2 компонентп и 2 фазы, имеет одну степень свободы (С=2-2+1=1), поэтому температура кристаллизации изменяется. Снижение скорости охлаждения системы при температурах ниже t1 связано с выделением в системе теплоты кристаллизации. При температуре tэ жидкий раствор становится насыщенным в отношении вещества В, которое при этих условиях также начинает кристаллизоваться. Система становится трехфазной (жидкость, кристаллы и кристаллы В), и число ее степеней свободы равно нулю (С=2-3+1=0). Таким образом, одновременная кристаллизация А и В из раствора происходит при постоянных температуре (tЭ) и составе жидкого раствора (xЭ).Эта температура называется эвтектической. На кривой охлаждения 1 (рис.1.) процессу одновременной кристаллизации А и В соответствует площадка при tЭ. Расплав, из которого одновременно выпадают кристаллы А и В, называется эвтектическим расплавом, образующаяся при этом смесь мелких кристаллов двух веществ


| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- При электролизе раствора нитрата серебра в течение 50 минут при силе тока 3 А на катоде выделилось 9,6 г серебра?
- В гомогенной газовой системе установилось равновесие. 2SO3 ⇄ 2SO2 + O2
- Объяснить, чем отличается коррозия сплава, состоящего из цинка и магния, в бензине, содержащем растворенный кислород и примеси серы, от коррозии этого же сплава в воде, содержащей растворенный кислород.
- Рассчитайте, сколько молекул электролита продиссоциирует из каждых 120 недиссоциированных молекул, если степень диссоциации составляет 95 %.
- Запишите уравнения реакций в молекулярной и ионных формах: a) NaOH + FeCl3 → b) CaCO3 + HNO3 → c) Mg(NO3)2 + KOH→ d) K2CO3 + BaCl2 → e) Na2S + HCl → f) AgNO3 + K3PO4 → g) Mg(NO3)2 + H2SO4 → h) Fe(OH)3 + HNO3 → i) CuO + HCl → j) Ba(NO3)2 + K2SO4 → k) ZnCl2 + KOH → l) K2CO3 + HNO3 →
- Степень диссоциации электролита равна 70 %.
- Определить рН раствора, полученного при смешении 20 мл 0,2 н.
- Какую окраску будет иметь метиловый оранжевый, который влили в раствор после окончания реакции между 1,5моль хлороводорода и 2 моль едкого кали?
- Закон Рауля для растворов электролитов.
- Запишите уравнения реакций в молекулярной и ионных формах между следующими веществами: а) сульфатом натрия и нитратом свинца; б) хлоридом магния и гидроксидом натрия; в) нитратом бария и сульфатом натрия; г) сульфитом калия и соляной кислотой.
