| 🎓 Заказ №: 22220 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
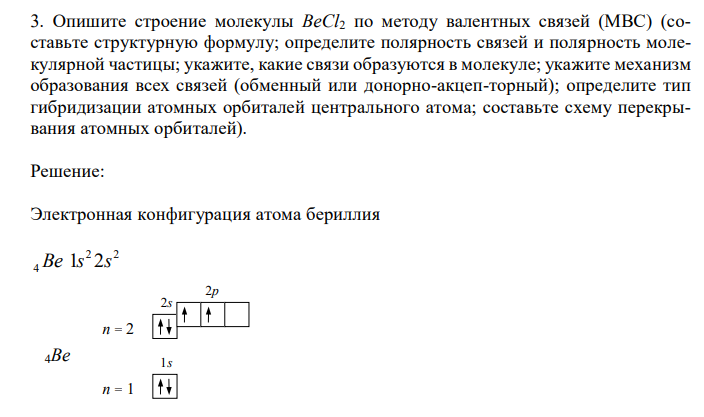
Опишите строение молекулы ВеСl2 по методу валентных связей (МВС).
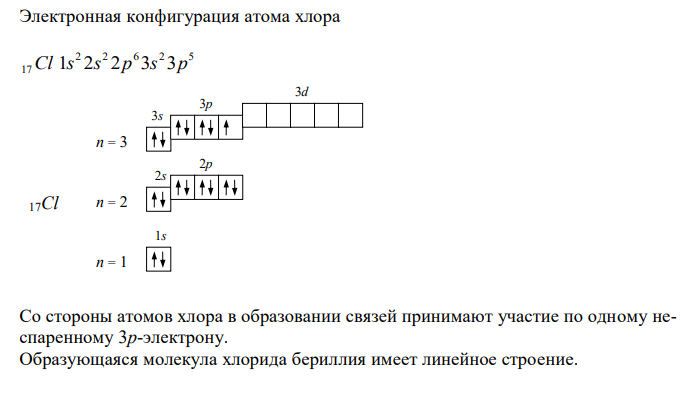
Решение: Электронная конфигурация атома бериллия 2 2 4 Be 1s 2s 4Be n = 2 n = 1 2s 2p 1s Перед образованием связей атом бериллия переходит в возбужденное состояние. Происходит распаривание пары 2s-электронов с переходом одного из электронов на вакантную 2p-орбиталь. Таким образом, у атома бериллия появляются два неспаренных электрона. 2 1 1 4 Be 1s 2s 2p Далее происходит процесс sp-гибридизации: электронные плотности s- и pорбиталей неспаренных электронов атома бериллия смешиваются (усредняются по энергии). В результате получаются две одинаковые гибридные sp-орбитали, расположенные в пространстве под углом 180º друг к другу. Электронная конфигурация атома хлора 2 2 6 2 5 17Cl 1s 2s 2p 3s 3p Со стороны атомов хлора в образовании связей принимают участие по одному неспаренному 3p-электрону. Образующаяся молекула хлорида бериллия имеет линейное строение.

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Написать выражение скорости реакции (по закону действующих масс), протекающих между азотом и водородом; определить, во сколько раз увеличится скорость реакции, если концентрация исходных веществ увеличится в 2 раза при стандартных условиях, написать выражение константы равновесия, определить направление смещения равновесия при увеличении давления.
- Подберите коэффициенты в уравнении реакции (по номеру варианта) двумя методами: ионно-электронным и балансовым. Укажите окислитель и восстановитель. K2MnО4 + Na2SО3 + H2О → MnО2 + Na2SО4 + KOH
- Какие объемы 40 %-ного раствора HNO3 (плотность 1,25 г/мл) и 10 %-но-го раствора этой же кислоты (плотность 1,06 г/мл) необходимо взять для при-готовления 2 л 15 %-ного раствора (плотность 1,08 г/мл)?
- Какие процессы протекают на электродах при электролизе сульфата никеля(II) (электроды никелевые)?
- К 500 мл раствора соляной кислоты (ρ = 1,1 г/мл) прибавили 2,5 л воды, и раствор стал 4 %-ный.
- Вычислите ЭДС гальванического элемента, составленного из стандартных электродов (железо и кобальт).
- Какой металл будет подвергаться коррозии, если заданная пара металлов (железо и кобальт), находящихся в контакте, попадет в кислую среду?
- Назовите и напишите графические формулы следующих оксидов: N2O5, P2O3, CaO, K2O, NO2.
- Напишите уравнения реакций солеобразования, доказывающие характер оксидов (кислотный, основной, амфотерный), указанных в разделе 1.2.
- Напишите электронно-графическую формулу атома элемента с порядковым номером 17.
