| 🎓 Заказ №: 22197 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
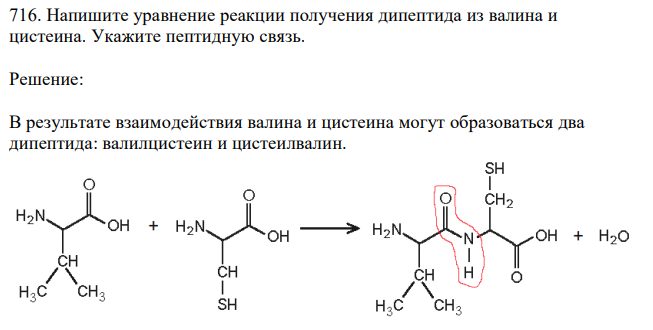
Напишите уравнение реакции получения дипептида из валина и цистеина. Укажите пептидную связь.
Решение: В результате взаимодействия валина и цистеина могут образоваться два дипептида: валилцистеин и цистеилвалин. валилцистеин
| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- При какой концентрации ионов Zn2+ (в г-ион/л) потенциал цинкового электрода будет на 0,015 В меньше его стандартного электродного потенциала
- Увеличится, уменьшится или останется без изменения масса цинковой пластинки при взаимодействии ее с растворами: a) CuSO4 b) MgSO4 c) Pb(NO3)2.
- Обменная емкость каолиновой глины составляет 13,5 ммоль/г
- Марганцевый электрод в растворе его соли имеет потенциал -1,23 В
- В окислительно-восстановительной реакции расставьте коэффициенты методом ионно-электронного баланса: MnO2 KI H2 SO4 MnSO4 I 2 K2 SO4 H2O
- Составьте уравнения процессов, происходящих на инертных электродах при электролизе раствора сульфата калия.
- На титрование 20,00 мл раствора карбоната натрия расходуется 23,45 мл раствора соляной кислоты с титром 0,003820 г/мл.
- Напишите выражения для констант нестойкости следующих комплексных ионов: [Ag(CN)2] — , [Ag(NH3)2] + , [Ag(SCN)2] — .
- Кадмий-никелевый аккумулятор имеет активную массу катода 0,8 кг
- Составьте схему, запишите электрохимические уравнения электродных процессов и рассчитайте ЭДС гальванического элемента, состоящего из пластин серебра и олова, опущенных в растворы своих солей с равновесными концентрациями потенциалопределяющих ионов [Ag+ ] = 1 моль/л, [Sn2+] = 0,25 моль/л.
