| 🎓 Заказ №: 22216 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Какие реакции называются окислительно-восстановительными? Для окислительно-восстановительных реакций составьте электронные уравнения, расставьте коэффициенты в уравнениях реакций. Укажите, какое вещество является окислителем, какое – восстановителем. Укажите процесс окисления и процесс восстановления. а) KI + KNO3 + H2SO4 → I2 + K2SO4 + NO + H2O б) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O в) Na2S + H2S → NaHS
Решение: Окислительно-восстановительными реакциями называются реакции, протекающие с изменением степеней окисления атомов, входящих в состав реагирующих веществ. При этом происходит перераспределение электронов между веществом-окислителем и веществом-восстановителем. В данном третья вторая реакция относится к реакциям обмена, остальные две реакции относятся к окислительно-восстановительным реакциям. а) K I KNO H SO I K SO N O H2O 2 2 4 0 2 4 2 5 3 1 В ходе данной окислительно-восстановительной реакции степень окисления йода повышается от -1 до 0, степень окисления азота понижается от +5 до +2.

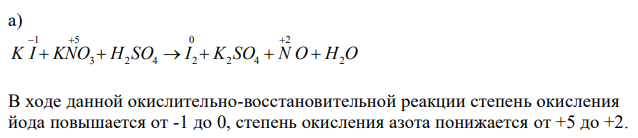
| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Правовые основы государственной политики в сфере оборота наркотических средств, психотропных веществ и в области противодействия их незаконному обороту в целях охраны здоровья граждан, государственной и общественной безопасности.
- Почему азотистая кислота может проявлять как окислительные, так и восстановительные свойства? На основании электронных уравнений составьте реакции HNO2: а) с бромной водой; б) c HI.
- Дайте обоснование фармакопейному методу количественного определения тетракаина гидрохлорида по методике ЛС-002432 (должно быть не менее 99,5 % в пересчете на сухое вещество). Напишите химизм реакций, рассчитайте титр анализируемого вещества по 0,1 М титрованному раствору.
- Дайте обоснование 3. Качественной реакции подлинности сульфадиметоксина, приведенной в ФС.2.1.0180.18 (Приложение № 3). Напишите химизм реакции
- Как можно определить точку эквивалентности в методе комплексонометрии?
- Что понимают под возбужденным состоянием атома? Напишите электронные формулы атома фосфора, находящегося в нормальном и возбужденном состояниях.
- Обоснуйте испытание фенилсалицилата по показателю «Хлориды» в соответствии с требованиями ФС.2.1.0199.18 (Приложения № 3, 7). Укажите категорию примеси, ее допустимость, способ испытания. Приведите химизм реакций.
- Из 1,3 г гидроксида металла получается 2,85 г его сульфата. Вычислите молярную массу эквивалента этого металла.
- Организация работы химико-токсикологической лаборатории наркологического диспансера (наркологической больницы).
- В каком объеме раствора CaCO3 содержится 1 г соли?
