| 🎓 Заказ №: 22183 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Какие из солей угольной кислоты имеют наибольшее промышленное применение? Как получить соду, исходя из металлического натрия, хлороводородной (соляной) кислоты, мрамора и воды? Почему в растворе соды лакмус приобретает синий цвет? Ответ подтвердите составлением уравнений соответствующих реакций.
Решение: Наибольшее промышленное применение имеет сода. Приводя во взаимодействие мрамор и соляную кислоту получим углекислый газ. CaCO3 2HCl CaCl2 H2CO3 H2CO3 H2O CO2

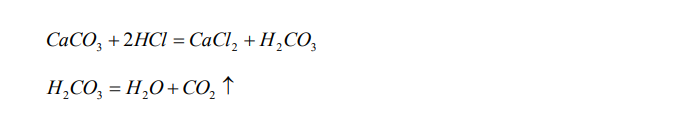
| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Составьте электронные уравнения на основе приведенных схем реакций. Для каждой реакции укажите окислитель и восстановитель.Hg + NaNO3 + H2SO4 → Na2SO4 + Hg2SO4 + NO + H2O
- Напишите ионно-молекулярные уравнения гидролиза, укажите реакцию и рН растворов перечисленных солей K3PO4, (NH4)2CO3, Fe(CNS)3, RbF.
- Мертвое море содержит 320 г солей на 1 л; на долю MgCl2 приходится 44 %, CaCl2 – 21 %, Ca(HCO3)2 – 8 %.
- Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между a) Sn(OH)2 и HCl; б) BeSO4 и КОН; в) NH4Cl и Ва(ОН)2
- Напишите выражения констант равновесия для систем: а) FeО(к) + СО(г) Fe(к) + СО2(г) (реакция экзотермическая) б) 2N2 (г) + О2(г) 2N2О(г) (реакция эндотермическая).
- В сторону какой реакции сместится равновесие системы 2NO Cl2 2NOCl, H 73,6 кДж , если повысить температуру на 30°С; Приведите расчет, если температурный коэффициент прямой реакции равен 2, а обратной 3.
- Реакция горения ацетилена протекает по уравнению С2Н2(г) + 2 5 О2(г) = 2СО2(г) + Н2О(ж).
- Как измеряют рН раствора в ходе анализа?
- Какую высшую степень окисления могут проявлять германий, ванадий, марганец и ксенон?
- Реакция идет по уравнению 2NO + O2 = 2NO2.
