| 🎓 Заказ №: 22215 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Закончите уравнения реакций и укажите названия всех веществ: свет а) CH3 – CH2 – CH3 + Cl2 → …; соли ртути б) CH = CH + H2O → …
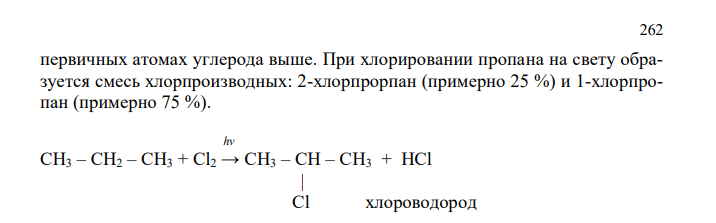
Решение а) Поскольку молекуле пропана два атома водорода находятся при вторичном атоме углерода и 6 атомов водорода находятся при первичных атомах углерода, то вероятность замещения атомом хлора одного из атомов водорода при 262 первичных атомах углерода выше. При хлорировании пропана на свету образуется смесь хлорпроизводных: 2-хлорпрорпан (примерно 25 %) и 1-хлорпропан (примерно 75 %). hv СH3 – CH2 – CH3 + Сl2 → СH3 – CH – CH3 + HCl | Cl хлороводород

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Составьте формулы всех солей, соответствующих взятым попарно кислотам и основаниям, приведенным для вашего задания в табл.7 CsOH
- Дайте обоснование фармакопейному методу количественного определения осальмида по методике ФС 42-3023-94 (Приложение № 3). Напишите химизм реакций, рассчитайте титр анализируемого вещества по 0,1 М титрованному раствору
- Дайте названия соединения СH3 – CH(CH3) – C(CH3)2 – CH3, составьте по два изомера и гомолога, укажите их названия.
- Напишите электронные структуры атомов N и B.
- Определите типы дисперсных систем: активированный уголь, холодец.
- Рассчитать pH раствора, в 4 л которого содержится 47,04 г H2SO4 (α=100%).
- Какова молярность раствора Ba(OH)2, pH которого равен 11? (α=100%)
- Реакции выражаются схемой: P + HNO3 → H3PO4 + NO2 + H2O Подберите коэффициенты в уравнении методом электронного баланса.
- Дайте обоснование испытанию резорцинола по показателю «Прозрачность раствора» в соответствии с требованиями ФС 001037-050315 (Приложения № 3, 6).
- Константа равновесия реакции N2 (г) + 3 Н2 (г) ↔ 2 NН3 (г) + Q равна при некоторой температуре 2,1. Равновесные концентрации водорода и аммиака в реакционной смеси составляли: [Н2] равн. = 0,2 моль/л, [NH3]равн = 0,8 моль/л
