| 🎓 Заказ №: 22204 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Дайте термодинамическую характеристику процесса согласно плану, представленному в примере (табл.4). CH4(г) O2(г) CO2(г) H2O(ж)
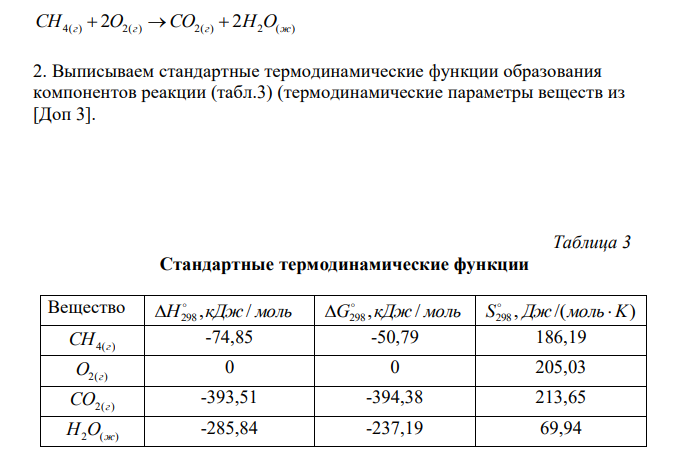
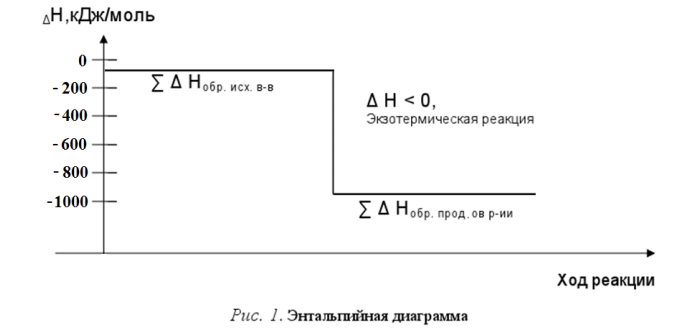
Решение: 1. Записываем стехиометрическое уравнение CH4(г) 2O2(г) CO2(г) 2H2O(ж) 2. Выписываем стандартные термодинамические функции образования компонентов реакции (табл.3) (термодинамические параметры веществ из [Доп 3]. Данные термодинамические функции относятся к 1 моль вещества и при расчетах должны быть умножены на стехиометрические коэффициенты 3. Изменение энтальпии химической реакции рассчитываем по формуле следствия из закона Гесса Hх. р. H298 (СO2(г) ) 2H298 (Н2О(ж) ) H298 (СН4(г) ) 2H298 (О2(г) ) 393,51 2(285,84) (74,85) 20 890,34 кДж Для построения энтальпийной диаграммы, определяем сумму энтальпий образования исходных веществ и продуктов реакции отдельно: Hобр.прод. рции 393,51 2(285,84) 965,19 кДж Hобр.исх.вв 74,8520 74,85 кДж


| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Вычислите стандартную теплоту (энтальпию) образования вещества А, участвующего в процессе 2А + B = 2C, если H B кДж моль обр ( ) 45 / 298 и H С кДж моль обр ( ) 60 / 298 H 150 кДж/ моль.
- Напишите известные Вам эндотермические и экзотермические процессы, происходящие: а) в неживой природе: б) в живой природе; в) в промышленности; г) в быту
- Потенциал серебряного электрода в растворе AgNO3 составляет 85 % от величины его стандартного электродного потенциала.
- Определите рН раствора, в 1 л которого содержится 0,1 г гидроксида натрия.
- Определите объем природного газа (который содержит 98 % метана), требуемого для получения 644 кг муравьиной кислоты методом каталитического окисления.
- Указать тип химической связи в ионе гидроксония H3O + .
- Почему кислород и сера, имея в наружном слое одинаковое число электронов, проявляют разную валентность?
- Напишите полную электронную формулу элемента церия Ce 58 .
- Имеется два образца сильвинита (калийное удобрение), содержащих 40 % K2O и 10 % K2O.
- Какой из 3-х растворов будет обладать наибольшим осмотическим давлением, если в 1 л каждого раствора содержится по 4,6 г: а) глицерина C3H8(OH)3; б) этилового спирта C2H5OH; в) хлорида натрия.
