| 🎓 Заказ №: 22214 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Вычислите тепловой эффект реакции (Q) восстановления оксида железа FeO водородом: FeO(к) + H2(г) = Fe(к) + H2O(г), используя следующие термодинамические данные. 1. FeO(к) + CO(г) = Fe(к) + CO2(г), H1 13,2 кДж 2. СО(г) + 1/2 О2(г) = СО2(г), H2 283,0 кДж 3. Н2(г) + 1/2 О2 (г) = Н2О (г), H3 241,8 кДж
Решение: C термохимическими уравнениями и их тепловыми эффектами можно оперировать так же, как и с алгебраическими уравнениями.
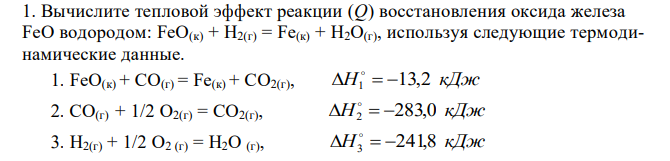

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Какие из ниже приведенных процессов характеризуются убылью энтропии: 1. H2O(ж) → H2O(к); 2. H2(г) + 2Na(к) → 2NaH(к); 3. 2HI(г) → H2(г) + I2(г)?
- Дан водный электролита Хлорид галлия (III) GaCl3
- Сделайте предварительный расчет объема 0,1 М раствора натрия нитрита, который израсходуется на титрование 0,25 г порошка растертых таблеток стрептоцида по 0,3 г (М.м. 172,21).
- Рассчитать массу навески перманганата калия, содержащую 5% индифферентных примесей, для приготовления 2,00 дм3 раствора с титриметрическим фактором пересчёта по пероксиду водорода 0,0001700 г/см3 .
- Руководствуясь Периодической системой, определите название химического элемента.
- Константы нестойкости комплексных ионов [Co(NH3)6] 3+, [Fe(CN)6] 4– , [Fe(CN)6] 3– соответственно равны 6,2 · 10–36, 1,0 · 10–37, 1,0 · 10–44.
- Рассчитать массовую долю CuSO4 в образце, если на навеску 0,5768 г идёт при титровании 14,25 см3 0,2000 моль/дм3 раствора трилона Б.
- Диффузия в полимерах. Растворимость полимеров. Процесс набухания. Структура растворов полимеров.
- Растворимость нитрата натрия при 30 °С составляет 40 г на 100 г раствора.
- Обоснуйте испытание калия бромида по показателям «Барий» и «Броматы» в соответствии с методикой и требованиями ФС.2.2.0023.18 (Приложение №3). Укажите категорию примеси, её допустимость, способ испытания. Приведите химизм реакций.
