Закон Гей-Люссака
При постоянном давлении 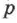 объём
объём 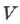 идеального газа меняется линейно с температурой.
идеального газа меняется линейно с температурой.
То есть
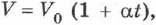
где 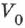 — начальный объём,
— начальный объём, 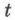 — разность начальной и конечной температур. Коэффициент теплового расширения идеальных газов
— разность начальной и конечной температур. Коэффициент теплового расширения идеальных газов 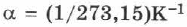 одинаков для всех газов.
одинаков для всех газов.
Процесс изменения состояния термодинамической системы при постоянном давлении называется изобарным (от греч. baros — вес, тяжесть).
Закон открыт французским учёным Ж. Гей-Люссаком в 1802 г. и независимо от него Дж. Дальтоном в 1801 г.
Закон Гей-Люссака, как и другие газовые законы, является следствием уравнения состояния идеального газа. Это становится очевидным, если в (2.18) заменить 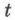 на абсолютную температуру
на абсолютную температуру 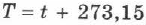 , а коэффициент расширения
, а коэффициент расширения 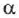 — его численным значением 1/273,15:
— его численным значением 1/273,15: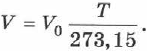
или
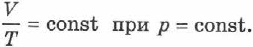
Эта зависимость графически изображается прямой, которая называется изобарой (рис. 69).
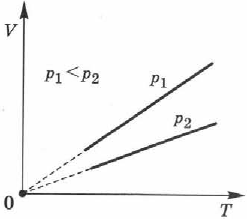
Различным давлениям соответствуют разные изобары. С ростом давления объём газа при постоянной температуре, согласно закону Бойля — Мариотта, уменьшается, поэтому изобара, соответствующая более высокому давлению 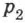 , лежит ниже изобары, соответствующей более низкому давлению
, лежит ниже изобары, соответствующей более низкому давлению 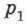 .
.
В области низких температур все изобары идеального газа сходятся в точке 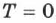 , но это не означает, что объём реального газа действительно обращается в нуль. При низких температурах все газы обращаются в жидкости, а к жидкостям уравнение состояния не применимо.
, но это не означает, что объём реального газа действительно обращается в нуль. При низких температурах все газы обращаются в жидкости, а к жидкостям уравнение состояния не применимо.
Эта лекция взята со страницы лекций по всем темам предмета физика:
Возможно эти страницы вам будут полезны:
| Закон Бойля — Мариотта в физике |
| Закон Шарля в физике |
| Свойства тел в разных агрегатных состояниях в физике |
| Испарение и конденсация в физике |

