Оглавление:
Расчеты по уравнению состояния идеальных газов
Во всех расчетах используется уравнение Клапейрона-Менделеева:
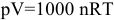
или
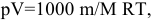
если объем измеряется в литрах, давление — в паскалях, масса — в граммах, молярная масса — в граммах на моль, температура — в кельвинах и R = 8,314 Дж/(моль*К).
Пример 24
Масса 227 мл газа, взятого при температуре 37°С и при давлении 730 мм рт.ст., равна 0,313 г. Определить молярную массу этого газа.
Решение:
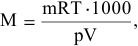
где р = 97325 Па; V = 0,227 л; Т = 310К.
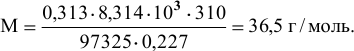
Пример 25
Определить объем, занимаемый 140 г азота при температуре 32°С и при давлении 2,8 атм.
Решение: 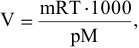
где 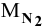 = 28 г/моль; Т = 305 К; р = 283710 Па.
= 28 г/моль; Т = 305 К; р = 283710 Па.
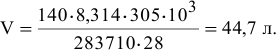
Пример 26
Определенное количество газа занимает объем 152 мл при давлении 745 мм рт.ст. и температуре 25°С. Найти объем того же количества газа при нормальных условиях 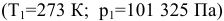 .
.
Решение: 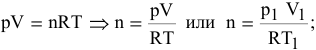
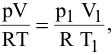
где 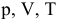 — начальные условия;
— начальные условия;
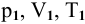 , — конечные условия;
, — конечные условия;
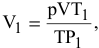
где р = 99 325 Па; Т = 298 К; V = 0,152 л;
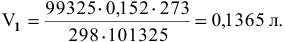
Пример 27
В закрытом металлическом сосуде находится газ при температуре 20°С. До какой температуры необходимо нагреть этот газ, чтобы увеличить его давление в 3 раза?
Решение:
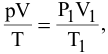 ,
,
где 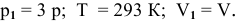
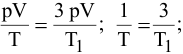
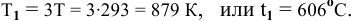
Эти задачи взяты со страницы решения задач по неорганической химии:
Задачи с решением по неорганической химии
Возможно эти страницы вам будут полезны:

