Задача В10. В баллоне находится газ при температуре 15 °C. Во сколько раз уменьшится давление газа, если 40 % его выйдет из баллона, а температура при этом понизится на 8 °C?
Обозначим t начальную температуру газа по шкале Цельсия, Т — эту же температуру по шкале Кельвина (абсолютную температуру), 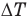 — изменение температуры, m — начальную массу газа,
— изменение температуры, m — начальную массу газа, 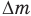 — изменение массы газа в баллоне (или массу газа, вышедшего из баллона), V — объем газа, R — молярную газовую постоянную, М — молярную массу газа,
— изменение массы газа в баллоне (или массу газа, вышедшего из баллона), V — объем газа, R — молярную газовую постоянную, М — молярную массу газа, 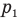 — начальное давление газа в баллоне,
— начальное давление газа в баллоне, 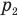 — его конечное давление.
— его конечное давление.
Указание: изменение температуры по шкале Цельсия 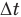 равно изменению температуры по шкале Кельвина
равно изменению температуры по шкале Кельвина 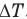 , т.е., если
, т.е., если 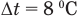 , то и
, то и 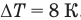 .
.
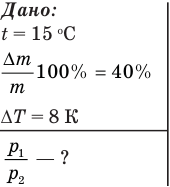
Решение:
Поскольку здесь речь идет о массе газа, воспользуемся уравнением Менделеева — Клапейрона, в которое эта масса входит. Запишем это уравнение для первого состояния, когда в баллоне была вся масса газа:
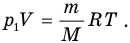
После того как из баллона вышла масса газа 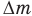 , в нем осталась масса
, в нем осталась масса 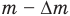 , и при этом температура газа понизилась на
, и при этом температура газа понизилась на 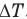 , т.е. стала равной
, т.е. стала равной 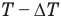 . Поэтому теперь запишем уравнение Менделеева — Клапейрона для нового состояния:
. Поэтому теперь запишем уравнение Менделеева — Клапейрона для нового состояния:
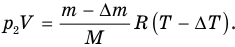
Теперь, чтобы найти отношение 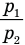 , надо разделить первое уравнение на второе и выполнить сокращения:
, надо разделить первое уравнение на второе и выполнить сокращения:
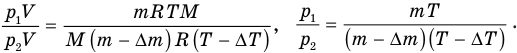
Но нам не даны ни масса газа m, ни ее изменение 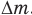 , а дано отношение
, а дано отношение 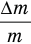 выраженное в процентах. Если
выраженное в процентах. Если 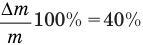 , то
, то 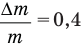 . Чтобы получить отношение
. Чтобы получить отношение 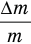 в последнем уравнении, разделим в его правой части числитель и знаменатель на m (от этого равенство не нарушится):
в последнем уравнении, разделим в его правой части числитель и знаменатель на m (от этого равенство не нарушится):
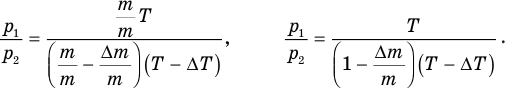
Теперь заменим отношение 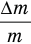 его числовым значением
его числовым значением 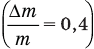 :
:
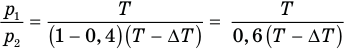
Выразим начальную температуру в единицах СИ:
15 °C = 288 К.
Произведем вычисления:
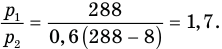
Ответ: 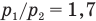 .
.
Эта задача взята со страницы подробного решения задач по физике, там расположена теория и подробное решения задач по всем темам физики:
Возможно вам будут полезны эти задачи:
