Выход по току
Отношение массы полученного вещества к массе, теоретически вычисленной на основании закона Фарадея, называется выходом по току.
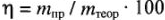 , где
, где
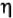 — выход по току, %;
— выход по току, %;
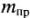 — масса вещества, реально полученного при электролизе, г;
— масса вещества, реально полученного при электролизе, г;
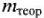 — масса, рассчитаная по закону электролиза, г.
— масса, рассчитаная по закону электролиза, г.
Выход по току меньше 100 % потому, что наряду с основными электродными реакциями протекают побочные или параллельные реакции.
Алгоритм составления схем электролиза водных растворов
1. Составляем диссоциацию электролита:
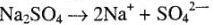
2. Указываем направление движения ионов в электролизере:
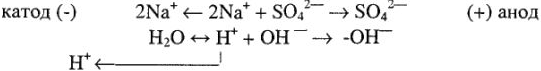
3. Выписываем электродные уравнения всех возможных процессов (на основе ТОВП):
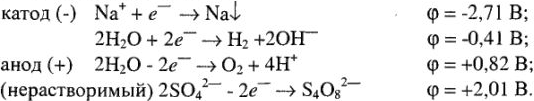
4. Записываем уравнения процессов, реально протекающих на электродах, учитывая следующее:
а) на катоде восстанавливается более сильный окислитель (нужно руководствоваться порядком разряда катионов):
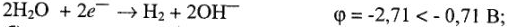
б) на аноде окисляется более сильный восстановитель (порядок анодных процессов, и можно использовать правило: чем проще по составу частица, тем она легче разряжается на аноде; исключение составляет 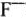 );
);
5. Составляем итоговое уравнение электролиза, суммируя реально протекающие процессы:
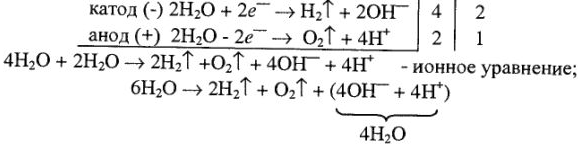
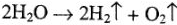 — молекулярное уравнение. Из продуктов реакций, образующихся на катоде и аноде, составляем микрогальванический элемент (учитывая, что электроды графитовые):
— молекулярное уравнение. Из продуктов реакций, образующихся на катоде и аноде, составляем микрогальванический элемент (учитывая, что электроды графитовые):
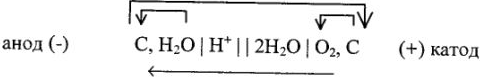
Рассчитываем потенциал разложения (теоретический и практический) с учетом поляризации на электродах:
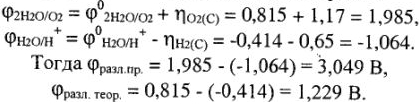
Эта теория взята со страницы подробного решения задач по всем темам химии:
Возможно эти страницы вам помогут:
| Поляризация в химии |
| Законы электролиза (фарадея) в химии |
| Коррозия металлов в химии |
| Защита металлов от коррозии в химии |

