Оглавление:
Влияние комплексообразования на величину потенциала
Окисленная или восстановленная формы системы могут связываться в комплексы или образовывать малорастворимые соединения. В таких случаях образуется новая пара, стандартный потенциал которой связан с потенциалом пары Ox/Red через константу, характеризующую побочную реакцию. В случае образования комплекса -это константа устойчивости комплекса 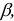 в случае образования малорастворимого соединения — константа растворимости малорастворимого электролита или произведение растворимости
в случае образования малорастворимого соединения — константа растворимости малорастворимого электролита или произведение растворимости 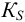 .
.
Учет комплексообразования можно провести через молярные доли форм по общему уравнению (5.4) с использованием (2.8). При условии преобладания комплекса одного состава — 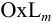 , для которого
, для которого
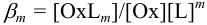
и при участии 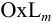 в полуреакции
в полуреакции
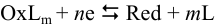
уравнение Нернста примет вид:
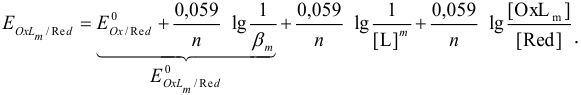
Аналогично, при связывании восстановленной формы в комплекс:
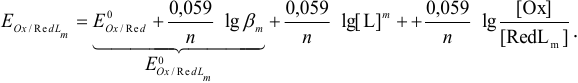
Суммы первых трех членов в этих уравнениях представляют собой формальные потенциалы пар: 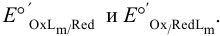 .
.
Формулы (5.7 — 5.10) могут быть использованы и в решении обратных задач — вычисления соответствующих констант по значениям потенциалов (примеры 5.9, 5.11).
Пример 5.8.
Рассчитать формальный потенциал окислительно-восстановительной пары, образованной ионами 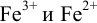 , в 2М растворе фторида аммония, если
, в 2М растворе фторида аммония, если 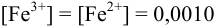 моль/л.
моль/л.
Решение:
Ионы 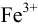 (окисленной формы) вступают в реакции комплексообразования с ионами
(окисленной формы) вступают в реакции комплексообразования с ионами 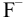 . Поскольку ионы
. Поскольку ионы 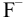 взяты в большом избытке, можно считать, что в растворе протекает реакция
взяты в большом избытке, можно считать, что в растворе протекает реакция
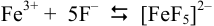
и образуется пара 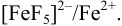
Рассчитаем 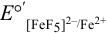 по формуле (5.7):
по формуле (5.7):
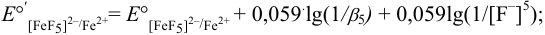
справочные данные: 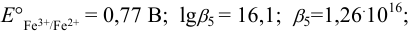
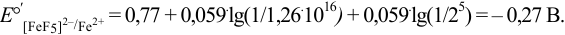
Следовательно, связывание 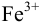 , т. е. окисленной формы в комплекс, привело к сильному снижению стандартного потенциала
, т. е. окисленной формы в комплекс, привело к сильному снижению стандартного потенциала 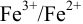 и, соответственно, окислительных свойств
и, соответственно, окислительных свойств 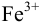 .
.
Учет конкурирующих реакций можно провести и по формуле (5.4), предварительно вычислив молярную долю свободных ионов 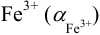 по формуле (2.8)
по формуле (2.8)
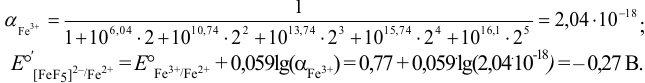
Результаты расчетов двумя способами получаются одинаковыми, что указывает на правильность предположения о преобладании формы 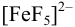 и об отсутствии необходимости учета других форм комплексных ионов.
и об отсутствии необходимости учета других форм комплексных ионов.
Пример 5.9.
Вычислите константу устойчивости комплексного иона 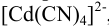 , если для полуреакции:
, если для полуреакции:
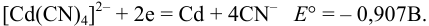
Решение:
Найти величину 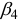 для комплекного иона
для комплекного иона 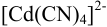 можно, используя формулу (5.7), согласно которой
можно, используя формулу (5.7), согласно которой
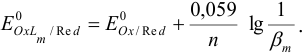
Стандартный потенциал 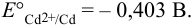 Тогда:
Тогда:
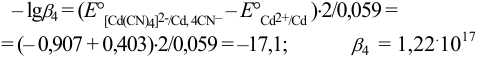
Эти примеры взяты со страницы примеров решения задач по аналитической химии:
Решение задач по аналитической химии
Возможны вам будут полезны эти страницы:

