Оглавление:
Расчеты при приготовлении растворов протолитов с заданным значением pH
При решении задач на указанную тему следует:
а) установить конкретный случай кислотно-основного взаимодействия (протолитической реакции): сильная, слабая кислота; сильное, слабое основание; амфолит; гидролизующаяся соль; буферный раствор; написать уравнения протолитических взаимодействий;
б) подобрать соответствующие формулы для расчета 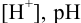 и др. и преобразовать их относительно неизвестной величины -концентрации раствора, или соотношения концентраций (для буферного раствора);
и др. и преобразовать их относительно неизвестной величины -концентрации раствора, или соотношения концентраций (для буферного раствора);
в) по найденному значению концентрации вычислить, если необходимо, другие величины: массу вещества, объем раствора и др.
Пример 3.12.
В каком объеме воды необходимо растворить 1,000 г 17,58 % раствора 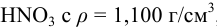 , чтобы pH полученного раствора был равен 1,50?
, чтобы pH полученного раствора был равен 1,50?
Решение:
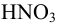 (М = 63 г/моль) — сильная кислота, поэтому pH в растворе связан с концентрацией соотношением (табл. 3.1):
(М = 63 г/моль) — сильная кислота, поэтому pH в растворе связан с концентрацией соотношением (табл. 3.1):
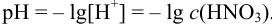
Зная pH, можно рассчитать молярную концентрацию полученного раствора:
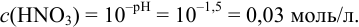
Рассчитаем массу 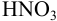 в 1г раствора с
в 1г раствора с 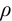 = 1,1 г/мл:
= 1,1 г/мл:
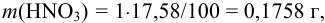
а также объем этого раствора: 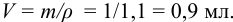
Находим объем полученного раствора с концентрацией 0,03 моль/л:
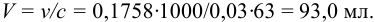
Необходимо добавить объем воды 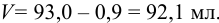 .
.
Пример 3.13.
Сколько мл 10,1 % 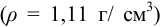 раствора
раствора 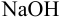 нужно добавить к 1000 мл 0,0010 М раствора
нужно добавить к 1000 мл 0,0010 М раствора 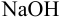 , чтобы pH был равен 12?
, чтобы pH был равен 12?
Решение:
Исходный (1) раствор 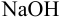 имеет pH:
имеет pH:
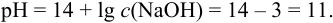
Следовательно, добавлением 10,1 % -го раствора нужно повысить pH на 1 и 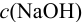 повысится до 0,010 моль/л (раствор 2). При смешивании растворов 1 и 2 справедливо правило:
повысится до 0,010 моль/л (раствор 2). При смешивании растворов 1 и 2 справедливо правило:
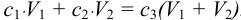
Рассчитаем
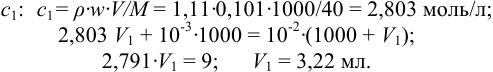
Пример 3.14.
Какую навеску 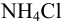 следует растворить в 100 мл воды, чтобы pH был равен 5,5?
следует растворить в 100 мл воды, чтобы pH был равен 5,5?
Решение:
При растворении 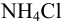 в воде протекает реакция:
в воде протекает реакция:
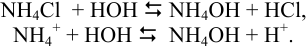
Рассчитаем константу гидролиза по формуле (3.5):
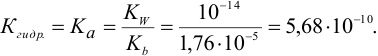
Используя формулу (3.5), рассчитаем концентрацию соли:
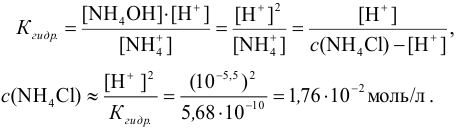
Вычислим навеску 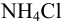 :
:
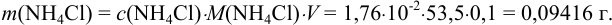
Пример 3.15.
Какую массу бензоата натрия нужно добавить к 500 мл 0,016 М раствора бензойной кислоты, чтобы получить раствор с pH 4,42?
Решение:
При растворении бензоата натрия в растворе бензойной кислоты 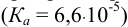 образуется буферный раствор.
образуется буферный раствор.
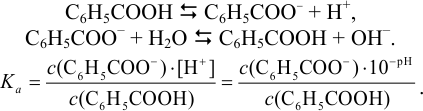
Из этого выражения можно найти молярную концентрацию соли:
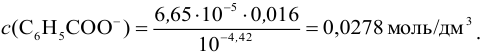
Тогда навеска бензоата натрия 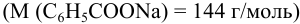 :
:
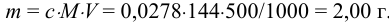
Пример 3.16. *
Буферные системы на основе а-аминокислот поддерживают pH в физиологических средах, в плазме крови; используются в анализе. В частности, из 0,100 М водного раствора аминоуксусной кислоты (глицина) и 0,100 М растворов 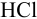 или
или 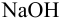 готовят буферные растворы с pH соответственно 1,10 ч- 3,50 или 8,53 ч- 12,9 на фоне 0,1 М
готовят буферные растворы с pH соответственно 1,10 ч- 3,50 или 8,53 ч- 12,9 на фоне 0,1 М 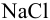 . В водном растворе глицина преобладает его биполярный таутамер:
. В водном растворе глицина преобладает его биполярный таутамер: 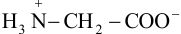
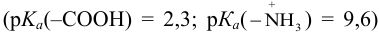 . Используя указанные концентрации растворов и приведенные справочные данные (ионную силу не учитывать):
. Используя указанные концентрации растворов и приведенные справочные данные (ионную силу не учитывать):
а) вычислите pH в 0,100 М водном растворе глицина с обоснованием расчетной формулы; б) рассчитайте объем 0,100 М раствора глицина, необходимый для приготовления 1000 мл буферного раствора с pH 3,00 (с буферной емкостью 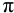 = 0,027).
= 0,027).
Решение:
а) глицин — амфолит, для которого через уравнения материального баланса или электронейтральности и соответствующих 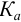 , можно вывести формулу для расчета
, можно вывести формулу для расчета 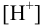 :
:
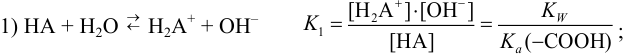
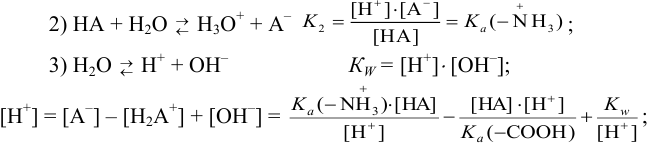
Преобразуя последнее выражение относительно 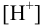 , получаем:
, получаем:
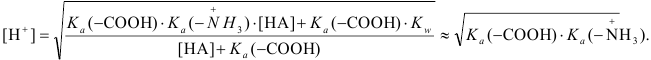
Расчет по выведенной формуле (считая [НА] ~ 0,1) и приближенной формуле приводит к pH = 6,86.
б) для получения “кислого” буферного раствора к 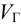 мл 0,1 М глицина нужно добавить
мл 0,1 М глицина нужно добавить 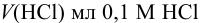 для частичного перевода основания в сопряженную кислоту:
для частичного перевода основания в сопряженную кислоту:
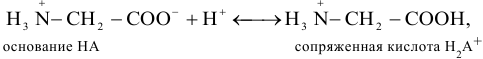
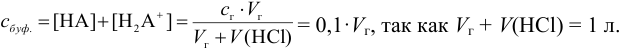
Расчет 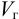 можно провести через уравнение для буферной емкости (
можно провести через уравнение для буферной емкости (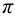 ):
):
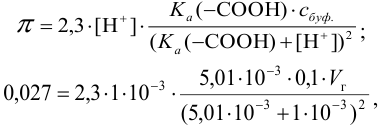
откуда 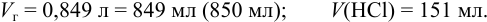
Для расчета можно также использовать уравнение (3.11), учитывая, что 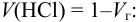
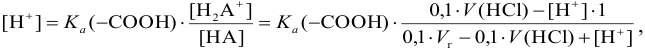
с последующей проверкой буферной емкости по формуле (3.13).
Эти примеры взяты со страницы примеров решения задач по аналитической химии:
Решение задач по аналитической химии
Возможны вам будут полезны эти страницы:

