Оглавление:



Произведение растворимости
- Растворимость продукта. большинство Вещество имеет ограниченную растворимость в воде и др. Растворитель. Поэтому на практике часто приходится встречаться В системе в равновесии Осадок и насыщенный электролит. Для динамики Равновесных характеристик скорости растворения Осадок соответствует проценту обратного процесса Крис talizatsii.
- Следовательно, в случае насыщенного раствора электролита ApB. Характеристика нахождения в равновесии с твердой фазой Ren следующий обратимый процесс: A „b ^ (m)». ■ = роспуск кристаллизация Этот процесс неравномерен. Другими словами, Поверхность месторождения. Следовательно, константа равновесия этого процесса Определяется только по продукту ионной активности.
В растворе, не зависящем от активности твердых компонентов: / (P-PRd ^ a __- ’c- (U1.20). Людмила Фирмаль
Следовательно, продукт ионной активности электролита, Содержится в насыщенном растворе при определенной температуре Есть круглые и постоянные значения. Это значение Как указать растворимость электролита и PR Константа равновесия, от которой зависит продукт растворимости Не только природа растворенного вещества и растворителя, Это температура и не зависит от активности ионов в растворе.
В настоящее время экспериментальные определения положительны Это проблема нерастворимости отдельных ионов. О н Этот продукт растворимости относится к Malora Фактический электролит, т.е. такой электролит, концентрация Нормативный насыщенный раствор. Рассчитать коэффициент Индивидуальные ионные факторы активности применяют ионные правила Замените активы с достаточной силой или достаточной точностью.
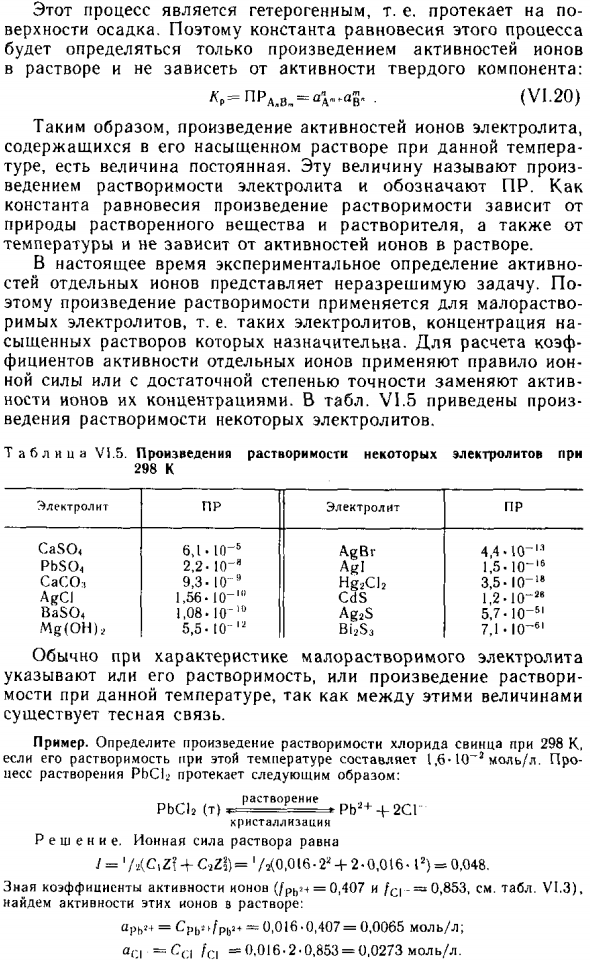
- Ионы ионизируются в зависимости от концентрации. В таблице. V I.5 отображается Поддерживает растворимость некоторых электролитов. Таблица U]. 5. Продукты растворимости нескольких электролитов 298 К Обычно при характеристике плохо растворимых электролитов Указывает на растворимость или продукт раствора Между этими значениями, поэтому мост при данной температуре.
Есть близкие отношения. Пример. Если растворимость при этой температуре составляет 1,6, моль / л Процесс растворения Pb C 12 протекает следующим образом: P b c b (t) роспуск Кристалл 1 Исайин Ионная сила раствора для определения Y = C22 |) = ‘/ 2 (0,016-2 ^ + 2-0,016-12) = 0,048 Знать коэффициент активности ионов (/ pb ^ — * = 0,407 и / (^ 1- = 0,853, см. Таблицу V I.3).
Определить продукт растворимости хлорида свинца при 298 К. Людмила Фирмаль
Найти активность этих ионов в растворе. == 0,016-0,407 = 0,0065 моль / л; ¡Ysh = ^ s; (1 \ == 0,016-2-0,853 = 0,0273 моль / л Учитывая это, продукт растворимости хлорида свинца при 298 К составляет nPphci ^ = Opbv + a ^; i- = 0.0065.0.0273 ^ = 4.8-U — ‘*. Знание ионной активности труднорастворимых электролитов в гонках Создатель, может приблизительно оценить, упадут ли данные Состояние депозита.
Для этого нужны ионные действия Введите в формулу (V I.20) и сравните с полученным значением Ссылка (таблица). Если получено, выпадут осадки Продукт ионной активности превышает таблицу. По формуле (V I.20) Один из ионов труднорастворимой электролитной активности Второй ион уменьшен. Так что, если есть небольшое решение Сделать электролит Сильный электролит, содержащий ионы с таким же названием, затем растворенный.
Менее растворимые электролиты снижаются. Например Добавить NaCO3. ^ Концентрация в растворе CaCO3 Концентрация ионов COz ~ и, следовательно, ионов Ca ^ ‘^ уменьшается Соответственно, растворимость CaCO3 уменьшается. Таким образом Слабо растворимые электролиты могут выпадать в осадок из раствора.
Смотрите также:
| Водородный показатель pH | Реакции в растворах электролитов |
| Кислотно-основные индикаторы | Смещение равновесия в растворах электролитов |

