Насыщенные и ненасыщенные пары
Если испарение происходит в закрытом сосуде, то сначала число молекул, вылетевших из жидкости, будет больше числа молекул, возвратившихся обратно в жидкость. Поэтому плотность пара в сосуде будет постепенно увеличиваться. С увеличением плотности пара увеличивается и число молекул, возвращающихся в жидкость. Довольно скоро число молекул, вылетающих из жидкости, станет равным числу молекул пара, возвращающихся обратно в жидкость. С этого момента число молекул пара над жидкостью будет постоянным. Для воды при комнатной температуре это число приблизительно равно 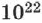 молекул за 1 с на
молекул за 1 с на 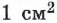 площади поверхности. Наступает так называемое динамическое равновесие между паром и жидкостью.
площади поверхности. Наступает так называемое динамическое равновесие между паром и жидкостью.
Пар, находящийся в динамическом равновесии со своей жидкостью, называется насыщенным паром.
Это означает, что в данном объёме при данной температуре не может находиться большее количество пара. При динамическом равновесии масса жидкости в закрытом сосуде не изменяется, хотя жидкость продолжает испаряться. Точно так же не изменяется и масса насыщенного пара над этой жидкостью, хотя пар продолжает конденсироваться.
При сжатии насыщенного пара, температура которого поддерживается постоянной, равновесие сначала начнёт нарушаться: плотность пара возрастет, и вследствие этого из газа в жидкость будет переходить больше молекул, чем из жидкости в газ; продолжаться это будет до тех пор, пока концентрация пара в новом объёме не станет прежней, соответствующей концентрации насыщенного пара при данной температуре (и равновесие восстановится). Объясняется это тем, что число молекул, покидающих жидкость за единицу времени, зависит только от температуры.
Итак, концентрация молекул насыщенного пара при постоянной температуре не зависит от его объёма.
Поскольку давление газа пропорционально концентрации его молекул, то и давление насыщенного пара не зависит от занимаемого им объёма. Давление 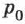 , при котором жидкость находится в равновесии со своим паром, называют давлением насыщенного пара.
, при котором жидкость находится в равновесии со своим паром, называют давлением насыщенного пара.
При сжатии насыщенного пара большая его часть переходит в жидкое состояние. Жидкость занимает меньший объём, чем пар той же массы. В результате объём пара при неизменной его плотности уменьшается.
Для идеального газа справедлива линейная зависимость давления от температуры при постоянном объёме. Применительно к насыщенному пару с давлением 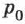 эта зависимость выражается равенством:
эта зависимость выражается равенством:
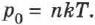
Так как давление насыщенного пара не зависит от объёма, то, следовательно, оно зависит только от температуры.
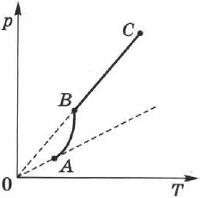
Экспериментально определённая зависимость 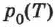 отличается от зависимости (2.20) для идеального газа (рис. 72). С увеличением температуры давление насыщенного пара растёт быстрее, чем давление идеального газа (участок кривой
отличается от зависимости (2.20) для идеального газа (рис. 72). С увеличением температуры давление насыщенного пара растёт быстрее, чем давление идеального газа (участок кривой 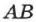 на рис. 72). Это становится особенно очевидным, если провести изохору через точку
на рис. 72). Это становится особенно очевидным, если провести изохору через точку 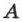 (пунктирная прямая). Происходит это потому, что при нагревании жидкости часть её превращается в пар и плотность пара растёт.
(пунктирная прямая). Происходит это потому, что при нагревании жидкости часть её превращается в пар и плотность пара растёт.
Поэтому, согласно формуле (2.20), давление насыщенного пара растёт не только в результате повышения температуры жидкости, но и вследствие увеличения концентрации молекул (плотности) пара. Главное различие в поведении идеального газа и насыщенного пара заключается в изменении массы пара при изменении температуры при неизменном объёме (в закрытом сосуде) или при изменении объёма при постоянной температуре. С идеальным газом ничего подобного происходить не может (МКТ идеального газа не предусматривает фазового перехода газа в жидкость).
После испарения всей жидкости поведение пара будет соответствовать поведению идеального газа (участок  кривой на рис. 72).
кривой на рис. 72).
Если в пространстве, содержащем пары какой-либо жидкости, может происходить дальнейшее испарение этой жидкости, то пар, находящийся в этом пространстве, является ненасыщенным.
Пар, не находящийся в состоянии равновесия со своей жидкостью, называется ненасыщенным.
Ненасыщенный пар можно простым сжатием превратить в жидкость. Как только это превращение началось, пар, находящийся в равновесии с жидкостью, становится насыщенным.
Эта лекция взята со страницы лекций по всем темам предмета физика:
Возможно эти страницы вам будут полезны:
| Свойства тел в разных агрегатных состояниях в физике |
| Испарение и конденсация в физике |
| Кипение жидкости в физике |
| Теплота парообразования в физике |

