Оглавление:






Кристаллическое строение металлов
- Кристаллическая структура металла Общими свойствами металлов и сплавов являются их кристаллическая структура, характеризующаяся постоянным и регулярным расположением атомов в пространстве. Для описания атомно-кристаллической структуры используется понятие кристаллической решетки, представляющей собой воображаемую пространственную сетку с ионами (атомами) в узлах. Атомно-кристаллическая структура может быть представлена изображением одной элементарной ячейки, а не серией периодически повторяющихся объемов. Это имя ячейки, которое повторяется во всех трех измерениях.
Перемещая этот наименьший объем, кристаллическая структура может быть полностью воспроизведена. 1.1). Элементарные частицы (атомы, ионы) в Кристалле сближаются для контакта. Для упрощения пространственного изображения принято заменять схему, в которой центр тяжести частиц представлен точками. На пересечении прямых линий находятся атомы, их называют узлами решетки. Расстояния между центрами атомов, расположенных в соседних узлах решетки a, b и C, называются параметрами, или периодами решетки.
Их величина равна металлу 0,1-0,7 нм или размеру базовой ячейки 0,2-0,3 Нм. Людмила Фирмаль
Для четкого описания единичных сеток кристаллической решетки необходимо знать параметры a, b, C и значения углов между ними. В 1848 году французский ученый Браве показал, что по изученной трансляционной структуре и симметричным элементам можно выделить 14 типов кристаллических решеток. Решетка Bravais 14, 7 проста и построена осевым переводом в узел ячейки, а 7 сложна и состоит из центра объема единичной ячейки(центрированного по объему) или поверхности ячейки. / 1 1-л/| — / \ \ / И- Один. — Д. — Я есть-4— -■> / К-Л — Я / /! С / * * * Я / \—год-/ п На рисунке в центре показаны 7 типов простой кристаллической решетки.
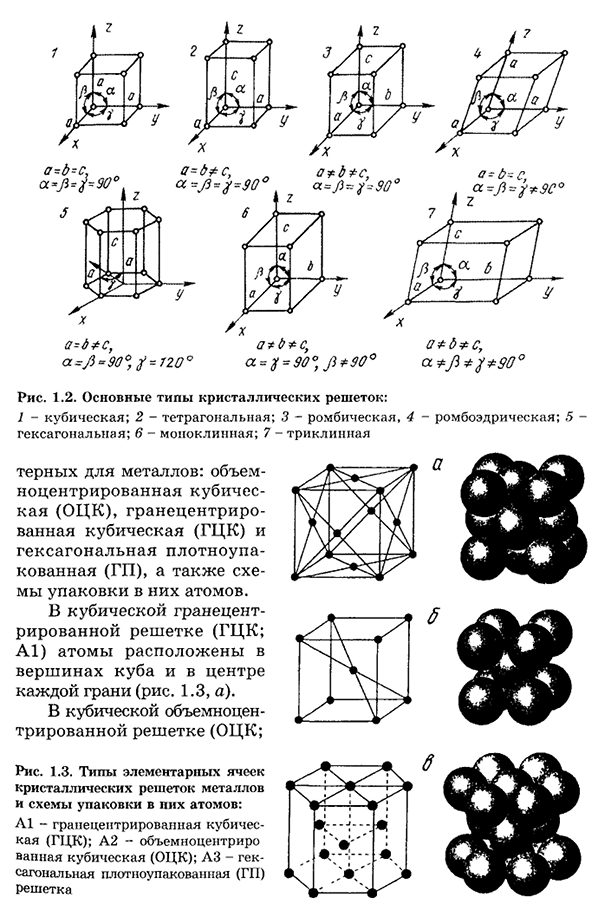
1.2 в большинстве случаев сам металл имеет более сложную решетку, поскольку элементарные частицы могут находиться не только в узлах, но и на их гранях и в центре решетки. Для риса. 1.3 показаны три вида основных ячеек кристаллической решетки, наиболее характерные- Рис 1.1. Кристаллическая решетка 22а=B * С, а=_fl=90А, ТФ=120° абс=^С О°Цзи * 9 0° Рис 1.2 основные типы кристаллической решетки:1-кубическая; 2-тетрагональная; 3-ромбическая; 4-ромбическая; 5-гексагональная;6-моноклинная; 7-триклинная Для металлов: объемно-центрированная кубическая (ОЦК), гранецентрированная кубическая (ГЦК) и гексагональная высокоплотная ковка (ГП), а также схемы заполнения их атомами.
- В гранецентрированной решетке Куба(HCC; A1) атомы расположены в верхней части куба и в центре каждой грани(рис. 1.3, а). Продукт кубической решеткой(КДС; Рис. 1.3. тип основных ячеек кристаллической решетки металлов и схема упаковки их атомов: А1-гранецентрированная кубическая (ГЦК); А2-объемноцентрированная кубическая (БЦК); АЗ-гексагональная плотная упаковка (ГЦК).) 23A2) атом расположен в верхней части куба, и один атом находится в центре его объема. 1.3, б). Атом расположен на вершине и в центре шестиугольного основания призмы, а три атома расположены на промежуточной грани призмы. 1.3, б).
Для характеристики кристаллической решетки введено понятие координационного числа и коэффициента компактности. Координационное число 1K — это число атомов, находящихся на самом близком равноудаленном расстоянии от этого атома. Для ОЦК решетки координационное число равно 8, а для ГЦК и ГП решеток 12. Показано, что решетка ОЦК менее компактна, чем решетки ГЦК и ГП. В решетке BCC каждый атом имеет 8 ближайших соседей, а в сетках HCC и GP-12. Предполагая, что атомы в решетке являются упругими шарами в
Контакте, легко увидеть, что в дополнение к атомам в решетке есть значительное свободное пространство. Людмила Фирмаль
Плотность кристаллической решетки, то есть, объем, занимаемый атомами, характеризуется коэффициентом компактности. Коэффициент компактности Q равен отношению общего объема атомов, входящих в решетку, к объему решетки: Q 4l7s п ЗУ Сто., Где R-радиус атома (Иона), n-основание, или число атомов в элементарной ячейке, и Y-объем элементарной ячейки. Для простой кубической решетки n=(1/8) −8=1;Y=A3==(2L) 3i компактный коэффициент Q=52%. Схема определения базиса решетки ВСС показана на рисунке. 1.4. Ячейка принадлежит 1/8 атома от каждого угла, поэтому есть атом как сумма центра и вершины. Для BCC p= (1/8)- 8 + 1 = 2. Учитывая континуум атомов \
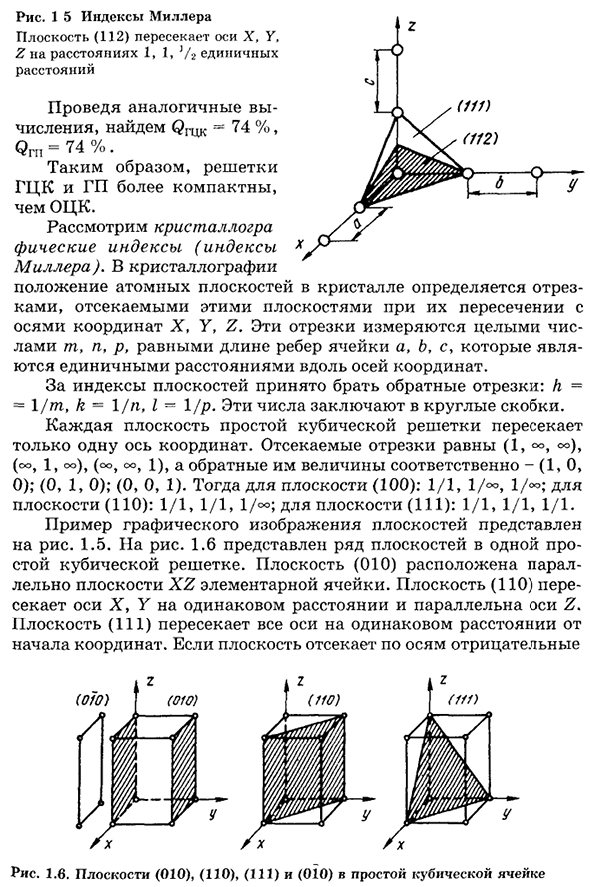
После Один. Семь. Восемь. * Вт’/ 4″^ы Параметр решетки равен a= = 1R — / z, а компактный коэффициент равен Q0L[K=68%]. 1 4 схемы определения основы решетки ВСС риса 24 часа 1 самолет индекса 5Miller (112) пересекает Х, Y, и оси Z на единицу расстояние расстояние расстояние 1, 1,’ / г 4z ящика После аналогичного расчета мы находим QnjK=74%, Qrn=74%. Поэтому сетки ГЦК и ГП более компактны, чем ГЦК. Рассмотрим кристаллографический индекс (x m-индекс иллера). В кристаллографии положение атомной плоскости в кристалле определяется отрезками, вырезанными этими плоскостями на пересечении с координатными осями X, Y, Z. Для индекса самолета, это общепринято, чтобы взять обратный сегмент: ч==1 / ТП, к=1/п, я=1/р. Каждая плоскость простой кубической решетки пересекает только одну координатную ось.
Отрезанные сегменты(1,°), (OO, 1, OO) и (OO, OO, 1) имеют противоположные значения(1, O, 0); (0, 1, 0); (0, 0, 1). Тогда за самолет(100): 1/1, 1/°=, 1/°°; для плоских поверхностей(110): 1/1, 1/1, 1/°°; для плоских поверхностей(111): 1/1, 1/1, 1/1. Пример графического представления плоскости показан на рисунке. За 1,5 рис. 1.6 представляет собой ряд плоскостей в одной простой кубической решетке. Плоскость (010)параллельна плоскости x-z элементарной ячейки. Плоскость (110)пересекает оси x, Y на одинаковом расстоянии и параллельна оси Z. Плоскость (111) пересекает все оси на одинаковом расстоянии от начала координат. Если плоскость отсекает отрицательную ось
Рис 1.6 самолет(010), (110), (111) и(010)в простой кубической ячейке Затем на соответствующей индексной цифре ставится знак минус, например, на рисунке (010). 1.6 Для учета явлений, происходящих в кристаллических телах, введено понятие индикатора направления расположения столбиков атомов в кристаллической решетке. Направление Кристалла проходит через начало координат и узлы кристаллической решетки. Длина ребра единичной ячейки (цикла сетки), как единицы измерения, позволяет определить координаты любой точки в этом направлении.
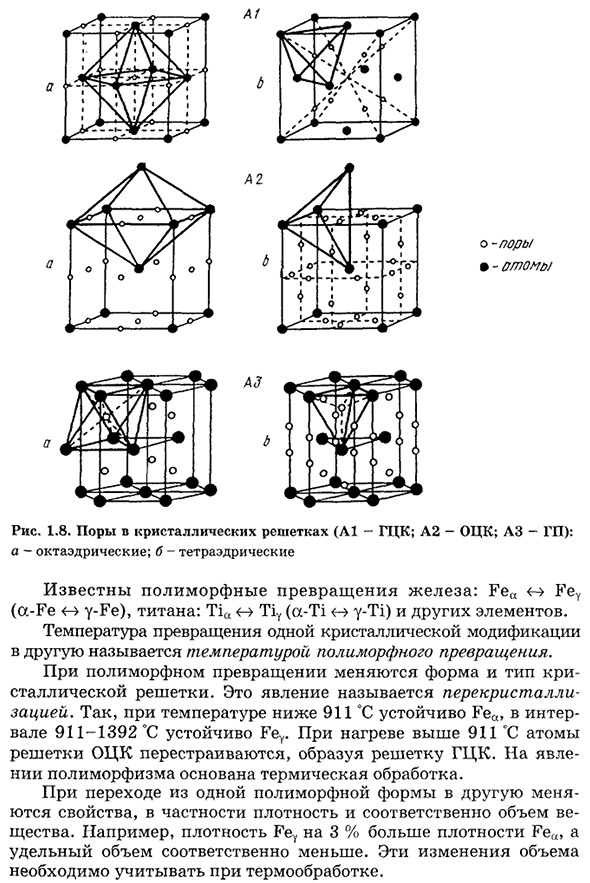
Они обозначаются простыми числами пропорционально координатам выбранных точек по координатным осям, заключенным в квадратные скобки. Их индексы в ориентации кристаллов и простой кубической решетке показаны на рисунке. 1.7 В пространственной решетке, помимо атомов, есть свободное пространство, которое образует поры. Есть октаэдрические и тетраэдрические отверстия. Центр этих пор обозначен маленькой точкой на рисунке. 1.8. Радиус октаэдрической поры ячейки A1 решетки ГЦК с коэффициентом компактности 74% равен 0,41 от радиуса основного атома (Иона), а радиус тетраэдра равен 0,22. Поры локализуются в центре ячейки
А1 и в центре ее ребер. Решетка a2bccc имеет коэффициент сжатости 68%. Радиус отверстия октаэдрического типа (6 в центре плоскости, 12 в центре ребра) равен 0,154 радиуса атома. 24 тетраэдрических типа отверстий, расположенных на поверхности ячейки, могут принимать»чужеродные» атомы с радиусом 0,29 от радиуса атома основного металла. АЗ ГП гриль также имеет коэффициент компактности 74%. Радиус 6 октаэдрических пор и 20 тетраэдрических пор равен g=0,147 каждая? А g=0,2257? А где 7? — Радиус главных атомов клетки. Некоторые металлы могут иметь различные кристаллические решетки при различных температурах. Способность металлов существовать в различных кристаллических формах называется полиморфной или аллотропной. Принято представлять стабильные полиморфные модификации при более низких температурах с индексом a (A-Fe),
более высоким p, затем y и т. д. 1.7 показатель ориентации кристаллов в простых кубических ячейках пространственной решетки 26Д. / б о-поры• — атом/ Рис 1.8. Поры в кристаллической решетке (A1-FCC; A2-BCC; AZ-GP) и октаэдрические B-тетраэдры Известны полиморфные превращения железа: Fe«o FeY (OS-Fe o y-Fe), титана: Tia TiY (a-Ti<->y-Ti) и других элементов. Температура превращения одной кристаллической модификации в другую называется температурой полиморфного превращения. При полиморфных превращениях форма и тип кристаллической решетки изменяются. Это явление называется перекристаллизацией. Таким образом, ВЭД стабилизирован при температуре ниже 911 ° с, ВЭД стабилен в диапазоне 911-1392°С.
При нагревании выше 911 ° с атомы решетки ВСС перестраиваются с образованием решетки ВСС. Термическая обработка основана на явлении полиморфизма. При переходе от одной полиморфной формы к другой характеристика изменяется, в частности, плотность и, соответственно, объем вещества. Например, плотность FeY на 3% больше плотности FetI, а удельный объем соответственно меньше. Эти изменения объема необходимо учитывать при термообработке. 27 полиаморфизм Мартина R британцы explorer. It была одной из причин гибели полярной экспедиции Скотта. Канистры были запечатаны керосином. При низкой температуре белого олова пластика полиморфное превращение происходило с образованием хрупкого порошка серого олова. Топливо пролилось, и в пути экспедиция осталась без топлива.
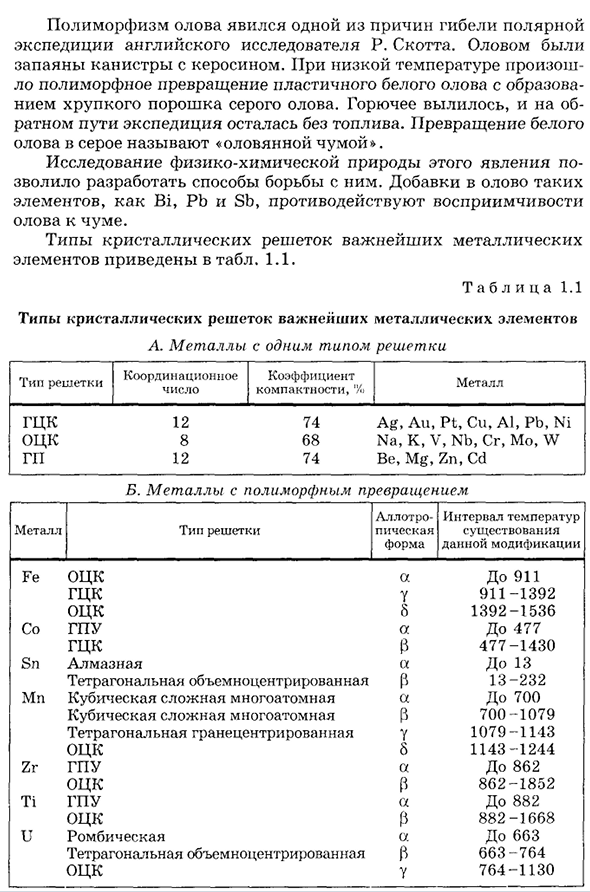
Превращение белого олова в серое называется «оловянной чумой».» Изучение физико-химических свойств этого явления позволило разработать методы борьбы с ним. Добавление к олову таких элементов, как Bi, Pb и Sb, противодействует восприимчивости олова к песто. Типы кристаллических решеток наиболее важных металлических элементов приведены в таблице. 1.1. Типы кристаллических решеток важнейших металлических элементов A. металл с одним видом решетки Т а б л и Ц А1. Один Настройка сетки тип количество Факторы малого размера,%металл HCC12 74Ag, Ас, ст, Си, Ас, ПБ, 68Na ни HCC8,К, В, Н, СГ, МО, ж GP Двенадцать. 74Be, мг, ЗН, КР B. металлы с полиморфными превращениями Металлические решетки типа Изотропная форма Температурный диапазон присутствия этого изменения Fe в ОЦК а911 Федеральная комиссия связи Y911-1392 БЦК 8 1392-1536 Со ГПУ в 477
Федеральная комиссия связи 3 477-1430 SN diamond A13 квадратный объемный Центр 3 13-232Mn кубический комплекс многоатомный a-700 кубический комплекс многоатомный 3 700-1079 квадратный лицевой центр 7 1079-1144bcc 8 1143-1244 Zr GPU до 862 БЦК 3 862-1852 Ti GPU a до 882 БЦК 3 882-1668 U ромб a-663 квадратный объемный Центр 3 663-764 BCC U764-1130 Свойства материалов зависят от природы атомов, из которых они состоят, и сил взаимодействия между ними. Аморфный материал характеризуется хаотическим расположением атомов. Таким образом, их свойства в разных направлениях одинаковы, другими словами, АМ или ф Н С Е М а Тер И Л С и З О Т Р О П Н Ы. в кристаллических материалах расстояния между атомами в разных направлениях кристаллов различны. Например, в ОЦК-решетке кристаллической плоскости, проходящей через грань куба, так как четыре атома вершины принадлежат четырем основным ячейкам (1/4), смежным одновременно, только один атом в то же время, в плоскости, проходящей через диагональ куба, есть возможность, что есть два атома.: 1 + (1/4) −4 = 2.
Из-за неодинаковой плотности атомов в разных направлениях Кристалла наблюдаются различные свойства. Различие свойств кристалла по направлению испытания называется анизотропией. Разница в физико-химических и механических свойствах в разных направлениях может быть очень значительной. При измерении с двумя взаимно перпендикулярными кристаллами цинка величина температурного коэффициента линейного расширения Чжана изменяется в 3-4 раза, а прочность кристалла железа-более чем в два раза. Анизотропия свойств характерна для монокристаллов или так называемых монокристаллов. Большая часть техногенного литого металла, закаленного в нормальных условиях, имеет поликристаллическую структуру. Они состоят из большого количества кристаллов или частиц(рис. 1.9, а). В этом случае отдельные зерна анизотропны.
Различные ориентации отдельных зерен обычно приводят к тому, что свойства поликристаллического металла усредняются. Но Рис 1.9 литье металлических гранул (а) и ориентация кристаллической решетки после обработки давлением(б) Шесть. 29 поликристаллические тела характеризуются квазиизотропной-СПГ-кажущейся независимостью свойств от направления испытания. Квазиизотропия сохраняется в литейном состоянии. При обработке давлением (прокатка, ковка), в частности, без нагрева, большинство металлических частиц приобретают примерно одинаковую ориентацию(так называемую текстуру). 1.9, 6), то металл становится анизотропным. Свойства вдоль и поперек направления основной деформации деформируемого металла могут существенно варьироваться. Анизотропия может привести к дефектам в металле (Рослау, волнистость листа). Необходимо учитывать анизотропию при проектировании и разработке технологии получения деталей.
Смотрите также:
Методические указания по материаловедению
| Дефекты строения кристаллических тел | Возникновение остаточных напряжении |
| Кристаллизация металлов | Общая характеристика металлов и сплавов |

