Оглавление:
Физико-химические свойства растворов
Задача 32.
Вычислить а) температуру кипения, б) температуру замерзания водного раствора, содержащего 0,1 моль сахарозы 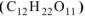 в 500 г раствора.
в 500 г раствора.
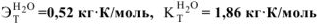

Решение:
а) Температура кипения водного раствора сахарозы рассчитывается по уравнению:
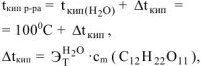
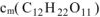 — моляльность сахарозы в растворе, моль/кг.
— моляльность сахарозы в растворе, моль/кг.
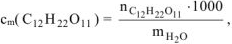
где 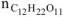 — количество растворенной сахарозы, моль.
— количество растворенной сахарозы, моль.
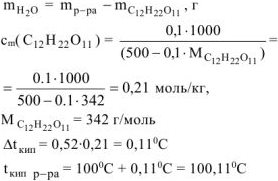
б) Температура замерзания водного раствора рассчитывается по уравнению:
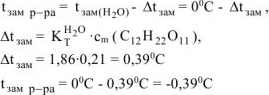
Ответ: 
Задача 33.
В 100 г воды содержится 2,3 г неэлектролита. Раствор обладает при 25°С осмотическим давлением, равным 618,5 кПа. Определить молярную массу неэлектролита. Плотность раствора принять равной 1,05 г/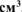 .
.

Решение:
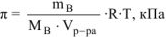
где 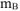 — масса растворенного неэлектролита, г
— масса растворенного неэлектролита, г
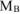 — молярная масса растворенного неэлектролита, г/моль.
— молярная масса растворенного неэлектролита, г/моль.
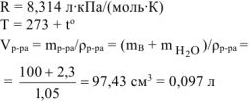
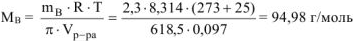
Ответ: молярная масса растворенного вещества равна 94,98 г/моль.
Задача 34.
Определить массу воды, которую необходимо прибавить к 10 г карбамида 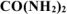 , чтобы давление пара над полученным раствором при температуре 298К составило 3,066 кПа. Давление пара над водой при этой температуре равно 3,166 кПа.
, чтобы давление пара над полученным раствором при температуре 298К составило 3,066 кПа. Давление пара над водой при этой температуре равно 3,166 кПа.
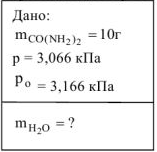
Решение:
Давление насыщенного пара воды над раствором электролита равно:
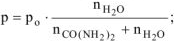
Откуда
где 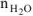 — количество воды, моль;
— количество воды, моль;
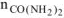 количество карбамида, моль.
количество карбамида, моль.
Откуда 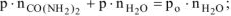
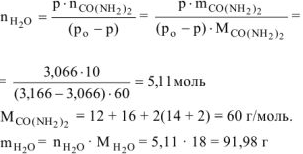
Ответ: 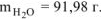 .
.
Задача 35.
Определить давление насыщенного пара воды над 0,05 М раствором хлорида кальция (р = 1,041 г/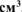 при 301 К, если давление насыщенного пара над водой при этой температуре равно 3,78 кПа. Кажущаяся степень диссоциации хлорида кальция равна 0,85.
при 301 К, если давление насыщенного пара над водой при этой температуре равно 3,78 кПа. Кажущаяся степень диссоциации хлорида кальция равна 0,85.

Решение:
Давление насыщенного пара воды над раствором электролита равно:
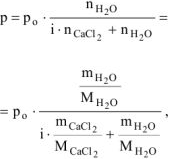
где 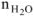 — количество воды, моль,
— количество воды, моль,
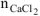 — количество
— количество 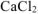 , моль
, моль
i — изотонический коэффициент.
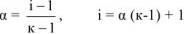
где 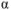 — кажущаяся степень диссоциации
— кажущаяся степень диссоциации 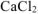
к — общее количество ионов, образующихся при полной диссоциации одной молекулы 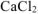 .
.

откуда 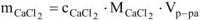 , r
, r
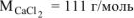
Для расчета берем 1л раствора
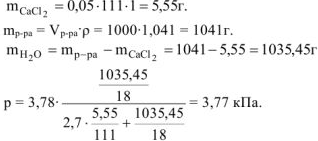
Ответ: давление насыщенного пара над раствором равно 3,77 кПа.
Задача 36.
Определить осмотическое давление 1,5% раствора карбоната натрия при 25°С. Плотность раствора равна 1,015 г/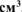 . Кажущаяся степень диссоциации карбоната натрия равна 0,9.
. Кажущаяся степень диссоциации карбоната натрия равна 0,9.

Решение:
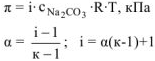
где 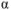 — кажущаяся степень диссоциации,
— кажущаяся степень диссоциации,
к — общее количество ионов, образующихся при полной диссоциации одной молекулы 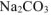
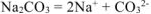
к = 3, тогда 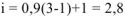
c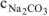 — молярная концентрация
— молярная концентрация 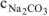 , моль/л
, моль/л
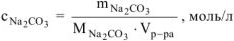
В 100 г 1,5%-ного раствора содержится 1,5 г 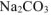
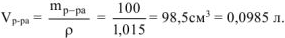
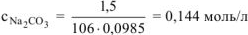
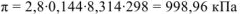
Ответ: осмотическое давление 1,5% раствора 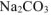 равно 998,96 кПа.
равно 998,96 кПа.
Задача 37.
Определить кажущуюся степень диссоциации соли, если водный раствор хлорида алюминия с массовой долей 1,5% кристаллизуется (замерзает) при температуре (-0,69°С).
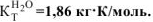

Решение:
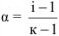
где к — общее количество ионов, образующихся при полной диссоциации одной молекулы 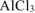
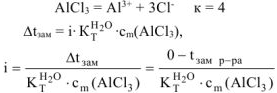
где 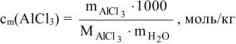
В 100 г 1,5%-ного раствора содержится 1,5г 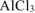 и 98,5 г воды. 1,5-1000
и 98,5 г воды. 1,5-1000
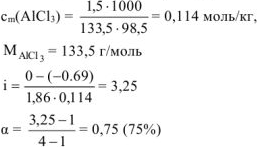
Ответ: кажущаяся степень диссоциации 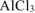 равна 0,75(75%).
равна 0,75(75%).
Эти задачи взяты со страницы готовых задач по предмету химия:
Возможно эти страницы вам будут полезны:

