Оглавление:



Физические свойства равновесно диссоциирующего газа
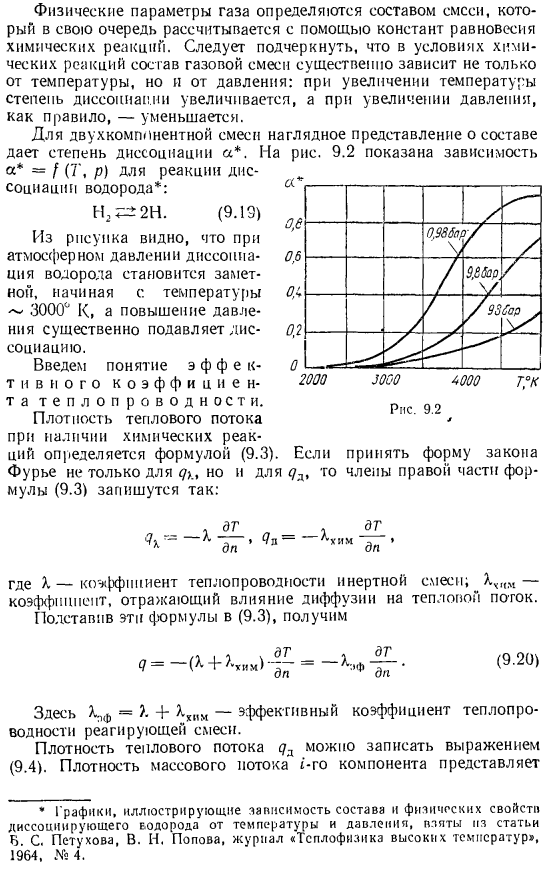
- При оценке теплообмена реакционной смеси, необходимо учитывать изменения физических параметров газа во всей системе. Поэтому перед расчетом теплопередачи необходимо оценить зависимость реакционной смеси от физических параметров температуры или от общей энтальпии. Физические параметры газа определяются составом смеси. Состав смеси рассчитывается с использованием константы равновесия химического вещества reaction.
Химические реакции, состав газовой смеси практически не зависят только、 Температура, но степень диссоциации От давления: когда температура повышается, температура повышается, и когда давление повышается、 Как правило, она уменьшается. Для двухкомпонентной смеси, визуальное представление состава При наличии химических реакций Она определяется по формуле (9.3). «y», а такжеДля D, также принимающего форму правила Фурье, член в правой части выражения (9.3) может быть записан как: X — теплопроводность инертных смесей. Х » ₁М-коэффициент, отражающий влияние диффузии на тепловой поток.
Решение уравнения потока довольно простое и указывает, что в установившемся потоке кривая распределения скорости имеет форму параболы. Людмила Фирмаль
Если вы подставите эти выражения в (9.3)、 (9.20 утра)) Где= X4-X, im-эффективный коэффициент теплопроводности реакционной смеси. Плотность теплового потока D можно описать выражением (9.4). массовая плотность потока I-го компонента равна Диссоциация водорода от температуры и давления, пластины от изделий 5. С. Петухова, В. И. Попова, журнал высокотемпературной теплофизики, 1964, № 4. Является результатом взаимодействия этого компонента со всеми другими компонентами газовой смеси и выражается в Формуле*.
- Где m(и m — 1-й компонент и молекулярная масса смеси; — коэффициент диффузии многокомпонентной смеси; C / — концентрация 1-го компонента. Коэффициент диффузии многокомпонентной смеси O сильно зависит от химического состава смеси, в отличие от коэффициента диффузии двухкомпонентной смеси Oy. Коэффициент диффузии бинарной смеси является частным случаем коэффициента диффузии многокомпонентной смеси при N = 2. Коэффициент диффузии многокомпонентной смеси вычисляется из коэффициента диффузии бинарной смеси с использованием определителя (31.
Подставляя формулу (9.21) в (9.3), можно получить многокомпонентную газовую смесь (9.22) Если сравнить формулу (9.20) с формулой (9.22)、 ОД В локальном химическом равновесии (9.23) _ ДС, ДТ, ДП д ДП ’ (9.24) Следовательно, формула Теплопроводность смеси инертных газов рассчитывается исходя из теплопроводности компонента 1191.In у некоторых веществ бинарный коэффициент диффузии имеется в 21 (но в большинстве случаев их необходимо оценивать на основе молекулярной теории строения газа). * Д-Хиршфельдер. Проблемы почвы» На рис. 9.3 показана зависимость диссоциации водорода в локальном химическом равновесии, полученная расчетным путем, X₄f= /(G, p).Судя по рисунку, зависимость X..
Затем некоторые члены в этом уравнении могут быть опущены вследствие особых условий, имеющих место в цилиндрической трубе с полностью установившимся потоком. Людмила Фирмаль
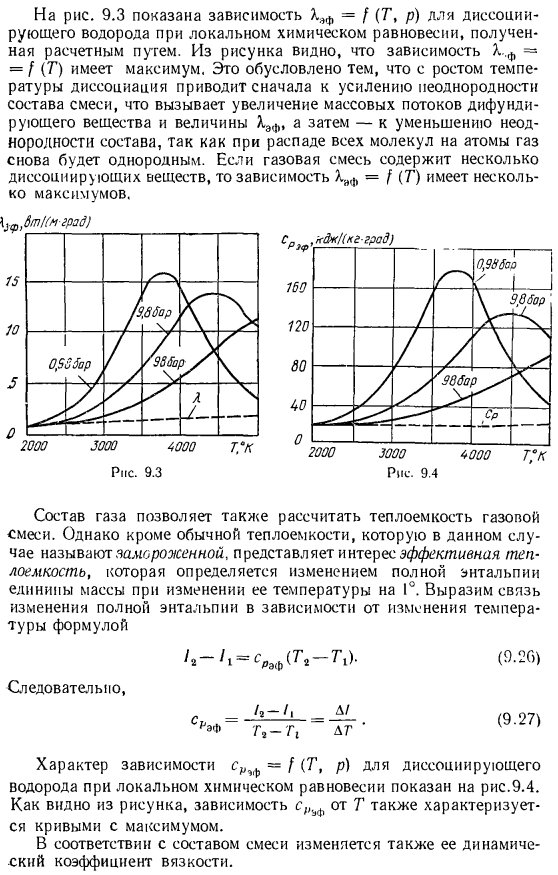
Вы можете видеть, что f = = I (T) является самым большим. Это связано с ростом Диссоциация сначала приводит к увеличению неоднородности состава смеси, что вызывает увеличение массового потока и величины Heff диффундирующего вещества, а затем к уменьшению неоднородности состава, поскольку при распаде всех молекул на атомы газ снова становится однородным. Если смешанный газ содержит некоторое диссоциирующее вещество, то зависимость Haf = [(T) имеет несколько максимальных значений. Рассчитайте теплоемкость газа в конкретном случае По составу газа г.— Смесь.
Правда, помимо нормальной теплоемкости. Они называются низкими температурами, поэтому важна эффективная теплоемкость. Это определяется изменением общей энтальпии единицы массы при изменении температуры на 1°.Выражаем отношение изменения полной энтальпии к изменению температуры уравнением Так… /,-/,= ^(7,-Л). 1, −1, Д / S’E * T, — T, DT (9.26) (9.27) Зависимость средней природы, f=! (Т, п) диссоциации водорода в локальном химическом равновесии показаны на рисунке 9.4.Зависимость ₍C и Эф на Т это тоже характеристика. Самая большая кривая.
Смотрите также:

