Оглавление:
Электролиз растворов
Таблица 11.1. Процессы протекающие на катоде при электролизе водных растворов
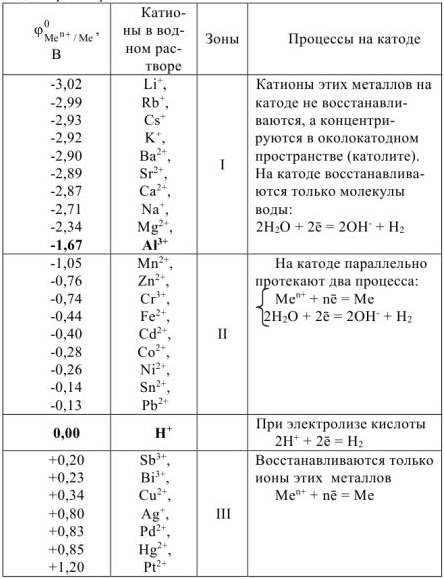
Таблица 11.2. Последовательность окисления анионов на инертном аноде в водном растворе.
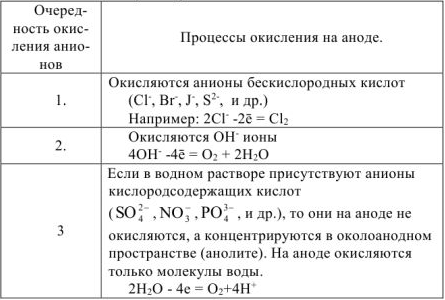
Примечание. Если анод изготовлен из металлов II или III зоны (растворимый анод), то при электролизе протекает только процесс его растворения 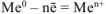
Задача 60.
Составить схемы электролиза и написать уравнения электродных процессов водных растворов (анод инертный): а) хлорида меди (II), б) гидроксида натрия.
Какие продукты выделяются на катоде и аноде?

Решение:
a) 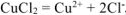 ,
,
Схему электролиза составляем в соответствии с таблицами 11.1 и 11.2:
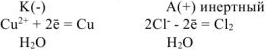
На катоде выделяется 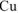 , на аноде выделяется
, на аноде выделяется 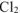 .
.
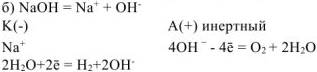
На катоде выделяется 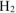 , на аноде выделяется
, на аноде выделяется 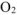 .
.
Задача 61.
Составить схемы электролиза и написать уравнения электродных процессов водного раствора сульфата никеля (II) , если: а) анод инертный, б) анод никелевый. Какие продукты выделяются на катоде и аноде?

Решение:
а) анод — инертный
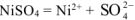
Схему электролиза составляем в соответствии с таблицами 11.1. и 11.2:
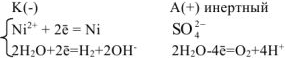
На катоде выделяется 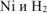 , на аноде выделяется
, на аноде выделяется 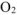 .
.
б)анод — никелевый:
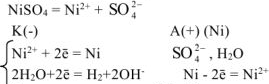
Нa катоде выделяется 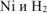 , на аноде растворяется
, на аноде растворяется 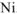 .
.
Задача 62.
При электролизе растворов а) нитрата кальция, б) нитрата серебра на аноде выделяется 560 мл газа (н.у.). Составить схему электролиза и написать уравнения электродных процессов. Определить какое вещество и в каком количестве выделилось на катоде? Анод инертный.

Решение:
a) 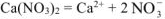
Схема электролиза:
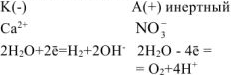
На катоде выделяется 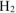 , на аноде выделяется
, на аноде выделяется 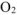
По закону эквивалентов: 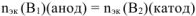
В соответствии со схемой электролиза:
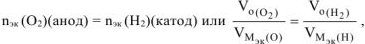
откуда
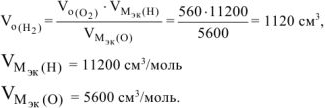
На катоде выделилось 1120 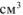 водорода.
водорода.
Ответ: 1120 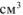 водорода.
водорода.
б) 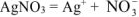
Схема электролиза:
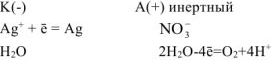
На катоде выделяется 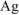 , на аноде выделяется
, на аноде выделяется 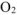 .
.
По закону эквивалентов: 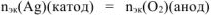 или
или 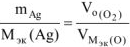 , откуда
, откуда 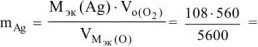 10,8 г.
10,8 г.
где 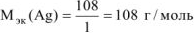
На катоде выделилось 10,8 г серебра.
Ответ: 10,8 г серебра.
Задача 63.
Составить схему электролиза и написать уравнения электродных процессов водного раствора сульфата калия (анод инертный). Определить какие вещества и в каком количестве выделяются на катоде и аноде, если проводить электролиз в течение четырех часов при силе тока 2А. Температура 298К, давление 99 кПа.

Решение:
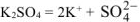
Схема электролиза:
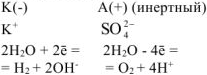
На катоде выделяется 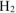 , на аноде выделяется
, на аноде выделяется 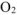
По закону Фарадея объемы водорода и кислорода, выделившиеся при (н.у.):
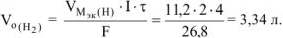
где 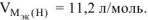 .
.
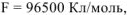 если
если 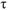 — сек,
— сек,
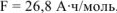 , если
, если 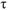 — час.
— час.
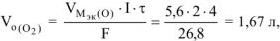
где 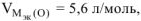 т.е.
т.е. 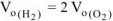
Объем водорода при заданных условиях отличных от нормальных определяем из уравнения:
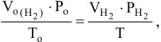
откуда: 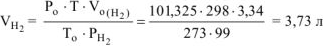
Объем кислорода при заданных условиях:
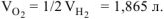
Ответ: 3,73 л водорода, 1,865 л кислорода.
Задача 64.
Металлическую деталь, площадь поверхности которой равна 100 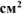 , необходимо покрыть слоем электролитически осажденной меди из раствора хлорида меди (II). Составить схему электролиза и написать уравнения электродных процессов, если анод медный. Сколько времени должно длиться осаждение при силе тока 8А и выходе по току 98%, если толщина покрытия 0,15 мм. Плотность меди — 8,9 г/
, необходимо покрыть слоем электролитически осажденной меди из раствора хлорида меди (II). Составить схему электролиза и написать уравнения электродных процессов, если анод медный. Сколько времени должно длиться осаждение при силе тока 8А и выходе по току 98%, если толщина покрытия 0,15 мм. Плотность меди — 8,9 г/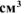 .
.

Решение:
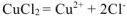
Схема электролиза:
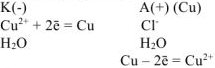
На катоде выделяется 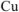 , на аноде растворяется
, на аноде растворяется 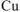 .
.
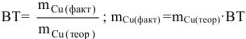
По закону Фарадея с учетом выхода по току (ВТ) масса меди, фактически выделившейся на катоде равна:
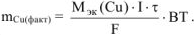
Масса меди, необходимая для получения медного покрытия:
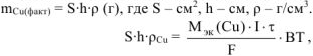
откуда
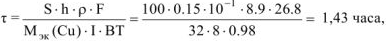
где 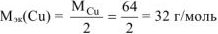
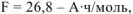
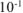 — коэффициент пересчета мм в см.
— коэффициент пересчета мм в см.
Ответ: 1,43 часа.
Задача 65.
Определить молярную концентрацию эквивалента раствора нитрата серебра, если для выделения всего серебра из 75 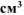 этого раствора потребовалось пропустить ток силой 4А в течение 25 минут. Составить схему электролиза и написать уравнения электродных процессов. Анод инертный. Выход по току серебра 100%.
этого раствора потребовалось пропустить ток силой 4А в течение 25 минут. Составить схему электролиза и написать уравнения электродных процессов. Анод инертный. Выход по току серебра 100%.

Решение:
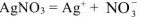
Схема электролиза:
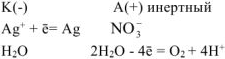
На катоде выделяется 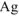 , на аноде выделяется
, на аноде выделяется 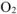 .
.
Молярная концентрация эквивалента раствора 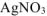 :
:
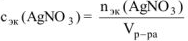
По закону эквивалентов: 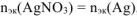 ,
,
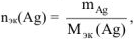
где 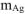 — масса серебра, выделившегося при электролизе с учетом 100 % выхода по току.
— масса серебра, выделившегося при электролизе с учетом 100 % выхода по току.
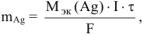 , откуда
, откуда
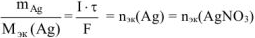
Молярная концентрация эквивалента раствора 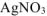 :
:
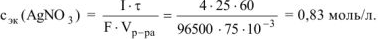
где 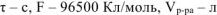 .
.
60 — коэффициент пересчета мин. в сек.
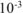 — коэффициент пересчета
— коэффициент пересчета 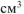 в л.
в л.
Ответ: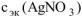 = 0,83 моль/л.
= 0,83 моль/л.
Эти задачи взяты со страницы готовых задач по предмету химия:
Возможно эти страницы вам будут полезны:

