Оглавление:







Энтропия.Второе начало термодинамики для случая большого числа нагревателей и холодильников.
- Энтропия § ’ м Второй закон термодинамики Для большого количества нагревателей Холодильник 2-е количественное выражение 6) начало термодинамики формы Д、 1 рабочая жидкость, 1 цикл 1 холодильник с обогревателем. Давайте максимально обобщим второй закон термодинамики Частое явление в природе и практике Большое количество обогревателей и холодильников. Запись 6) в слегка измененном виде. 0 * 2 \ ^ 2 0 * 2 ~~ 7 — \ — ^ ^ «t *’ * или t VI ’ 1 * 2 Откуда Количество Qi и Q2 соответственно、
Количество тепла, взятого из нагревателя и отданного ho* На лодочниках есть разные знаки. Берется из нагревателя, а другой переносится в холодильник В холодильнике. Я согласен предположить, что Qi положительна, а Q2 отрицательна Ему было присвоено воинское звание.
Учитывая эту ситуацию, не 3 Цикл учитывает 1 цикл с 1 нагревателем И холодильник. Людмила Фирмаль
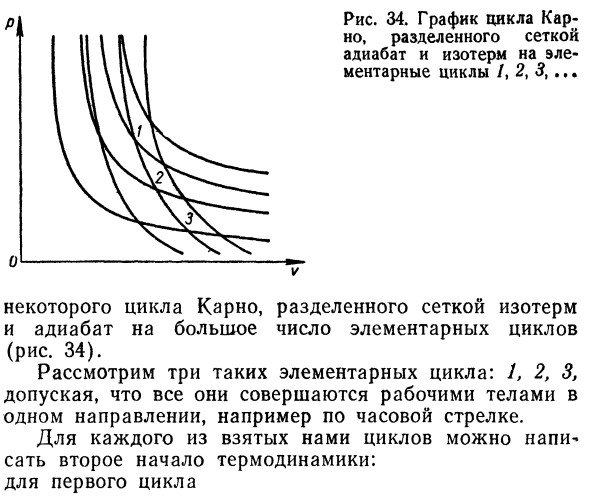
Тогда отношение E, 1) принимает вид: Или TG + 7G < ° — <5 ′ 2> значение-y представляет соответствующую теплоту Это называется температурой, и называется уменьшением тепла. Таким образом, из Формулы Е, 2) можно сделать вывод. 1 подогреватель и 1 в цикл Количество тепла в холодильнике меньше, чем Равный нулю. А теперь представьте себе какой-нибудь рабочий орган. Каждый завершает свой собственный цикл. На графике Этот сложный процесс можно представить следующим образом 8 В. Ф. Ноздрева с рис. 34.График цикла Кар- Но раскол в сетке изотермы над адиабаты и Эле Базовый цикл/, 2, 5,..
Цикл Карно разделен сетью Изотерм Теплоизоляция ряда основных циклов 34). Рассмотрим 3 таких основных цикла: 1, 2, 3、 Предполагая, что они совершаются всеми рабочими органами Одно направление, например, по часовой стрелке. Для каждого выполненного цикла можно написать: Второй закон термодинамики: Первый цикл Для Для Второй Третий. Цикл * ? Цикл 1 2 1 _、^ * || 1-1 И так далее 。 д. Найти сумму всех полученных соотношений. Е, 3) Легко показать, что это не так Члены, связанные с сегментами изотермы* Основной цикл находится в Контакте.
- Действительный* Сто четырнадцать Но вдоль этих сегментов изотермы система Процесс в обратном направлении direction. So … Например, в первом цикле, если рабочая жидкость дает Хо теплотворная способность лодильника Qf2, 2-й цикл Получает такое же количество тепла от нагревателя Q2 ’= SQ\», следовательно, уменьшение суммы общего Теплота изотермы равна нулю. * Подобный Ожидания относительно другой изотермы также могут быть даны.
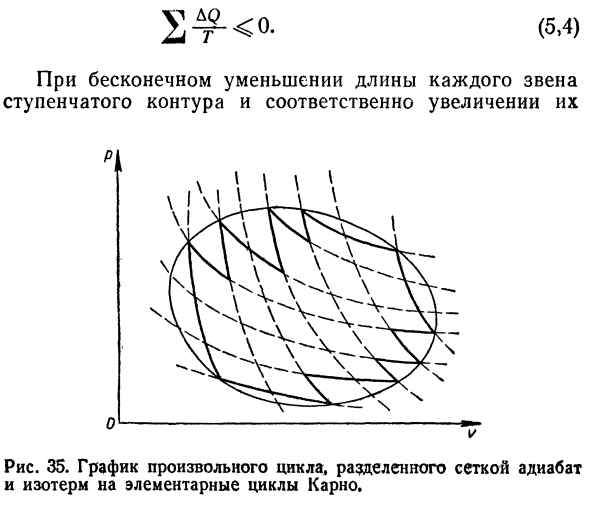
Теперь рассмотрим цикл любой формы Давление и объем Тора непрерывно изменяются(рис. 35)* Потому что температура меняется в этом цикле Продолжая, для него второй закон термодинамики В форме Е, 3) не является applicable. In это дело мы будем ломать Рассматриваемый контур представляет собой сетку Изотерм и теплоизоляции. Можно создать ступенчатые контуры. Для этого Последнего второго закона термодинамики Писать следующим образом: Е, 4) Уменьшите длину каждой ссылки до бесконечности Шагайте по контурам и, соответственно, увеличивайте их ч(ч \ л: Рис.35.
Следовательно, д’у-О. Это происходит потому, что работа, выполняемая обратимым Изотермический цикл равен нулю. Мы рассмотрели закрытый процесс. Людмила Фирмаль
График любого цикла L делится на сетку адиабата Изотерма основного цикла Карно. 8 * 115 Число ступенчатых схем приближается к непрерывному Непрерывный контур и Формула Е, 4) принимает вид: Е, 5) Формула Е, 5) дает количественную формулировку Формулировка второго закона термодинамики в наиболее распространенных случаях Для любого замкнутого контура: кривая dQ Интеграл замкнутого цикла — ^- Для обратимого процесса он равен нулю и меньше или равен нулю В случае необратимых процессов яуля. 5) рассмотрим уравнение, которое применяется к изолятору.
Изотермический замкнутый обратимый цикл: С Т = const Тогда вы можете написать: Но с тех пор И затем… В этом случае d’q = 0 и dt / = O Процесс завершился. Од- Однако на самом деле существует открытый процесс、 Второй закон термодинамики также применим Применимый. Более общая формулировка второго закона Термодинамика, комплексный и открытый процесс、 Вы можете получить его, введя новую концепцию- Энтропия.
Смотрите также:
Решение задач по термодинамике
| Уравнение Клапейрона—Клаузиуса. | Энтропия. |
| Зависимость поверхностного натяжения от температуры. | Энтропия изотермических обратимых процессов. |

