Оглавление:


Экспериментальные значения вязкости газов.
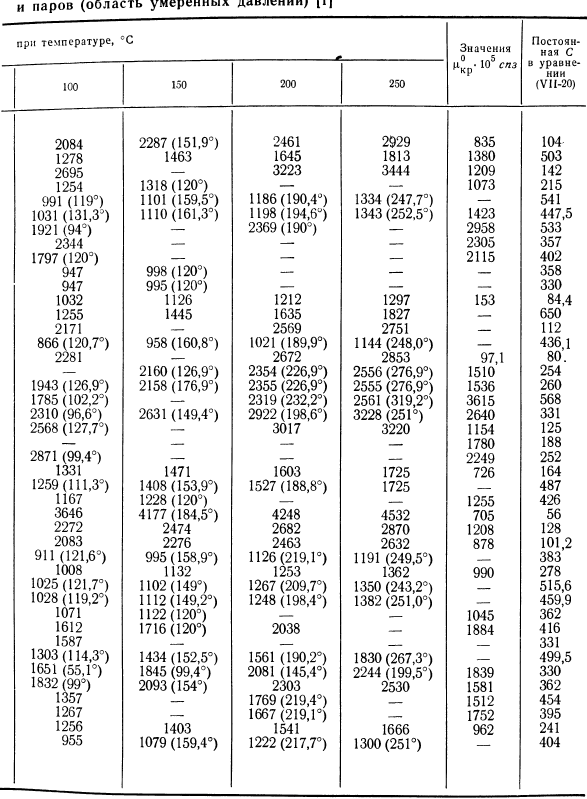
Экспериментальные значения вязкости газов. Вязкость большого количества газов определялась экспериментально в широком диапазоне температур и давлений. Внутри таблицы. УП-4 указывает значение коэффициента кинематической вязкости Р°газа и пара для конкретного вещества, а также значение константы с уравнения Сазерленда(УП-20). значение Р0 дан для некоторых температур и критическая температура(PKR в гр). Если вязкость определяется при различных температурах, то измеренная температура указывается в скобках. Значения коэффициента кинематической вязкости газа в интервале температур 0-1000°с приведены в таблице. УП-5.
Широкий спектр экспериментальных данных по вязкости газа был собран по монографии Голубева. Людмила Фирмаль
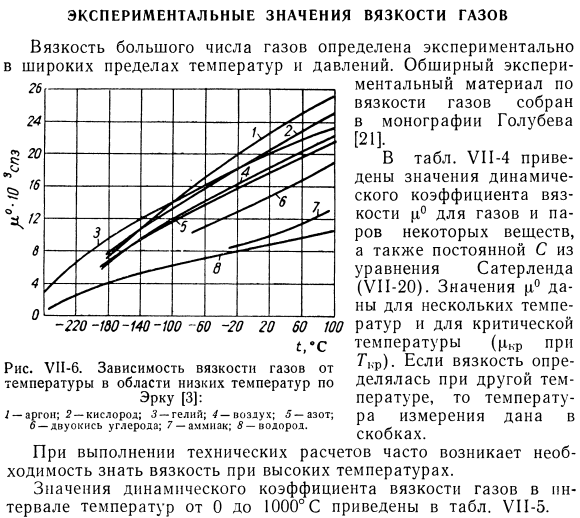
- Когда температура повышается от 0 до 1000°C, p°повышается примерно в 3-4 раза. Для учета влияния температуры на вязкость газа можно использовать формулу Сазерленда (VI1-20).Однако вы должны помнить константы Сазерленда C, показанные в таблице. УП-4 чаще всего относится к температурному диапазону от 0 до 300°С. UP-6 показано на рисунке(область низких температур). Согласно кинетической теории газа, вязкость не должна зависеть от давления. Ведь, например, про воздух приобрели[1: Где с-вязкость воздуха при давлении р при температуре 15°С. Вязкость воздуха при давлении М-0-15°С при температуре 1 Из приведенных выше данных видно, что отклонение наблюдается только в области очень низкого давления (меньше или равно порядка 2 мм рт. ст.).
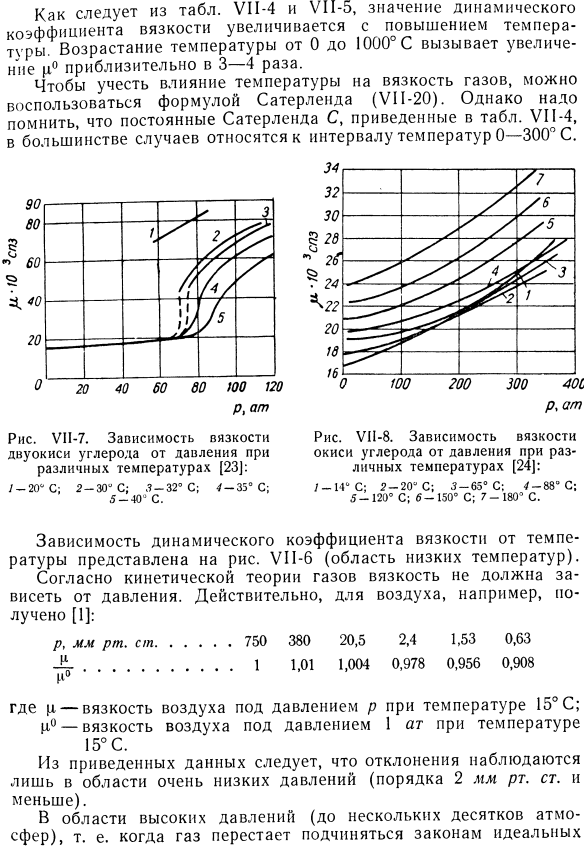
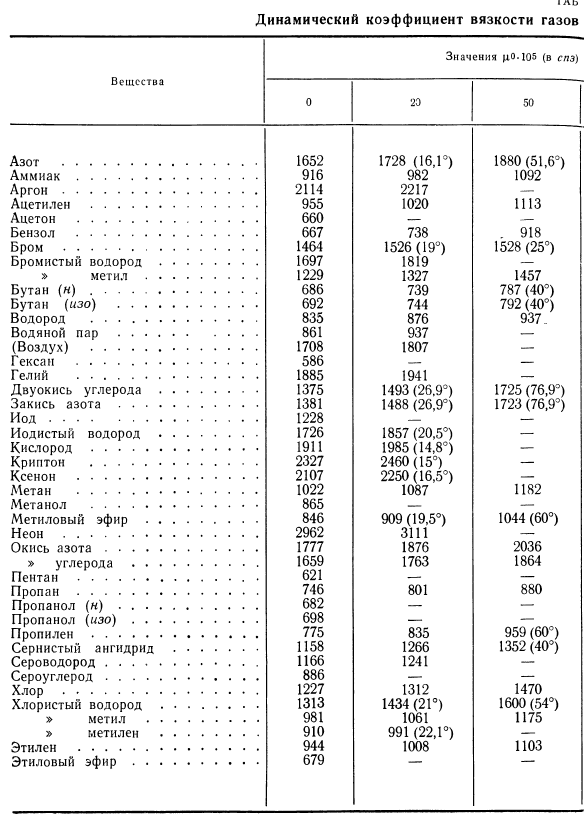
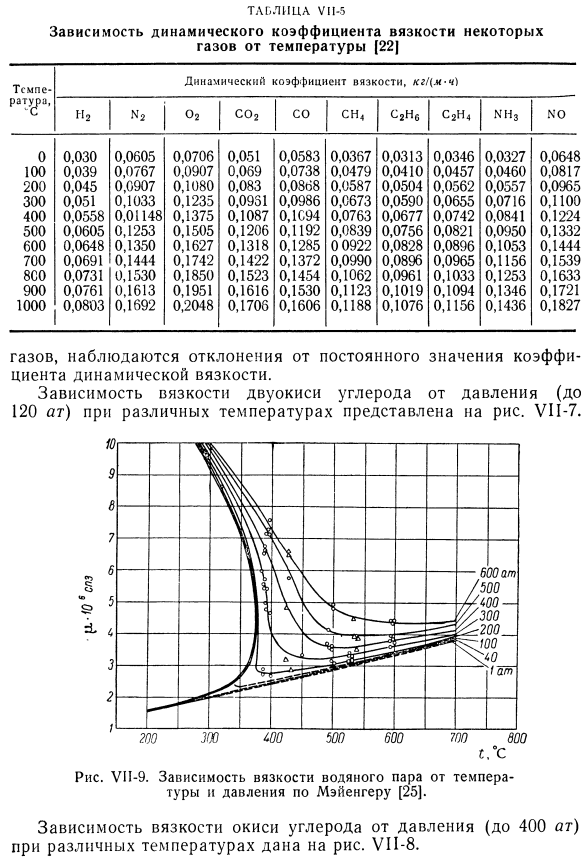
- Области высокого давления(до нескольких десятков атмосфер), то есть, когда газ перестает подчиняться законам идеального Кинематическая вязкость газа И пара (зоны умеренного давления/ Таблица VI1-5 Зависимость некоторых коэффициентов кинематической вязкости Газ от температуры(22 | Наблюдается отклонение от постоянного значения коэффициента кинематической вязкости газа. На рисунке показана зависимость давления вязкости углекислого газа при различных температурах (до 120 Ат). УП-7. Рисунок UI-9. По мнению Мейенгера, зависимость вязкости водяного пара от температуры и давления (25). На рисунке показана зависимость вязкости монооксида углерода при различных температурах от давления (до 400 атмосфер). UI-8. VII от фиг.? Так, вязкость углекислого газа в большом диапазоне давлений(до 60-70 атмосфер) практически не зависит от pressure. As температура повышается, давление начинает отклоняться от определенного значения.
Зависимость вязкости водяного пара от температуры и давления показана на рисунке. Людмила Фирмаль
- При превышении определенного давления вязкость газа начинает быстро увеличиваться с увеличением pressure. At при высоком давлении, при высокой температуре вязкость газа увеличивается с повышением температуры, а при низких температурах, когда температура повышается, вязкость уменьшается (в результате изотермы пересекаются на рисунке UN-8). Учитывая, что Формулы (UN-15) и (UP-16) были выведены в предположении столкновения только 2 молекул в системе, отклонение от наблюдаемой вязкости объясняется на основе кинетической теории газа. Однако при низком давлении число столкновений молекул и стенок увеличивается, что усложняет механизм явления, в результате чего наблюдается deviations. At высокое давление, обусловленное взаимным сближением молекул, взаимным притяжением молекул и увеличением столкновения 3 молекул начинают оказывать большое влияние на вязкость.
Смотрите также:
Возможно эти страницы вам будут полезны:

