Оглавление:




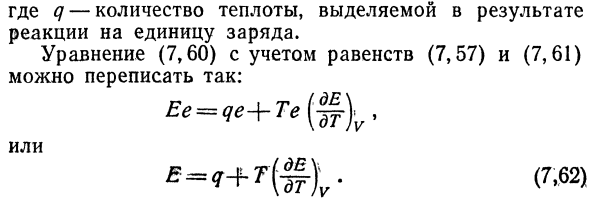




Свободная энергия и максимальная работа.
- Свободная энергия и максимальная производительность. Уравнение Гиббса Гельмгольца Необратимые изотермические свойства Формат технологического соотношения G, 44) имеет вид: Даллас, г, 49) Увеличение свободной энергии В этом случае в системе выполняется меньше работы. Если формула G, 45′) интегрирована Начальное и конечное состояние системы、
Тогда можно определить работу W = Fi-F2. Необратимый процесс Вт> Ф2-ФВ Это следует Получается, что при заданном состоянии оно обратимо Процесс между этими условиями. Макс. Максимальная работа равна разнице в свободной энергии. Эти 2 Государства: Ш Ф-Ф Макс — * 1l2 * 11 В. Ф.
Самая большая работа, которую может сделать система Совершить при изотермическом процессе между 2 Людмила Фирмаль
Ноздрев 161 найти уравнение максимальной работы. Для этого Используйте уравнение Гиббса Гельмгольца. Легко получить из объединения формул G, 9) и G, 12) Формат такой: Предположим, что система переходит изотермически Из одного состояния в другое. Затем%первый и государства м : Л-С + Р ^. GD)) И во 2-м государстве: (^). Г, 50 ’)
Найдите разницу в свободной энергии в 2-х состояниях. Равный максимальному процесс работы: Ш ^ ^ ф — ф ^ У. — У. + т ^ ф — ф ^ г, г, 51) Или ВДМ = — А(/ + Т(^ П») К, Г, 52) Куда? С самого начала процесса равенства Форма термодинамики (B, 9) является: Или Гв ^ У2-Уи = dU1 г, 53)
- Тогда, если вы присваиваете значение dU равенству G, то 51)、 。 Г, 54) Уравнение G, 54) называется максимальным уравнением* Ноя work. It устанавливает взаимосвязь между теплотой и Эффект и максимальная реакция во время определенной работы* Т и в *
Электродвижущая сила гальванического Элементы Посмотрите на соотношение гальванической ЭДС. Элементы, характеризующие другие параметры
Как пример использования свободы* Энергия для решения термодинамической задачи Людмила Фирмаль
Состояние системы. Рассмотреть дело В случае обратимого изотермического процесса. Писать Выражение работы гальванического элемента: d’w = Ede, G, 55) Где E-электродвижущая сила элемента, e-электрический заряд、 Он протекает через цепь во время изотермического процесса. Принимая во внимание уравнение G, 45), получим: ДФ = — Эде> г, 56) Или Форекс-Ф2 = УО, Г, 57)
То есть работа, выполняемая гальваническими элементами、 Равна разности между 1-й и 2-й свободной энергией Состояние it. To найдите эту разницу、 Уравнение Гиббса-Гельмгольца для обоих состояний: Г, 58) Г, 59) \ В / г Отсюда ФЛ-Р2 ^ = Ул-У2 — \ — ТВт (ФЛ-Ф2) В. Г, 60) Мы покажем Ул-У2 = = qе, г, 61) Где q-количество тепла, выделяющегося в результате Реакция на единицу заряда. Уравнение G, 60)уравнение G, 57) и G, 61)
Вы можете переписать его следующим образом. Разница выражает количество E и Q через Ф4-Ф2、 из равенства q1-u2a G, 57)- FF G, 63) Е И из равенства G, 61) д.- ^=^= Г, 64) Из Формулы G, 62), G, 63), G, 64) мы видим: ДТ) г-С-он =} [(Ля.^- ( ^ — ^)]. Г, 65) И я думаю, что F = U-TS、 Мы получаем: Или Где S2-5i-разность между конечной и начальной энтропией Состояние гальванической батареи. T = Const для интегрирования выражения d ’ Q = TdS、
Присвоить результат равенству G, 66) и, наконец, Мы получаем: 2Л \ — ВОПРОС WJv-e• Где Q-количество тепла, которое получает элемент Термостат. е. д. с гальванической Если гальванический элемент увеличивается, т. е.-> 0, то количество Электричество работает потому что тепло положительное Химическая энергия элемента
Приток тепла от термостата. — dtr-для <0, Q <0.In этот случай, часть химиката Химическая энергия элемента выделяется в виде тепла、 Подойдите к термостату. Сто шестьдесят четыре Поэтому, используя термодинамику Связь между параметрами способа, гальваническая Пустой элемент. Потому что очень много химических реакций Изотермически свободная энергия используется особенно часто Используется в химической термодинамике.
Смотрите также:
Решение задач по термодинамике
| Соотношение взаимности. | Свободная энергия равновесных систем. |
| Физический смысл понятия свободной энергии. | Тепловая функция. Эффект Джоуля Томсона. |

