Оглавление:


Потери работоспособности (эксергии) потока
- Канал на входе из параметров ИС, Т, И г, есть канал выходного параметра иг, иг,$₂, г, г-рабочая жидкость установившегося потока считать. Параметры окружающей среды: ₀, 5, 5, Т», р₀ и₀₀. Максимальный объем работы, который поток может произвести при отсутствии равновесия с окружающей средой, должен увеличиваться на величину, затраченную на преодоление давления окружающей среды. Р1Щ-Р 1 — » 1(Р1-Ро)- значение o (p₀-p₀) представляет операцию выталкивания в окружающую среду.
Итак, с учетом формулы (17.5), работа единицы массы установившегося потока в результате обратимого перехода из состояния 1 в состояние о 1м («1—» о) — Ро(o₀— 1) — тай («1-5₀» + » 1(П1 — по)= = ( » .+Р1 «1) — (о+Ро» о)( «、-«»)=(Ч — о) — ’ Го («1-V (17.17) Если кинетическая энергия потока и> / 2 имеют значения, которые нельзя игнорировать, а?₀ =О / w. x = W-o +(w | / 2) — T₀ (%- 5o). (17.18) Из формул (17.17), (17.18) видно, что максимальный объем работы является функцией, специфичной для состояния системы, зависящей от начальных параметров и параметров окружающей среды.
Количественная оценка того факта, когда поток пограничного слоя можно считать квазистационарным, теперь может быть сделана путем сравнения первого члена в уравнении (6-16) со вторым членом. Людмила Фирмаль
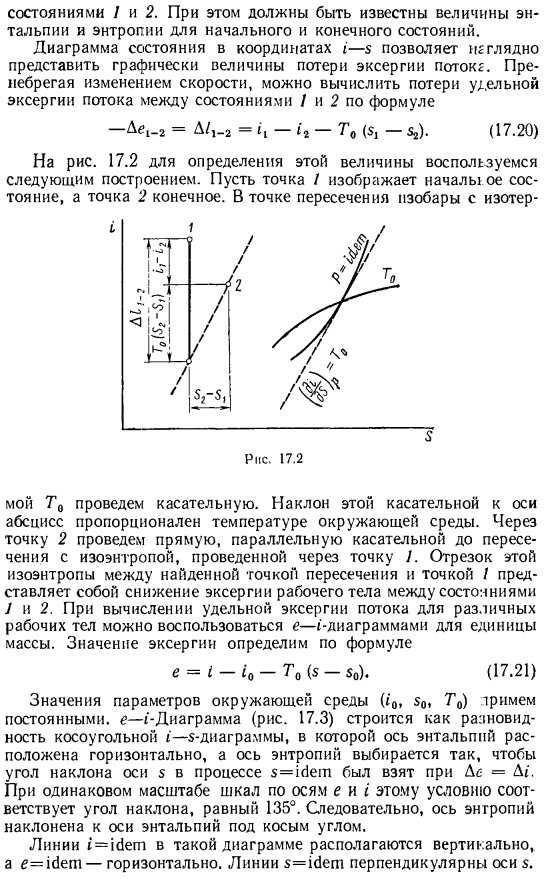
Ухудшение производительности между состояниями/и 2 вдоль пути стабильного потока является 。 (17.19) Величина этого снижения по сравнению с работой, выполненной в среде вне потока, является мерой необратимости термодинамических процессов Интер-адиабатических В этом случае значения энтальпии и энтропии начального и конечного состояний должны быть известны. Диаграмма состояния в координатах 1-3 позволяет визуально визуализировать величину потерь Эксергетического потока. Если вы игнорируете изменение скорости, вы можете рассчитать призрачную потерю Эксергии потока между уравнением/и 2. — Де-Г = Д/, −2= -»», — Т» ($, -$.).
- Рисунок 17.2 чтобы определить это значение, используйте следующую конфигурацию: предположим, что точка/представляет начальное состояние, а точка 2-конечное состояние. Пересечение Изобар и Изобар Рисунок 17.2 Затем нарисуйте касательную. Наклон этой касательной к абсциссе пропорционален температуре окружающей среды. Через точку 2 Проведите линию, параллельную касательной пересечения с изэнтропией, проведенной в точке 1.Это сегмент энтропии между найденным пересечением и точкой / состоянием/и 2.Е- » — использует цифру единицы массы. Величина Эксергии определяется по формуле e = 1-T₀ (s-$₀). (17.21) Параметры окружающей среды ( ₀₀ , ₀₀, то) постоянны. e — — — диаграмма рис.
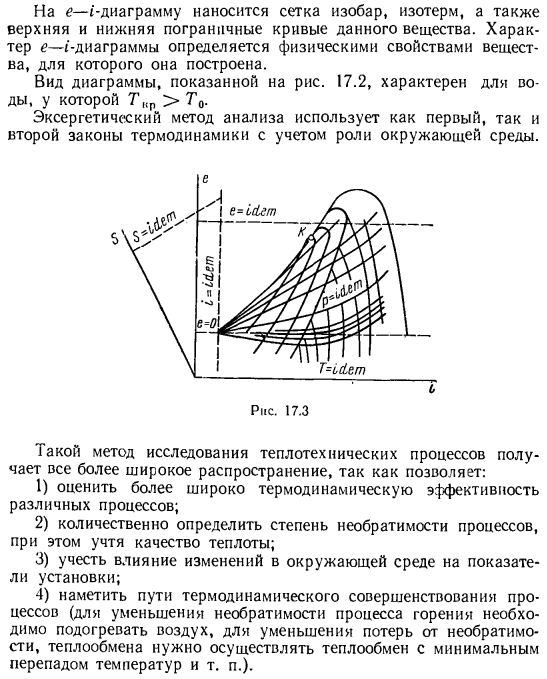
Построена как своего рода косая-ось энтальпии 5 горизонтальна, ось энтропии-наклон оси процесса угла 5$ = 1 1e1n, Di = D «’был взят. если масштаб вдоль осей e и ям одинаков, то это условие соответствует углу наклона 135°. в результате ось энтропии наклоняется под косым углом к оси энтальпии. Линия a = |(1et на этом рисунке расположена вертикально, а e = 1de-горизонтально. Линия 5 = 1 1et перпендикулярна оси 5. Верхняя и нижняя граничные кривые изобарных, изотермических и специфических веществ изображены на е — (- диаграмме).e — (- характер диаграммы определяется физическими свойствами вещества, к которому она построена.
Кроме того, один из двух членов вязкости в оставшемся уравнении количества движения также опущен. Людмила Фирмаль
Характеристики воды, которая является В методе Эксергетического анализа используются как первый, так и второй законы термодинамики, учитывающие роль окружающей среды. е — » д? Л> / \ — Л Один 1 = 0 Рисунок 17.3 Этот метод исследования теплотехнических процессов получает все большее распространение, поскольку позволяет: 1) более широко оценить термодинамическую эффективность различных процессов. 2) количественно оценить степень необратимости процесса, рассматривая при этом качество теплоты. 3) рассмотрите влияние изменений в окружающей среде на производительность установки.
Смотрите также:
| Максимальная работа. Эксергетический метод исследования | Химическая термодинамика |
| Потери работоспособности в циклах | Первый закон термодинамики и применение его к химическим процессам |

